
- •Учебно-методические разработки для самостоятельной работы студентов по курсу «Теоретические основы защиты окружающей среды»
- •Часть II
- •Специальные методы очистки сточных вод и основные методы сепарации твердых отходов
- •Введение
- •Глава 1. Химические методы очистки сточных вод
- •1.1 Нейтрализация
- •1.1.1. Нейтрализация смешиванием
- •1.1.2. Нейтрализация добавлением реагентов
- •1.1.3. Нейтрализация фильтрованием кислых вод через нейтрализующие материалы
- •1.2. Нейтрализация кислыми газами
- •1.2.1. Окисление и восстановление
- •1.2.2. Окисление пероксидом водорода
- •1.2.3. Окисление кислородом воздуха
- •1.2.4. Озонирование
- •Контрольные вопросы
- •Глава 2. Явление осмоса и его использование при очистке сточных вод
- •2.1. Осмотическое давление
- •2.2. Биологическая роль осмотического давления
- •2.3. Законы осмотического давления
- •2.4. Термодинамика осмотического давления
- •Контрольные вопросы
- •Глава 3. Физические основы электродных процессов при очистке сточных вод от примеси
- •3.1. Явления электролиза, поляризации и перенапряжения
- •3.1.1 Электролиз
- •3.1.2. Кривая напряжения
- •3.1.3. Электродвижущие силы разложения
- •3.1.4. Потенциал разложения
- •3.1.5. Концентрационная поляризация
- •3.1.6. Деполяризация
- •3.1.7. Перенапряжение
- •3.2. Электрокапиллярные явления
- •3.2.1. Зависимость поверхностного напряжения от заряда
- •3.2.2. Влияние адсорбции на электрокапиллярную кривую
- •3.2.3. Проблема абсолютных потенциалов
- •3.3. Электрокинетические явления
- •3.3.1. Диффузионный двойной слой и электрокинетический потенциал
- •3.3.2. Емкость двойного слоя
- •3.3.3. Электроосмос
- •3.3.4. Потенциал течения
- •3.3.5. Электрофорез
- •3.3.6. Потенциалы осаждения
- •3.4. Электрохимические методы очистки сточных вод
- •3.4.1. Анодное окисление и катодное восстановление
- •3.4.2. Электрокоагуляция
- •3.4.3. Электрофлотация
- •3.4.4. Электродиализ
- •Контрольные вопросы
- •Глава 4. Физические основы процессов переработки твердых бытовых отходов
- •4.1. Процессы измельчения и дробления
- •4.1.1. Назначение операций дробления и измельчения
- •4.1.2. Степень дробления и измельчения
- •4.1.3. Стадиональность и схемы дробления и измельчения
- •4.1.4. Удельная поверхность диспергированного материала
- •4.1.5. Современные представления о разрушении твердого материала
- •4.1.6. Механические свойства твердых тел при простых видах деформации
- •4.1.7. Законы дробления
- •4.1.8. Способы дробления, классификация машин для дробления и измельчения
- •4.2. Процесс грохочения
- •4.2.1. Основные понятия и назначение грохочения
- •4.2.2. Просеивающая поверхность
- •4.2.3. Способы определения гранулометрического состава
- •4.2.4. Ситовый анализ
- •4.2.5. Характеристики крупности
- •4.2.6. Аналитическое представление характеристик крупности
- •4.2.7. Дифференциальные функции распределения по крупности
- •4.2.8. Вычисление поверхности и числа частиц по уравнениям суммарной характеристики крупности
- •4.2.9. Эффективность процесса грохочения
- •4.2.10. «Легкие», «трудные» и «затрудняющие» частицы
- •4.2.11. Вероятность прохождения частиц через отверстия сита
- •4.2.12. Факторы, влияющие на процесс грохочения
- •4.3. Электромагнитная сепарация. Физические основы процесса
- •4.4. Электростатическая сепарация. Физические основы процесса
- •4.5. Электродинамическая сепарация
- •4.6. Сепарация твердых материалов по коэффициенту трения
- •4.7. Сепарация на основе явления смачиваемости
- •4.8. Аэросепарация
- •4.9. Составление балансной схемы переработанного твердого сырья
- •4.9.1. Баланс материалов при переработке твердых отходов
- •4.9.2. Технологические и технико-экономические показатели переработки твердых отходов
- •Контрольные вопросы
- •Варианты домашнего задания по курсу «Теоретические основы защиты окружающей среды»
- •1. Отстаивание, сгущение, осветление.
- •2. Флотация
- •3. Экстракция
- •4. Дробление и грохочение
- •5. Измельчение и классификация
- •6. Магнитное и электрическое разделение
- •Примеры выполнения домашних заданий
- •Темы заданий для курсовых работ по курсу «Теоретические основы защиты окружающей среды»
- •Пример выполнения курсовой работы
- •Литература
- •Оглавление
- •Глава 1. Химические методы очистки сточных вод 6
- •Глава 2. Явление осмоса и его использование при очистке сточных вод 20
- •Глава 3. Физические основы электродных процессов при очистке сточных вод от примеси 31
- •Глава 4. Физические основы процессов переработки твердых бытовых отходов 73
Пример выполнения курсовой работы
Материальный и энергетический балансы
Для правильного выбора способов очистки окружающей среды от отходов производства необходимо, прежде всего, провести анализ возможности возникновения отходов в реальном процессе и составить уравнение материального баланса.
Например, для изготовления эпитаксиальных кремниевых пластин широко используется водородное восстановление трихлорсилана по уравнению:
2SiHCl3(г)+2H2(г)2Si(тв)+6HCl.
Рассмотрим процесс получения трихлорсилана и составим схему материального баланса производства. Трихлорсилан - это бесцветная дымящаяся и легкозагорающаяся на воздухе жидкость плотностью 1,35 г/см3, кипящая при 31,8 °С и кристаллизирующаяся при –127 °С.
Для получения трихлорсилана производится обработка технического кремния хлористым водородом:
Si(тв)+3HCl(ж)=SiHCl3(г)+H2(г).
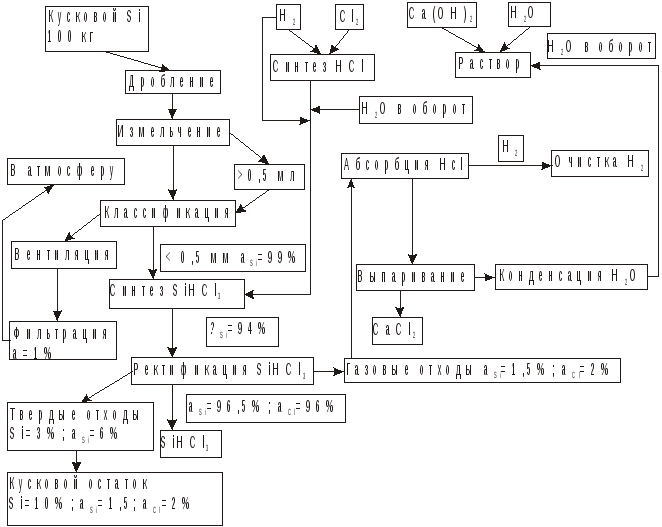
Рис. 1. Общая схема получения трихлорсилана
Реакция проводится обычно при температуре 300 400 °С с использованием измельченного кремния. Выход трихлорсилана возрастает при добавлении к хлористому водороду чистого водорода.
Очень важна хорошая очистка поступающей газовой смеси от кислорода и водяного пара, присутствие которых вызывает осаждение продуктов реакции гидролиза на кремний и снижение его реакционной способности.
Общая по этапам схема получения трихлорсилана с учетом потерь α на каждой операции приведена на рис. 1 продуктов реакции, например, получения 100 кг кремния в табл.1 расчет по уравнениям (1.1) и (1.2).
Таблица 1.
Материальный баланс процесса получения трихлорсилана (из 100 кг Si)
|
Наименование |
Количество, кг |
Si |
Cl | ||
|
% |
кг |
% |
кг | ||
|
1. Трихлорсилан |
428 |
21 |
89,81 |
78,3 |
335 |
|
2. Твердые отходы синтеза |
19,8 |
30 |
5,94 |
|
|
|
3. Кубовой остаток ректификации |
13,9 |
10 |
1,39 |
|
|
|
4. Газы при ректификации |
93,0 |
2 |
1,86 |
|
|
|
Итого: |
|
|
100 |
|
|
Материальный баланс
Для получения трихлорсилана производится обработка 100 кг технического кремния хлористым водородом:
Si(тв)+3HCl(ж)=SiHCl3(г)+H2(г).
Первоначально из 100 кг кускового кремния на фильтрацию тратится 1%, т.е.:
![]() .
.
На синтез SiHCl3 поступает (100 – 1) = 99 кг кремния. Из них, на твердые отходы синтеза теряется 6%, т.е.
![]() .
.
Оставшиеся (99 – 5,94) = 93,06 кг поступает на ректификацию, где 2% кремния расходуется на газовые отходы, т.е.
![]() ,
,
а 1,5% - на кусковой остаток, т.е.
![]() .
.
Следовательно, масса кремния в полученном трихлорсилане составляет (93,06 – 1,8612 – 1,3959) = 89,8 кг.
Таблица 2.
|
Наименование |
Количество, кг |
Si |
Cl | ||
|
% |
кг |
% |
кг | ||
|
1 |
2 |
3 |
4 |
5 |
6 |
|
1. Трихлорсилан |
428 |
21 |
89,8 |
78,3 |
335 |
|
1 |
2 |
3 |
4 |
5 |
6 |
|
2. Твердые отходы синтеза |
19,8 |
30 |
5,94 |
- |
- |
|
3. Кубовой остаток ректификации |
13,9 |
10 |
1,396 |
50,22 |
6,98 |
|
4. Газы при ректификации |
93,0 |
2 |
1,86 |
7,5 |
6,98 |
|
Итого: |
|
|
100 |
|
348,96 |
По таблице 1 масса хлора в трихлорсилане равна 335 кг, что составляет 96% от первоначальной массы хлора, т.е.
![]() .
.
Из них 2% составляет кусковой остаток, т.е.
![]() .
.
и 2% (6,98 кг) - газовый отходы при ректификации. Рассчитаем процентное содержание хлора (для табл.1) в кубовом остатке ректификации:
![]() ,
,
в газах при ректификации:
![]() кг.
кг.
Энергетический баланс
Таблица 3.
|
Элемент (вещество) |
H0298 кДж/моль |
S0298 Дж/мольК |
G0298 кДж/моль |
T, К интервал температур |
|
Si(тв) |
0 |
18,83 |
0 |
298-1685 |
|
HCl(ж) |
-92,31 |
186,79 |
-95,30 |
298-2000 |
|
SiHCl3(г) |
-657,52 |
330,95 |
-617,62 |
298-1000 |
|
H2(г) |
0 |
130,50 |
0 |
298-3000 |
m (кг) 100 428
Si(тв)+3HCl(ж)=SiHCl3(г)+H2(г)
М (г/моль) 28,1 36,51 135,61 2,02
Масса трихлорсилана:
m(SiHCl3) = m(Si)+m(H)+m(Cl3) => m(H) = 428 – 89,81 – 335 = 3,19 кг
Т.к. потерь водорода в реакции нет, то масса выделившегося водорода:
m(H2)=3,19∙2 = 6,38 кг.
Следовательно, m(HCl) = 3[m(H) + m(Cl)] = 3∙(3,19 + 335/3) = 344,5 кг.
Количество вещества:
ν(Si) = 100/28,1 = 3,559 моль,
ν(HCl) = 344,5/36,51 = 9,436 моль,
ν(SiHCl3) = 428/135,61 = 3,156 моль,
ν(H2) = 6,38/2,02 = 3,158 моль.
Энтальпия реакции:
![]()
![]()
= 3,156∙(–657,52) – 9,436∙(–92,31) = –2075,133 + 871,037 =
= –1204,096 кДж/моль
Энтропия реакции:
![]()
![]()
= [3,156∙330,95 + 3,158∙130,50] – [9,436∙186,79 + 3,559∙18,83] =
=1456,5972 – 1829,5663 = –372,9691 Дж/моль∙К.
Свободная энергия Гиббса:
![]()
![]()
= 3,156∙(–617,62) – 9,436∙(–95,30) = –1049,9579 кДж/моль.
Вывод:
Т.к. энтальпия данной реакции ΔH < 0, то, следовательно, реакция получения трихлорсилана является экзотермической, т.е. протекает с выделением тепла. Т.к. энтропия реакции ΔS < 0, то, следовательно, данный процесс обратим. Т.к. свободная энергия Гиббса так же ΔG < 0, то это свидетельствует о том, что данная реакция идет.
Тесты
Порядок выдачи вопросов теста: в случайном порядке.
Считать вес каждого вопроса равным единице.
В математической форме первое начало термодинамики записывается как:
Q = ΔU + A.
Q = ΔU.
Q = A.
Q = ΔU +Δ A.
Q = ΔU – A.
Какое выражение первого начала термодинамики является правильным, если работа совершается самой системой:
Q = ΔU + A.
Q = ΔU.
Q = A.
Q = ΔU +Δ A.
Q = ΔU – A.
Какое выражение первого начала термодинамики является правильным, если работа совершается за счет внешних сил над системой:
Q = ΔU + A.
Q = ΔU.
Q = A.
Q = ΔU +Δ A.
Q = ΔU – A.
В дифференциальной форме уравнение первого начала термодинамики записывается:
δQ = δU + δA.
δQ = dU + δA.
δQ = dU + dA.
dQ = dU +dA.
dQ = δU – dA.
Какое выражение из ниже перечисленных, с точки зрения энтропии, является критерием обратимости процесса в идеальной системе:
ΔS = 0.
ΔS > 0.
ΔS < 0.
ΔS ≥ 0.
ΔS ≤ 0.
Какое выражение из ниже перечисленных с точки зрения энтропии является критерием необратимости процесса в идеальной замкнутой системе:
ΔS = 0.
ΔS > 0.
ΔS < 0.
ΔS ≥ 0.
ΔS ≤ 0.
С учетом первого начала термодинамики дифференциальное уравнение энтропии имеет вид:
dS = 1/T (dU + pdV).
ΔS = 1/T (ΔU + pdV).
ΔS = 1/T (δU + pδV).
dS = 1/T (ΔU + ΔpΔV).
ΔS = 1/T (dU + ΔpΔV).
Энтропия системы при стремлении температуры к абсолютному нулю стремится к
0.
∞.
к конечной величине.
к отрицательной величине.
к положительной величине.
Укажите выражение, связывающие энтропию с вероятностью осуществления данного макроскопического состояния
S = k lnΩ (ε, N).
S = R ln Ω(ε, N).
S = k lnΩ(N).
S = k ln Ω(ε).
S = R lnΩ(N).
S = R lnΩ(ε).
В термодинамике неравновесных процессов баланса энтропии записывается:
– ρdS/dt = – div Is + σ.
ρdS/dt = div Is + σ.
ρdS/dt = – div Is + σ.
ρdS/dt = – div Is – σ.
– ρdS/dt = div Is + σ.
Информационная энтропия равна:
n
H = -∑Pk lnPk при ∑Pk=0.
k=1 к=1
∞
H = -∑Pk lnPk при ∑Pk=1.
k=1 к=1
∞
H = ∑Pk lnPk при ∑Pk=1.
k=1 к=1
n n
H = -∑Pk lnPk при ∑Pk=0.
k=1 к=1
∞∞
H = ∑Pk lnPk при ∑Pk=0.
k=1 к=1
В статистической физике энтропия системы, состоящей из N частиц, описывается уравнением:
S = Kб ln Ω.
S = T ln Ω.S = R ln Ω.
S = KбT ln Ω.
S = RT ln Ω, где Ω - плотность состояний или статистический вес.
Энтропия системы обладает свойством:
неаддитивности.
аддитивности.
скачкообразности.
плавно изменяется.
равна нулю.
Если система приходит в состояние разупорядочения, то полная энтропия системы равна:
ΔSраз = ΔSпоз – ΔSкол + ΔSэл.
ΔSраз = ΔSпоз + ΔSкол + ΔSэл.
ΔSраз = - ΔSпоз + ΔSкол + ΔSэл.
ΔSраз = ΔSпоз – ΔSкол – ΔSэл.
ΔSраз = ΔSпоз + ΔSкол – ΔSэл.
С точки зрения закона баланса энтропии процессы защиты окружающей среды являются:
энергетически выгодными.
энергетически не выгодными.
от энергии не зависят.
вопрос поставлен некорректно.
в зависимости от условий проведения процесса.
Какие основные уравнения лежат в основе расчетов процессов и аппаратов химической технологии:
закон сохранения массы.
закон сохранения энергии.
ни один из этих вопросов.
вопрос поставлен некорректно.
закон сохранения массы и закон сохранения энергии.
Какие системы называются двухфазными?
системы, состоящие только из твердых частиц и жидкости.
системы, состоящие только из твердых частиц и газа.
системы, состоящие только из твердых частиц.
системы, состоящие только из газа или жидкости.
системы, состоящие из твердых частиц и жидкости, а также системы, состоящие из твердых частиц и газа.
Поведение двухфазных систем определяется в основном:
концентрацией твердой фазы.
размером частиц.
концентрацией жидкой фазы.
концентрацией твердой фазы и размером частиц.
гранулометрическим составом частиц.
Двухфазная система приближается к однофазной, когда:
чем больше размер частиц и меньше их концентрация.
чем больше размер частиц и больше их концентрация.
чем меньше размер частиц и больше их концентрация.
чем меньше размер частиц и меньше их концентрация.
чем больше размер частиц и меньше их концентрация.
Как обезвоживают грубые суспензии с размером частиц более 10 мм?
грохочением.
гидроциклонированием.
при помощи вибрации.
центрифугированием.
дренажем под действием собственного веса.
Как обезвоживают суспензии с размером частиц от -10 до 2 мм?
грохочением.
гидроциклонированием.
при помощи вибрации.
сушкой.
дренажем с учетом силы тяжести.
Как обезвоживают суспензии с размером частиц от -2 до 0,5 мм?
дренажем под действием собственного веса.
дренажем под действием собственного веса и грохочением.
сушкой.
гидроциклонирование.
прокаливанием.
Как обезвоживают суспензии с размером частиц менее 0,5 мм?
дренажем под действием собственного веса.
дренажем под действием собственного веса и грохочением.
отстаиванием.
отстаиванием совместно с гидроциклонированием.
отстаиванием совместно гидроциклонированием и применением флокулянтов.
Как обезвоживают суспензии с размером частиц от -0,5 до 0,1 мм
дренажем под действием собственного веса.
дренажем под действием собственного веса и грохочением.
отстаиванием.
отстаиванием с применением флокулянтов.
отстаиванием с применением флокулянтов и гидроциклонированием.
Механические методы обезвоживания можно описать с помощью процессов:
оседания частиц в жидкости с переменной вязкостью.
фильтрации частиц через поры.
фильтрации частиц несжимаемый во времени осадок.
оседания частиц в жидкости с переменной вязкостью и фильтрации воды через поры.
фильтрации частиц через сжимаемый во времени осадок.
Можно ли достичь 100% обезвоживания с применением лишь только одного способа?
нет.
да.
в зависимости от условий.
вопрос некорректен.
это зависит от крупности материала.
Химически связанную воду называют:
кристаллизационной.
адсорбционной.
конституционной.
капиллярной.
гравитационной.
Координационно-химически связанную воду в кристалло-гидратах называют:
кристаллизационной.
адсорбционной.
конституционной.
капиллярной.
гравитационной.
Влагу на поверхности твердых тел называют:
кристаллизационной.
адсорбционной.
конституционной.
пленочной.
гравитационной.
Вода имеет конечную скорость вытекания из капилляра, эта скорость:
увеличивается по мере уменьшения гидростатического напора.
уменьшается по мере уменьшения гидростатического напора.
не зависит от гидростатического напора.
является функцией гидростатического напора.
вопрос поставлен некорректно.
Вода, остающаяся в осадке, называется:
кристаллизационной.
адсорбционной.
капиллярной
гравитационной.
обусловлена всеми механизмами образования.
Энергия связи конституционной воды равна:
тепловому эффекту реакции разложения гидрооксида металла до его окисла (100-200 ккал/моль).
тепловому эффекту удаления кристаллизационной воды ~ 10 ккал/моль.
дифференциальной теплоте адсорбции (2-3)L, где L – скрытая теплота конденсации.
энергии удаления капиллярно удерживаемой влаги.
вопрос поставлен некорректно.
Тепловой эффект реакции при удалении кристаллизационной воды равен:
энергии связи конституционной воды.
дифференциальной теплоте адсорбции.
энергии удаления капиллярно удерживаемой влаги.
~ 10ккал/моль.
тепловому эффекту разложения гидрооксида металла.
Дифференциальная теплота адсорбции паров зависит:
от степени заполнения поверхности.
от давления пара.
от температуры пара.
от состава пара.
от давления, температуры и состава пара.
Энергию удаления капиллярно-удерживаемой влаги можно оценить:
по тепловому эффекту удаления кристаллизационной воды.
по тепловому эффекту реакции разложения гидрооксида металла, до его окисла.
по дифференциальной теплоте адсорбции.
по величине работы перемещения объема жидкости с высоты, соответствующей капиллярному поднятию до уровня жидкости в широком сосуде.
по необходимому перепаду давлений (работа против сил вязкости).
Энергию удаления гравитационной влаги можно оценить:
по тепловому эффекту удаления кристаллизационной воды.
по тепловому эффекту реакции разложения гидрооксида металла до его окисла.
по дифференциальной теплоте адсорбции.
по величине работы перемещения объема жидкости с высоты соответствующему капиллярному поднятию до уровня жидкости в широком сосуде.
по необходимому перепаду давлений (работа против сил вязкости).
Для определения энергии связи воды с поверхностью твердого тела необходимо знать:
величины поверхностей твердых частиц.
размер пор.
диаметр капилляр в осадке.
только а и б или б и в.
а, б, в.
Макропористые материалы – материалы, размер пор которых:
менее 2*10-4 мм.
6*10-6 < δ < 2*10-4.
более 2*10-4.
менее 6*10-6 мм.
вопрос поставлен некорректно.
Материалы, относящиеся к переходному классу, имеют размер пор:
менее 2*10-4 мм.
6*10-6 < δ < 2*10-4.
более 2*10-4.
менее 6*10-6 мм.
вопрос поставлен некорректно.
Микропористые материалы - это материалы, размер пор которых:
менее 2*10-4 мм.
6*10-6 < δ < 2*10-4.
более 2*10-4.
менее 6*10-6 мм.
более 6*10-6.
Степень пористости материалов определяет величину:
внешней поверхности частицы.
величину пустого объема.
величину внутренней поверхности.
величину внутренней поверхности и пустого объема.
величину реального объема частицы.
Гигроскопичными называются тела, которые удерживают значительное количество влаги. Это происходит потому, что:
размеры пор приближаются к размерам адсорбируемых молекул воды.
адсорбция в микропорах приводит к заполнению их объема.
совместно а и б.
данные явления не зависят от указанных факторов.
данное явление обусловлено другими причинами.
Явление капиллярной конденсации отсутствует:
в больших порах δ > 2*10-4 мм.
в порах переходного размера 6*10-6 < δ < 2*10-4мм.
в малых порах δ < 6*10-6 мм.
в больших порах δ > 2*10-4 мм и малых порах δ < 6*10-6 мм.
в указанных ответах нет правильного.
Дренированием называют операцию обезвоживания:
за счет стекания жидкости по капиллярам осадка под влиянием собственного веса.
за счет стекания жидкости по капиллярам осадка под влиянием собственного веса и силы вибрации.
за счет стекания жидкости по капиллярам осадка под влиянием собственного веса и центробежной силы.
за счет стекания жидкости по капиллярам осадка под влиянием силы вибрации или центробежной силы.
за счет стекания жидкости по капиллярам осадка под влиянием силы Кориолиса.
При плотной упаковке шарообразных зерен эффективный радиус межзеренных каналов:
Rэфф = 0,51 rзер.
Rэфф = 0,41 rзер.
Rэфф = 0,47 rзер.
Rэфф = 0,31 rзер.
Rэфф = 0,21 rзер.
При дренировании чаще всего наблюдается:
турбулентный режим течения жидкости.
ламинарный режим течения жидкости.
переходный режим течения жидкости.
в начале дренирования переходной режим, а в конце - ламинарный.
в начале дренирования турбулентный режим течения жидкости, а в конце - переходный режим.
Зависит ли скорость течения жидкости от формы частиц и природы материала?
не зависит.
сильно зависит.
сильно зависит от формы частиц материала.
сильно зависит от природы материала.
сильно зависит от формы частиц материала и незначительно от природы материала.
Отстаивание - это процесс обезвоживания материала, происходящий при расслоении суспензии
под влиянием силы Кориолиса.
под влиянием силы вибрации.
под влиянием центробежной силы.
под влиянием собственного веса.
сила, под действием которой происходит расслоение суспензии, не указана.
Процесс отстаивания описывается законом Стоксом, если:
Cтв>0,1 - 1%, rтв = 100мкм - 1мм, μ - возрастающая величина, а V - скорость движения относительно твердого, соответствует значению скорости для турбулентного режима.
Cтв>0,1 - 1%, rтв = 10 > 1 мм, μ = Const, V не превышает значения для ламинарного потока.
Cтв>0,1 - 1%, rтв = 10 ÷ 100 мкм, μ - возрастающая величина, V не превышает значения для ламинарного потока.
Cтв>0,1 - 1%, rтв =10 ÷ 100 мкм, μ = Const, V не превышает значения для ламинарного течения.
среди ответов нет правильного.
При осаждении вязкость суспензии:
не изменяется.
изменяется незначительно.
изменятся, т.к. зависит от концентрации твердого тела.
изменятся, т.к. зависит от радиуса твердых частиц.
вопрос некорректен.
Правильный ответ:50.3
Жидкости, в которых величина вязкости постоянна и не зависит от скорости ее течения, называются:
неньютоновскими.
абсорбционными.
ньютоновскими.
гравитационными.
адсорбционными.
К какому классу относится концентрированная суспензия (массовое осаждение 15-25% твердого)
I.
II.
III.
IV.
суспензии не подразделяются на классы.
Суспензии какого класса подвергаются сгущению:
I и II.
I и III.
II и III.
III и IV.
II и IV.
В процессе сгущения пульпы образуется осветленная зона, которая находится:
выше границы осаждения.
ниже границы осаждения.
четкой границы осаждения не существует.
в процессе сгущения пульпы осветленный слой не образуется.
вопрос некорректен.
По кривой процесса сгущения можно определить:
степень содержания взвешенных частиц в растворе.
радиус осаждающихся частиц.
объем сосуда.
скорость осаждения твердых веществ.
состав осадка.
Удельная поверхность согласно методу Коу и Клевенжера рассчитывается как:
f = RнRж/ρжK1.
f = RнRж/ρжv0K1.
f = - RнRж/ρжv0K1.
f = RнRж v0/ρжK1.
f = RнRж v0/ρж.
Удельная поверхность согласно методу Кинча рассчитывается как:
f = 695*tp/C0H0.
f = 685*tp/C0H0.
f = 695*tp/H0.
f = tp/C0H0.
f = 65*tp/C0H0.
Какая величина определяется по формуле tc*(1/ρтв + (1/ρж)*Rcp)/f:
высота осветленной зоны.
высота переходной зоны.
высота уплотненной зоны.
высота зоны свободного падения.
из перечисленных ответов нет верного.
Скорость осаждающейся частицы под действием центробежной силы:
не достигает предельного значения.
достигает предельного значения.
остается постоянной.
в данном процессе скорость частицы определить невозможно.
вопрос некорректен.
В процессе осаждения под действием центробежной силы при Re < 0.2, когда имеет место ламинарный закон движения частиц, сила сопротивления определяется законом Ньютона:
F = 6 π μ r v.
F = 8 π μ r v.
F = 6 π μ r ρ.
F = 6 μ r v.
F = (6 π μ r v)/f.
При увеличение значения Re происходит:
увеличение роста эффективности действия центрифуг.
эффективность центрифуг не зависит от данного параметра.
уменьшение роста эффективности действия центрифуг.
увеличение значения расхода.
вопрос задан некорректно.
Фильтрование - это процесс:
обезвоживания растворов.
отделения растворимых твердых частиц с пористых перегородок.
отделения нерастворимых твердых частиц с пористых перегородок.
осаждения твердых частиц на пористые перегородки.
осаждение суспензий, содержащих большое количество мелких частиц.
По характеру процесса фильтрование бывает с образованием осадка и без него, целью этих процессов является получение товарного продукта в виде:
осадка и фильтрата соответственно.
фильтрата и осадка соответственно.
таких видов фильтрования не существует.
концентрата в обоих случаях.
вопрос некорректен.
К числу практически несжимаемых можно отнести:
гидроокиси металлов.
осадки, состоящие из легкодеформируемых материалов.
осадки, состоящие из относительно мелких кристаллических частиц менее 45 мкм.
осадки, состоящие из относительно крупных кристаллических частиц более 45 ÷ 100 мкм.
осадки, состоящие из относительно крупных кристаллических частиц более 70 ÷ 100 мкм.
Чему препятствуют вспомогательные вещества, используемые при фильтровании:
увеличению скорости фильтрования.
проникновению твердых веществ в поры фильтровальной перегородки.
увеличению эффективности фильтрования.
упрощению извлечения шлама.
вспомогательные вещества при фильтровании не используются.
В общем виде скорость течения жидкости через пористый слой определяется:
размерами пор.
перепадом давления.
а и б.
производительностью.
б и г.
Коэффициент сопротивления определяется формулой:
λ = 133/Re - 2.34.
λ = 133*Re + 2.34.
λ = Re/133 + 2.34.
λ = 133/Re + 0.34.
λ = 133/Re + 2.34.
Ламинарный режим практически существует при Re:
>50.
< 50.
= 50.
режим течения жидкости не зависит от данного параметра.
среди ответ нет правильного.
Пористость находят по формуле:
ε = (V-V0)/V.
ε = (V-V0)*V.
ε = (V-V0)/V0.
ε = (V-V0)*V0.
вопрос некорректен.
Переменная скорость фильтрования в дифференциальной форме выражается:
W = dV*Sdτ.
W = dVS/dτ.
W = dV + Sdτ.
W = dV/dτ.
W = dV/Sdτ.
Удельное и полное сопротивления связаны между собой уравнением:
Rос = r0H = - r0x0(V/S).
Rос = r0H = r0x0(V/S).
Rос = r0H + r0x0(V/S).
Rос = r0H = r0x0(V*S).
Rос = r0H = r0(V/S).
Как гидравлическое сопротивление осадка Roc может меняться по ходу процесса из-за:
гидравлическое сопротивление остается на протяжении всего процесса постоянным.
возрастает из-за засорения пор мелкими частицами.
возрастает из-за некоторой сжимаемости осадка.
уменьшается из-за применения вспомогательных веществ.
б и в.
В каких случаях можно проинтегрировать дифференциальное уравнение фильтрации при допущении постоянства удельного сопротивления осадка?
при ΔР = Const.
при dV/dτ = const.
при ΔР и dV/dτ = const.
в случаях а, б и в.
в случаях а и в.
Если жидкость фильтруется сквозь осадок постоянной толщины, то:
ΔР=0, W=const.
ΔР=const, W=const.
ΔР=0, W=0.
ΔР=1, W=0.
ΔР=0, W=∞.
Полный цикл работы фильтра периодического действия состоит из операций:
загрузки суспензии, фильтрования, промывки осадка, продувки его и удаления.
подготовки фильтра, загрузки суспензии, фильтрования, промывки осадка и его продувки.
подготовки фильтра, загрузки суспензии, фильтрования, промывки осадка, продувки его и удаления.
подготовки фильтра, загрузки вспомогательных веществ, фильтрования, промывки осадка, продувки его и удаления его.
подготовки фильтра, промывки суспензии, загрузки суспензии, фильтрования, продувки его и удаления.
После прохождения условной скорости фильтрации максимума, условная скорость:
резко уменьшается.
уменьшается медленно.
увеличивается постепенно.
увеличивается резко.
не изменятся.
Какими свойствами должна обладать фильтровальная перегородка?
способностью хорошо задерживать твердые частицы суспензии и небольшим гидравлическим сопротивлением.
возможностью легкого отделения осадка и достаточной механической стойкостью.
стойкостью к воздействию среды, реагентов, температуры, а также высокой пористостью.
а, б, и стойкостью к воздействию среды, реагентов, температуры.
среди ответов нет правильного.
От размера частиц суспензии, свойств осадка, его удельного сопротивлении, свойств осадка сниматься, производительности зависит:
выбор фильтра.
выбор циклона.
выбор вспомогательных веществ.
размер фильтровальной перегородки.
среди ответов нет правильного.
Удельная производительность вычисляется по формуле:
qw = (St)/Q.
qw = - Q/(St).
qw = Q/(St).
qw = -St/Q.
qw = (Qt)/S.
По формуле Sфq рассчитывается:
производительность фильтра.
скорость фильтра.
скорость частиц суспензии.
высота осадка.
пористость.
Скорость фильтрации меняется от времени в зависимости от:
давления и температуры воздуха.
вида суспензии.
от вида взвешенных частиц.
степени изношенности и забивки фильтровальной перегородки.
от количества взвешенных частиц.
При процессе центробежного фильтрования среднеарифметическое значение площади осадка вычисляется по формуле:
Sср.лог. = (r2 – r1)h.
Sср.лог. = (r2 – r1)πH.
Sср.лог. = (r2 + r1)πh.
Sср.лог. = (r2 – r1)πh.
Sср.лог. = (r2 – r1)/πh.
Осаждение суспензий, содержащих большое количество мелких частиц, ускоряет процесс:
фильтрации.
осаждения.
агрегирования.
абсорбции.
адсорбции.
Закон Эйнштейна-Смолуховского определяется формулой:
ΔХ =
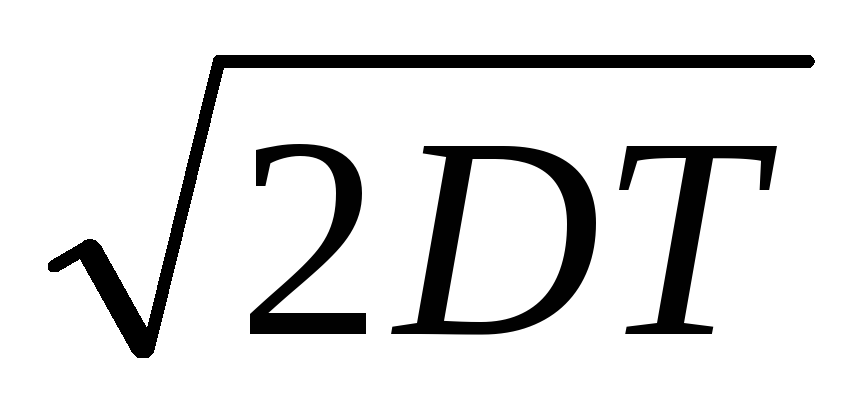 .
.ΔХ =
 .
.ΔХ = 2DT.
ΔХ = – 2DT.
ΔХ =
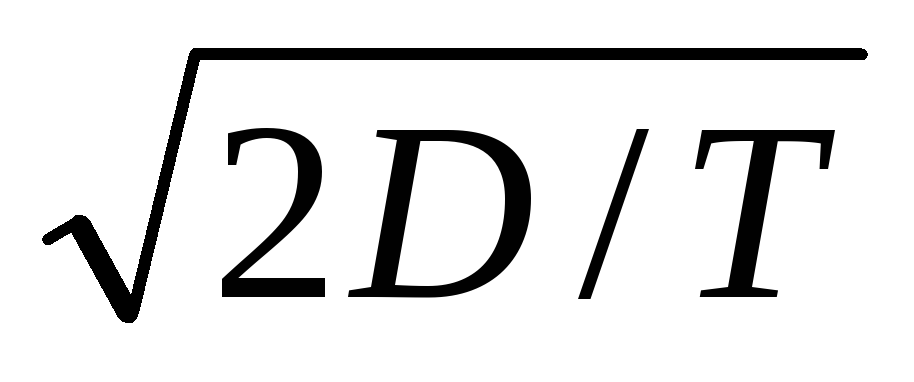 .
.
Мелкие частицы могут сталкиваться друг с другом за счет:
сил трения.
броуновского движения.
диффузионного механизма.
гравитационных сил.
сил взаимного притяжения.
Энергия взаимодействия под действием сил Ван-дер-Ваальса определяется некой формулой, в которой один из членов определяется как (P12d2 + P22d1) и называется:
ориентационное слагаемое.
индукционное слагаемое.
дисперсионное слагаемое.
дипольный момент молекулы.
поляризуемость.
Характерной особенностью сил Ван-дер-Ваальса является то, что они:
самые прочные.
самые слабые.
не насыщаются.
насыщаются.
среди ответов нет правильного.
Закон изменения сил Ван-дер-Ваальса для двух шаров одинаковой формы имеет вид:
U = - AR/12H2.
U = AR/12H2.
U = - AR*12H2.
U = - AR/10H2.
U = - AR/12H.
Энергия взаимодействия частиц конечного размера примерно вдвое меньше энергии взаимодействия двух бесконечных полупространств, если:
δ = 0.
δ = H.
δ = ∞.
H = 0.
среди ответов нет правильного.
На границе раздела твердое тело - жидкость возникает:
двойной электрический слой.
гидростатические силы.
разность потенциалов.
поверхностное натяжение.
силы взаимного притяжения.
Главной особенностью электростатических сил является то, что:
радиус их действия является функцией концентрации электролита.
они самые прочные.
они самые слабые.
они возникают за счет двойного электрического слоя.
вопрос некорректен.
Сила коагулирующего действия электролитов в большей мере определяется:
размером частиц.
видом вспомогательных веществ.
валентностью ионов.
пористостью.
среди ответов нет правильного.
Коагуляционный механизм наблюдается при:
добавлении вспомогательных веществ.
сгущении суспензии.
добавлении электролита.
применении высокомолекулярных полимерных веществ.
искусственной гидрофобизации.
Флокуляция наблюдается при:
добавлении вспомогательных веществ.
сгущении суспензии.
добавлении электролита.
применении высокомолекулярных полимерных веществ.
искусственной гидрофобизации.
Мостиковый механизм наблюдается при:
добавлении вспомогательных веществ.
сгущении суспензии.
добавлении электролита.
применении высокомолекулярных полимерных веществ.
искусственной гидрофобизации.
Знаком и величиной заряда поверхности минеральных частиц определяется:
величина адсорбции молекул.
величина абсорбции молекул.
величина сил Ван-дер-Ваальса.
производительность.
вопрос некорректен.
Селективная флокуляция наблюдается:
в условиях селективной адсорбции.
в условиях селективной абсорбции.
при нормальных условиях.
при добавлении вспомогательных веществ.
среди ответов нет правильного.
Под процессом поглощения одного или нескольких компонентов из газовой смеси или раствора твердым веществом, понимают процесс:
абсорбции.
фильтрации.
коагуляции.
адсорбции.
осаждения.
При небольших концентрациях поглощаемого вещества в исходной смеси применяется процесс:
сгущения.
фильтрации.
коагуляции.
адсорбции.
осаждения.
Пористые твердые вещества применяют в качестве:
вспомогательных веществ.
адсорбентов.
абсорбентов.
флокулянтов.
электролитов.
Для сушки газа применяются:
иониты.
цеолиты.
силикагели.
активные угли.
фильтровальные перегородки.
Процесс извлечения адсорбированного вещества из твердого поглотителя называется процессом:
сгущения.
фильтрации.
коагуляции.
адсорбции.
десорбции.
Основными методами десорбции являются:
вытеснение.
испарение.
а и б.
сгущение.
испарение.
Метод разделения материалов, основанный на различии физико-химических свойств поверхности материалов, называется процесс:
флотации.
фильтрации.
коагуляции.
адсорбции.
осаждения.
Флотируемость различных материалов зависит от:
способности поверхности материалов смачиваться водой.
размера частиц.
вида вспомогательных веществ.
валентности ионов.
пористости.
На молекулу внутри жидкости действуют силы:
взаимного притяжения.
Ван-дер-Ваальса.
гидростатические.
взаимного отталкивания.
вопрос некорректен.
Уравнение адсорбции Гиббса имеет вид:
Г = - (dσ/dC)/(C/RT).
Г = (dσ/dC)*(C/RT).
Г = - (dσ/dC)/(CRT).
Г = (dσdC)/(C/RT).
Г = - (σ/C)*(C/RT).
Уравнение адсорбции Ленгмюра имеет вид:
Г = Г∞ = bC/(1+bC).
Г = Г0 = bC/(1+bC).
Г = Г∞ = bC*(1+bC).
Г = Г∞ = bC/(1-bC).
Г =1/ Г∞ = bC/(1+bC).
Уравнение адсорбции Фрейндлиха в логарифмической форме имеет вид:
lgГ = lgq + (1/n)lgC.
lgГ = lgk + (1/n)lgC.
lgГ = lgk - (1/n)lgC.
lgГ = lgq - (1/n)lgC.
lgГ = - lgk - (1/n)lgC.
Отставание периметра смачивания от изменения краевого угла называется:
гистерезисом смачивания.
флотацией.
флокуляцией.
коагуляцией.
среди ответов нет правильного.
Реагенты-регуляторы применяются для:
изменения флотируемости материалов.
увеличении скорости процесса флотации.
изменения щелочности.
устранения гистерезиса смачиваемости.
повышения устойчивости воздушных пузырьков.
Регуляторы среды применятся для:
изменения флотируемости материалов.
увеличения скорости процесса флотации.
изменения щелочности.
устранения гистерезиса смачиваемости.
повышения устойчивости воздушных пузырьков.
Регуляторы-пенообразователи применяются для:
изменения флотируемости материалов.
увеличения скорости процесса флотации.
изменения щелочности.
устранения гистерезиса смачиваемости.
повышения устойчивости воздушных пузырьков.
Процессом извлечения одного или нескольких компонентов из растворов или твердых тел с помощью избирательных растворителей называется процесс:
экстракции.
фильтрации.
коагуляции.
адсорбции.
осаждения.
Коэффициент распределения определяется выражением:
m = y* - x.
m = y*+ x.
m = y*/x.
m = -y*/x.
m = y**x.
Процессы массо- и теплообмена одновременно протекают при:
сушке.
экстракции.
фильтрации.
коагуляции.
адсорбции.
Практически нейтральными считаются воды, имеющие:
pH < 6.5.
pH = 6.5 ÷ 7.
pH = 7 ÷ 10.
pH = 6.5 ÷ 8.5.
pH = 6.5 ÷ 10.
Если на предприятии имеются кислые и щелочные воды, не загрязненные другими компонентами, то применяется метод:
нейтрализации смешиванием.
нейтрализации добавления реагентов.
нейтрализации кислыми газами.
окисления и восстановления.
среди ответов нет правильного.
Для нейтрализации каких сточных вод используют гидроксид кальция (известковое молоко):
щелочных.
кислых.
нейтральных.
радиоактивных.
вопрос некорректен.
Количество кислого газа, необходимого для нейтрализации, определяется по формуле:
M = χ·β·F·Δc.
M = χ·β·F·c.
M = χ·β·F/Δc.
M = - χ·β·F·Δc.
M = χ·F·Δc.
При введении Cl2 в воду образуется:
хлорноватистая кислота.
соляная кислота.
оксид хлора.
а и б одновременно.
реакция не пойдет.
Как называется сумма Cl2 + HOCl + OCl-
известковое молоко.
доломит.
свободный активный хлор.
магнезит.
сжиженный хлор.
Потребность реагентов Xi (кг/сутки) для окисления рассчитывается по формуле:
Xi = XClQ/a.
Xi = XNaQn/a.
Xi = XClQn/a.
Xi = XClQna.
Xi = - XClQn/a.
При очистке воды от железа используют:
известковое молоко.
доломит.
свободный активный хлор.
кислород.
пероксид водорода.
Если раствор отделен от чистого растворителя полупроницаемой перегородкой, то растворитель просачивается через нее в раствор. Такое явление называется:
нейтрализация.
осмос.
фильтрация.
электролиз.
электрофорез.
Согласно закону Гей-Люссака осмотическое давление:
при данной концентрации пропорционально абсолютной температуре.
при данной температуре пропорционально концентрации.
при данном объеме пропорционально температуре.
при данной температуре пропорционально объему.
закон Гей-Люссака не применим к осмотическому давлению.
Общее уравнение состояния для осмотического давления выглядит следующим образом:
P = - RTc.
P = R + Tc.
P = RTc.
P = RT/c.
P = R/Tc.
Согласно закону Вант-Гоффа: растворенное вещество содержит в разбавленном растворе столько же молекул, сколько оно имело бы их в состоянии …. При той же температуре, в том же объеме и при газовом давлении, равном осмотическому давлению раствора. Вставьте пропущенное слово:
воды.
газа.
пара.
невесомости.
здесь нет пропущенных слов.
Химические процессы на электродах, сопровождающие пропускание тока через раствор электролита, называются:
нейтрализация.
осмос.
фильтрация.
электролиз.
электрофорез.
Электрод, соединенный с отрицательным электродом источника тока называется:
катодом.
анодом.
катионом.
анионом.
вопрос некорректен.
Электрод, соединенный с положительным электродом источника тока называется:
катодом.
анодом.
катионом.
анионом.
вопрос некорректен.
При электролизе на катоде идут процессы …, а на аноде - процессы ….
восстановления и окисления соответственно.
окисления и восстановления соответственно.
обезвоживания и сушки соответственно.
нейтрализации и окисления соответственно.
среди ответов нет правильного.
Закон Ома для явления электролиза выглядит следующим образом:
E + Ep = iw.
E – Ep = i/w.
E = iw - Ep.
E – Ep = i.
E – Ep = iw.
Кривая силы тока в функции от электродвижущей силы называется кривой:
тока.
электродвижущей силы.
напряжения.
разности потенциалов.
электрокапиллярной.
Изменения, происходящие в гальванической цепи при прохождении через нее тока, называется:
поляризация.
электродвижущая сила поляризации.
электродвижущая сила разложения.
концентрационная поляризация.
среди ответов нет правильного.
Электролиз сопровождается изменением концентрации электролита около электродов, что ведет к появлению обратной электродвижущей силы. Это явление называется:
поляризацией.
электродвижущей силой поляризации.
электродвижущей силой разложения.
концентрационной поляризацией.
среди ответов нет правильного.
Уменьшение обратной электродвижущей силы поляризации путем более или менее полного устранения ее причин называется:
перенапряжением.
деполяризацией.
электроосмосом.
электродвижущей силой разложения.
электрофорезом.
Если потенциал выделения отличается от термодинамического обратимого электродного потенциала, то имеет место:
перенапряжение.
деполяризация.
электроосмос.
возникновение электродвижущей силы разложения.
электрофорез.
Какого вида мениск образует ртуть на границе с водой вследствие поверхностного натяжения?
вогнутый.
прямой.
выпуклый.
мениск не образуется.
вопрос некорректен.
Зависимость поверхностного натяжения от приложенного поляризующего потенциала изображается …. кривой:
тока.
электродвижущей силы.
напряжения.
разности потенциалов.
электрокапиллярной.
Электрокапиллярная кривая выражается уравнением:
δσ/δЕ = -ε.
δσ*δЕ = -ε.
δσ/δЕ = ε.
δσ/Е = -ε.
σ/δЕ = -ε.
При движении раствора электролита относительно граничащей с ним твердой поверхности и, наоборот, при движении этой поверхности относительно раствора возникает:
электрокинетические явления.
деполяризация.
электроосмос.
электродвижущая сила разложения.
электрофорез.
Из каких частей состоит диффузный двойной слой?
плоской поверхности.
диффузной поверхности.
а и б.
электрических поверхностей.
в и г.
Сумма скачков потенциалов в обеих частях диффузного двойного слоя определяется формулой:
E = ψ – ξ.
E = ψ + β.
E = ψ + ξ.
E = χ + ξ.
E = ψ / ξ.
Движение жидкости в электрическом поле относительно твердой поверхности называется:
перенапряжением.
деполяризацией.
электроосмосом.
электродвижущей силой разложения.
электрофорезом.
Скорость движения жидкости определяется по формуле:
u = (q ξDE)/ 4πηl.
u = q ξDE4πηl.
u = (q ξDE)/ πηl.
u = (q ξDE)/ 4ηl.
u = (q DE)/ 4πηl.
Потенциал течения определяется по формуле:
E = ξDP/4πηχ.
E = ξDP4πηχ.
E = ξDP/4πη.
E = ξDP + 4πηχ.
E = ξDP/πηχ.
Как называется явление, обратное электроосмосу:
перенапряжением.
деполяризацией.
электроосмосом.
электродвижущей силой разложения.
электрофорезом.
Скорость электрофореза подсчитывается по формуле:
u = ( ξDE)/ 4πηl.
u = q ξDE4πηl.
u = (q ξDE)/ πηl.
u = (q ξDE)/ 4ηl.
u = (q DE)/ 4πηl.
Процесс очистки сточных вод, при котором используют нерастворимые электроды, называется
электрокоагуляция.
электродиализ.
электрофлотация.
дробление.
вопрос некорректен.
Процесс очистки сточных вод, происходящий при помощи пузырьков газа, образующихся при электролизе воды, называется:
электрокоагуляция.
электродиализ.
электрофлотация.
дробление.
вопрос некорректен.
Процесс очистки сточных вод, основанный на разделении ионизированных веществ под воздействием электродвижущей силы, называется:
электрокоагуляция.
электродиализ.
электрофлотация.
дробление.
вопрос некорректен.
Количественная характеристика процесса, показывающая, во сколько раз уменьшился размер кусков или частиц материала при дроблении, называется:
грохочением.
стадиональностью.
избирательным дроблением.
степенью дробления.
дренированием.
Степень дробления определяется по формуле:
i = Dmax/dmax.
i = Dmax*dmax.
i = Dmax + dmax.
i = Dmax - dmax.
i = Dmin/dmin.
Конструктивная степень дробления определяется по формуле:
i = B*b.
i = B + b.
i = B – b.
i = B/b.
i = b/B.
Степень дробления, достигаемая в каждой отдельной стадии, называется:
первичной.
суммарной.
частной.
циклической.
общей.
Последовательность операций при дроблении называется:
стадией дробления.
правилом дробления.
принципом дробления.
схемой дробления.
способом дробления.
Площадь поверхности диспергированного материала, состоящего из отдельных кусков, зависит от их:
количества.
веса.
крупности.
формы.
массы.
Дефекты кристаллической структуры подразделяют на:
средние.
частичные.
точные.
точечные.
линейные.
Удельный расход энергии определяется как:
Еуд = - Е/Q.
Еуд = Е*Q.
Еуд = Q/E.
Еуд = - Q/Е.
Еуд = Е/Q.
Рассев сыпучего материала с целью определения его гранулометрического состава называется:
гранулированным анализом.
общим анализом.
ситовым анализом.
дисперсным анализом.
фотолитографией.
Графическое изображение гранулометрического состава сыпучего материала является характеристикой:
сыпучести.
скорости осаждения.
дробления.
крупности.
пористости.
Уравнение Годэна-Андреева имеет вид:
F(x) = (x/xmax)k.
F(x) = (x/xmax)x.
F(x) = (x*xmax)k.
F(x) = (x/xmin)k.
F(x) = (x/xmax)x.
Какое уравнение наиболее применимо для описания полимодальных распределений:
Розина-Раммлера.
Годэна-Андреева.
Харриса.
Лапласа.
среди ответов нет правильного.
Для количественной оценки полноты отделения мелкого материала от крупного при грохочении введено понятие:
грохочение.
эффективность грохочения.
избирательное дробление.
степень дробления.
дренирование.
Характеристика, выраженная в процентах или в долях единицы, отношение массы подрешетного продукта к массе нижнего класса в исходном материале называется:
грохочением.
эффективностью грохочения.
избирательным дроблением.
степенью дробления.
дренированием.
Эффективность грохочения определяется формулой:
E = (C*Qa)*104.
E = (C + Qa)*104.
E = (C/Qa)*104.
E = (C - Qa)*104.
E = (C/Qa)/104.
Зерна, диаметр которых меньше трех четвертей отверстия сита, называются:
трудными.
затрудняющими.
легкими.
тяжелыми.
крупными.
Зерна, диаметр которых более трех четвертей отверстия сита, называются:
трудными.
затрудняющими.
легкими.
тяжелыми.
крупными.
Зерна, диаметр которых более полуторного размера отверстия частиц, называются:
трудными.
затрудняющими.
легкими.
тяжелыми.
крупными.
Вероятность прохождения зерна через отверстие сита определяется по формуле:
P = (1 – d*l)2.
P = (1 + d/l)2.
P = (1 – d/l)3.
P = 1 – (d/l)2.
P = (1 – d/l)2.
Угол над горизонтом определяется по формуле:
cosθp = (1 - (1 + 8k2)1/2)/4k.
cosθp = (1 + (1 + 8k2)1/2)/4k.
cosθp = (1 + (1 + 8k2)2)/4k.
cosθp = (1 + (1 - 8k2)1/2)/4k.
cosθp = (1 + (1 + 8k2)1/2)/k.
Возможно ли грохочение каменных углей при их влажности более 6%?
да.
нет.
практически невозможно.
вопрос поставлен некорректно.
процесс грохочения не зависит от влажности материала.
Как зависит производительность грохота от ширины сита?
практически прямо пропорциональна.
обратно пропорциональна.
равна.
не зависит.
вопрос некорректен.
Сколько областей можно выделить на поверхности сита, различающиеся скоростью прохождения частиц?
2.
3.
4.
5.
1.
Диаметр свободно проходящего через отверстия зерна, определяется по формуле:
d = lcosα – hsinα.
d = lcosα + hsinα.
d = lcosα – hcosα.
d = lsinα + hsinα.
d = lsinα – hcosα.
Сила, с которой магнит действует на другой магнит или на любое другое магнитное вещество, называется:
силой притяжения.
магнитной.
гравитационной.
трения.
вопрос некорректен.
Напряженность магнитного поля определяется по формуле:
H = m*r2.
H = m + r2.
H = m/r2.
H = m - r2.
H = r2/m.
Магнитная проницаемость тела определяется по формуле:
μ = B/H.
μ = B*H.
μ = B+H.
μ = B – H.
μ = H/B.
Магнитная восприимчивость тела определяется формулой:
χ = (μ + 1)/4π.
χ = (μ – 1)*4π.
χ = (μ – 1)/4π.
χ = (1 - μ)/4π.
χ = (μ – 1)/π.
Магнитное сопротивление определяется по формуле:
R = l*μcS.
R = l/μcS.
R = l+μcS.
R = l - μcS.
R = μcS.
Магнитный силовой поток определяется выражением:
Ф = F*R.
Ф = F+R.
Ф = F – R.
Ф = F/R.
Ф = R/F.
Минералы, отталкивающиеся при любом знаке заряда, называются:
реверсивно положительными.
нереверсивными.
реверсивно отрицательными.
немагнитными.
сильномагнитными.
Комбинированный процесс магнитного обогащения, основанный на использовании различий в магнитной восприимчивости, называется:
электрокоагуляцией.
электродиализом.
электрофлотацией.
дроблением.
электродинамической сепарацией.
Содержание цветных металлов в ТБО составляет около:
100%.
50%.
0,7%.
70%.
0%.
Процесс разделения материалов, основанный на различии в величине коэффициентов трения, называется:
обогащением по трению.
электродиализом.
электрофлотацией.
дроблением.
электродинамической сепарацией.
Сила трения при обогащении по трению определяется по формуле:
F = fPsinα.
F = f/Pcosα.
F = fAcosα.
F = fPcosα.
F = fqcosα.
Процесс обогащения в движущейся газовой среде, основанный на использовании различий в плотности компонентов и их скорости витания, называется:
обогащением по трению.
электродиализом.
электрофлотацией.
дроблением.
аэросепарацией.
