
- •Лекции «Молекулярная Фотоника»
- •1. Энергетический фактор
- •2. Кинетический фактор
- •3. Особенности распределения электронной плотности в эв состоянии.
- •Основное и возбужденное (синглетное) состояния
- •Формальдегид
- •Дипольный момент
- •4. Форма (вид) потенциальной кривой в эв состоянии
- •5. Синглетные и триплетные состояния.
Лекции «Молекулярная Фотоника»
Лекция 5. Особенности фотохимических реакций
Законы фотохимии.
Любая ф/х реакция начинается с поглощения света. 1-ый закона фотохимии - закона Гроткуса-Дрепера:
«Фотохимические превращения происходят только под действием того света, который поглощается веществом»
2-ой закон фотохимии - закона Штарка-Эйнштейна
«Каждый поглощенный квант света вызывает превращение только одной молекулы»
Существуют 4 фактора, определяющие особенность ф/х реакций:
Энергетический фактор.
Кинетический фактор.
Особенности распределения электронной плотности в ЭВ состоянии и в основном состоянии
Форма (вид) потенциальной кривой в ЭВ состоянии.
1. Энергетический фактор
А В (1) термическая
А* В (2) фотохимическая


 EА*
EА*

G < 0
В
 h
h
G > 0
А
2. Кинетический фактор
= k [A],
где
k = k0 exp(- E/RT)
 А
В
А
В
 E
E

E



координата реакции
Связь между E и G,
E G (при G > 0)
E 0 для G < 0.
3-х случая
I IIIII
 А В А
В А В
А В А
В А В
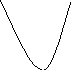
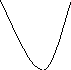
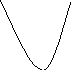


 E1
E1
 G > 0
E2
E3
G > 0
E2
E3

 G
< 0
G
< 0

E1
> E2
> E3

 координата
реакции
координата
реакции
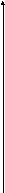

Е
 А*
А*

В

h

 А
А

координата реакции
Т .о.А
В энергетически
не выгодна и кинетически
.о.А
В энергетически
не выгодна и кинетически
медленная реакция
А* В энергетически выгодна и кинетически
быстрая реакция
Для бимолекулярных ф/х реакций … время жизни ЭВ состояния и концентрацию реагента.
h
A А* + В C + D, kr
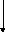
k0 (1/)
A
Выражение для квантового выхода D имеет вид
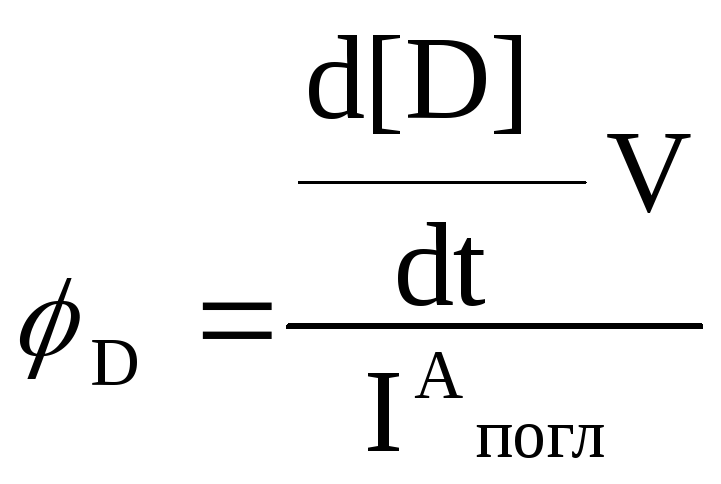
![]()
![]()
Метод стационарных концентраций
![]()
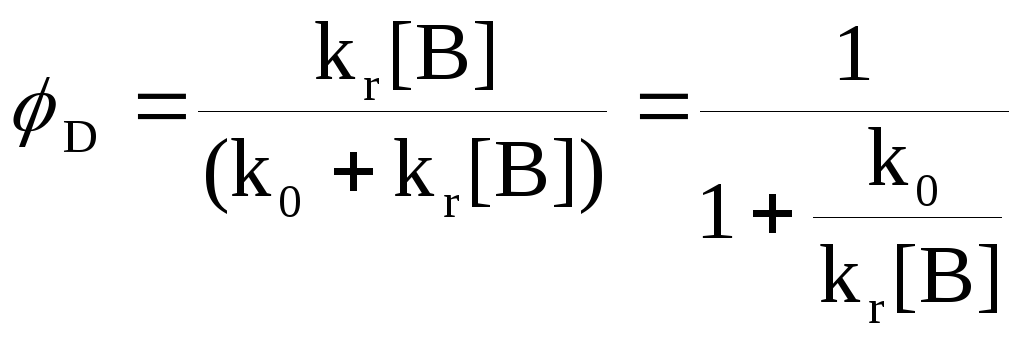
D определяется отношением k0/kr [B]
3. Особенности распределения электронной плотности в эв состоянии.
Распределение электронной плотности в ЭВ состоянии отличается от распределения электронной плотности в основном состоянии, что, проявляется в изменении реакционной способности молекулы (потенциал ионизации, сродство к электрону, кислотно-основные свойства) и в изменении ее геометрии (длины связей, углы) и др. (дипольный момент).
Формальдегид. Два типа электронных переходов: n * и *
Формальдегид ( > C=O)
