
- •Киров 2010
- •1.1. Теоретические предпосылки
- •l.2. Ход выполнения работы
- •1.3. Обработка экспериментальных данных
- •1.4. Правила техники безопасности
- •2.1. Теоретические предпосылки
- •2.2. Ход выполнения работы
- •2.3. Правила техники безопасности
- •3.1. Теоретические предпосылки
- •3.1.1. Коррозия с водородной деполяризацией
- •3.1.2. Коррозия с кислородной деполяризацией
- •3.2. Ход выполнения работы
- •3.3. Правила техники безопасности
- •4.1. Теоретические предпосылки
- •4.2. Ход выполнения работы
- •4.3. Обработка результатов экспериментов
- •4.4 Правила техники безопасности
- •5.1. Коррозия бетона и железобетона в жидких средах
- •5.2. Коррозия бетона и железобетона в условиях агрессивной атмосферы
- •5.3. Подземная коррозия бетона и железобетона
- •5.4. Ход выполнения работы
- •6. ЗАЩИТА СТРОИТЕЛЬНЫХ КОНСТРУКЦИЙ ОТ КОРРОЗИИ
- •6.1. ЗАЩИТНЫЕ ПОКРЫТИЯ
- •6.1.1 Защитные покрытия по металлу
- •6.1.1.2. Битумные покрытия по металлу
- •Составы битумных мастик
- •6.1.1.3. Полимерные покрытия по металлу
- •6.1 1.4. Металлические покрытия.
- •6.1.1.5. Композиционные покрытия по металлу
- •6.1.2. Защитные покрытия по бетону и железобетону
- •6.1.2.2. Битумные покрытия
- •6.1.2.3. Защитные покрытия с использованием рулонно-оклеечной изоляции
- •6.1.2.4. Неорганические покрытия по бетону
- •6.1.2.5. Композиционные покрытия
- •6.1.2.6. Гидрофобизаторы
- •6.2. Изменение природы корродирующего материала
- •6.2.1.Легирование стали
- •6.2.2. Повышение химической стойкости бетона и железобетона
- •Виды ингибиторов коррозии арматуры и их попутное действие
- •6.3. Обработка коррозионной среды
- •6.4. Изменение условий коррозии
- •ПРИЛОЖЕНИЕ
- •ЗАДАЧИ ДЛЯ ИНЖЕНЕРНО-СТРОИТЕЛЬНОГО ФАКУЛЬТЕТА
- •БИБЛИОГРАФИЧЕСКИЙ СПИСОК
9
l.2. Ход выполнения работы
В настоящей лабораторной работе изучение газовой коррозии производится при высокой температуре в муфельной печи, температура в которой контролиру-
ется с помощью хромель-алюмелевой термопары, соединенной с цифровым вольтметром. В ходе экспериментов изучается влияние на газовую коррозию тем-
пературы, продолжительности коррозии и природы металла в зависимости от конкретного задания.
В качестве задания к лабораторной работе преподавателем может быть пред-
ложен один из следующих вариантов исследований:
а) при постоянной температуре и продолжительности опыта изучить влияние природы металла на скорость газовой коррозии;
б) исследовать влияние температуры окружающей среды на скорость корро-
зии конкретного металла;
в) исследовать скорость газовой коррозии во времени.
Порядок исследования.
1.Включить печь и нагреть ее до необходимой температуры.
2.Подготовить образцы к испытаниям:
определить площадь исследуемых образцов;
удалить с их поверхности продукты коррозии зачисткой наждачной бума-
гой;
промыть образцы водой, обезжирить этиловым спиртом, высушить, про-
маркировать.
3.Взвесить образцы исследуемых металлов на аналитических весах.
4.Загрузить образцы в печь. Зафиксировать время. При загрузке в печь рас-
полагать образцы в тиглях так, чтобы они не экранировали друг друга.
5.По окончании процесса коррозии достать образцы из печи, охладить и описать их внешний вид.
6.Удалить продукты коррозии в соответствующих растворах или ластиком.
7.После удаления продуктов коррозии образцы тщательно промыть, проте-
10
реть этиловым спиртом, высушить.
8.Взвесить образцы без продуктов коррозии.
9.Экспериментальные данные записать в табл. 1.1.
Таблица 1.1
Экспериментальные данные по газовой коррозии
|
Изме- |
Пло- |
Масса |
Масса |
Внеш- |
|
Кол-во |
Показатели кор- |
|
N |
няю- |
щадь |
образца |
образца |
ний |
вид |
прокор- |
розии |
|
|
щийся |
образца, |
до кор- |
после |
образца |
|
родиро- |
|
|
п/п |
фактор |
S, см2 |
розии, |
коррозии, |
после |
|
вавшего |
Массов. |
Глубин. |
|
|
|
m1, г |
m2, г |
коррозии |
металла, |
г/см2час |
мм/год |
|
|
|
|
|
|
|
|
m, г |
|
|
|
|
|
|
|
|
|
|
|
|
1.3.Обработка экспериментальных данных
1.По количеству прокорродировавшего металла определить массовый пока-
затель коррозии Кm = m/St г/см2 ·ч.
2. Исходя из средней величины Km, полученной при обработке параллель-
ных опытов, определить глубинный показатель коррозии П (П=Кm/g), где g -
плотность металла, г/см3. Выразить глубинный показатель в мм/год и по его вели-
чине в соответствии с таблицей коррозионной стойкости металлов определить жаростойкость металла в исследуемых условиях (таблица П.1 Приложения).
3. Построить график зависимости "скорость коррозии - изменяющийся фак-
тор", пояснить его ход и соответствие с теорией. 4. Сделать выводы.
1.4. Правила техники безопасности
При выполнении работы соблюдать меры безопасной работы с электронагре-
вательными приборами. Загрузка и выгрузка тиглей с образцами в печь произво-
дится с помощью специальных щипцов, руки при этом защищаются перчатками.
Тигли после выгрузки из печи ставятся на мраморную подставку. Перед дальней-
шей работой с образцами их необходимо остудить. Снятие продуктов коррозии производится в чашках Петри, которые располагаются в пластмассовой кювете.
11
После травления образцы погружаются в стакан с водой, также находящийся в кювете, и только затем окончательно промываются в раковине под струей воды.
Использованные для травления кислоты с помощью воронки сливаются обратно в соответствующие колбы. Перед взвешиванием образцы сушатся фильтровальной бумагой и протираются спиртом.
Лабораторная работа 2
ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ МЕТАЛЛОВ И АНАЛИЗ
КОРРОЗИОННОЙ СИТУАЦИИ
Цель работы: ознакомиться с понятием электрохимической коррозии металлов,
научиться проводить анализ коррозионного процесса исходя из рН и состава кор-
розионной среды.
2.1. Теоретические предпосылки
Процесс электрохимической коррозии наблюдается всегда, когда на поверх-
ности металла появляется электролит. В строительной практике электрохимиче-
ская коррозия - это коррозия металлических конструкций в условиях атмосфер-
ной, подводной и грунтовой коррозии, это коррозия арматуры во влажном бетоне,
коррозия транспорта и т.д. При электрохимической коррозии на поверхности ме-
талла одновременно протекают две электрохимические реакции: реакция иониза-
ции металла (анодная реакция коррозионного процесса), реакция восстановления какого-либо окислителя (лей), присутствующего (щих) в коррозионной среде (ка-
тодная реакция коррозионного процесса).
Корродирующий в электролите металл за счет одновременного протекания на нем двух электрохимических реакций, связанных с переносом электронов,
приобретает потенциал, который называют потенциалом коррозии Е . Этот по-
кор
тенциал измеряют с помощью вольтметра, если имеется электрод сравнения с из-
вестным потенциалом (например, хлорсеребряный электрод сравнения с потен-
12
циалом + 0,201 В).
Катодная реакция коррозионного процесса заключается в восстановлении окислителя, каковым в строительной практике обычно является растворенный в коррозионной среде кислород:
O2 + 4Н+ + 4е ↔ 2H2O |
или 02 + 2H2O + 4е ↔ 40Н- |
(кислая среда) |
(нейтральная или щелочная среда) |
Вторым по распространенности окислителем являются ионы водорода (Н+), в |
|
некоторых случаях в коррозионной среде могут присутствовать и другие окисли-
тели (например, SO2, H2S и т.д.).
+
Если в качестве одного из окислителей выступают ионы Н, что обычно ха-
рактерно для кислых сред, тогда коррозия металла сопровождается выделением водорода. В этом случае катодная реакция коррозионного процесса следующая:
2Н+ + 2е ↔ H2 |
или 2H2O + 2е ↔ Н2 + 20Н- |
(кислая среда) |
(нейтральная или щелочная среда) |
Анодная реакция коррозионного процесса может протекать разными путями,
что приводит к появлению на поверхности металла или в коррозионной среде
разнообразных продуктов коррозии (ими могут быть оксиды, гидроксиды, ком-
плексные соединения, растворимые в коррозионной среде соли, труднораствори-
мые соли).
гидратированные катионы[Ме(Н2О)]ne+ комплексные соединения[Ме(Кn)]m+, [Ме(Кn)]m-
Ме - ne |
оксиды и гидроксиды МеО, Ме(ОН)2 |
2- |
|
- |
|
|
сложные анионы металла МеО2, МеО2 |
|
труднорастворимые соли МеА
Вид образующихся продуктов оказывает решающее влияние на скорость, и
следовательно, на опасность коррозии.
Наиболее опасен для практики случай, когда в результате анодной реакции коррозионного процесса получаются растворимые продукты коррозии(гидрати-
рованные катионы, сложные анионы металла, комплексные соединения). Такие продукты не оказывают тормозящего влияния на скорость коррозии, и, следова-
тельно, она постоянно идет с высокой скоростью.
13
Если в результате анодной реакции коррозионного процесса получаются не-
растворимые продукты коррозии (оксиды, гидроксиды, труднорастворимые соли),
то такие продукты обычно снижают скорость коррозии во времени, и тем в боль-
шей степени, чем выше степень упорядоченности(плотности) получаемых про-
дуктов коррозии. В том случае, когда нерастворимые продукты коррозии получа-
ются с очень высокой степенью упорядоченности, коррозия резко тормозится во времени, продукты коррозии защищают металл, и он становится пассивным(яв-
ление пассивности).
Таким образом, чтобы проанализировать коррозионную ситуацию и оценить опасность коррозии необходимо выяснить:
1) какие катодные реакции идут на поверхности металла при коррозии, т.е.
какие окислители ее вызывают; 2) по какому пути идет анодная реакция коррозионного процесса, т.е. какие
продукты коррозии получаются: растворимые, нерастворимые, упорядоченные,
неупорядоченные.
Чтобы ответить на поставленные вопросы, необходимо знать состав коррози-
онной среды, ее рН и измерить значение стационарного потенциала коррозии
(Екор).
Исходя из состава коррозионной среды прежде всего определяется, какие окислители в ней присутствуют. Обычно их как минимум два: ионы водорода (Н+)
и растворенный в коррозионной среде кислород (O2). Иногда в коррозионной сре-
де могут быть и дополнительные окислители(Fе3+, N0з-, S2- и т.д.). Чтобы узнать,
какие из этих окислителей участвуют в процессе коррозии, необходимо сравнить стационарный потенциал коррозии(Екор) с равновесными потенциалами этих окислителей (Eoxpaвн). Если выполняется соотношение
Екор < Е охравн ,
то данный окислитель участвует в процессе коррозии.
Это соотношение проверяется для всех окислителей, которые присутствуют в
ох
данной коррозионной среде, причем значения Е равн находятся в литературе или рассчитываются, например:
14 |
|
Е равнН2 = -0,06 рН; Е Оравн2 =1,23 - 0,06рН |
(2.1) |
В дальнейшем, также с учетом состава коррозионной среды, ее рН и величи-
ны стационарного потенциала коррозии(Екор), определяется возможный путь анодной реакции коррозионного процесса и, следовательно, получающиеся про-
дукты коррозии. Если в коррозионной среде присутствует комплексообразова-
тель, способный образовывать с корродирующим металлом растворимые ком-
плексы, то продуктами коррозии будут именно эти комплексы и опасность корро-
зии резко возрастает.
В том случае, когда в коррозионной среде имеются анионы, способные обра-
зовывать с корродирующим металлом труднорастворимые соли, эти соли в той или иной мере обязательно будут оказывать тормозящее влияние на коррозию и опасность ее уменьшается, а в некоторых случаях коррозия практически прекра-
щается (явление солевой пассивации). Если в коррозионной среде отсутствуют комплексообразователи и анионы, способные давать труднорастворимые соли, то дальнейшие предположения о характере образующихся продуктов делают с -по мощью диаграмм Пурбе при известных рН коррозионной среды и стационарном потенциале коррозии. Диаграммы Пурбе дают представление о наиболее термо-
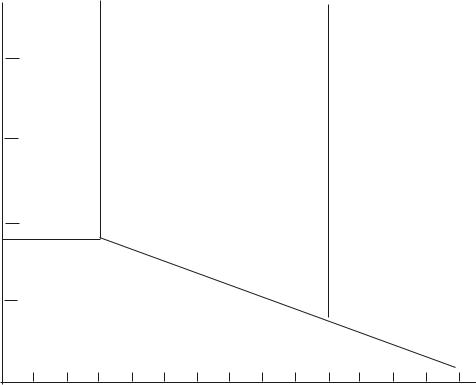
динамически устойчивых соединениях металла в зависимости от его потенциала и рН коррозионной среды. Пример такой диаграммы для алюминия приведен на рис. 2.1.
|
|
|
|
|
15 |
|
|
|
|
|
|
|
|
|
Е, В |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-0,8 |
Al3+ |
|
|
|
Al O |
|
|
|
|
|
AlO |
- |
|
|
|
|
|
|
3 |
|
|
|
|
|
|||||
|
|
|
|
|
2 |
|
|
|
|
|
|
2 |
|
|
-1,2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-1,6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-2,0 |
|
|
|
Al |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 рН |
|
Рисунок 2.1- Диаграмма Пурбе для алюминия |
|
|
||||||||||||
Согласно диаграмме, алюминий в средах, близких к нейтральным (рН 3-10),
корродирует с образованием упорядоченного нерастворимого оксида алюминия
A12О3, который хорошо защищает металл от дальнейшей коррозии, поэтому в этих средах алюминий устойчив. В кислых (рН<3) и щелочных (рН>10) средах получаются растворимые продукты коррозии А13+ и AlО2-, они не могут оказы-
вать тормозящего влияния на коррозию, и в этих средах алюминий не устойчив
(алюминий относится к классическим амфотерным металлам). Применять алюми-
ний и его сплавы в кислых и щелочных средах без специальных мероприятий по защите нельзя.
Для примера можно проанализировать, коррозию железа в растворахNa2S04
с рН 2, рН 7, рН 12, если известно, что потенциалы коррозии железа (Екор) в этих средах соответственно равны: -0,35, -0,40 и -0,46 В (н.в.э.).
Прежде всего рассматривают, какие окислители могут быть в этих растворах.
16
Так как речь идет о водных растворахNa2S04, то ясно, что в них есть ионы водо-
рода Н+ и растворенный кислород О2, ионы Na+, S042- окислителями не являются.
Равновесные потенциалы этих двух окислителей для растворов с различным рН могут быть рассчитаны по уравнениям (2.1) и соответственно равны
рН = 2 |
Е равнН2 |
= -0,12 В, |
Е Оравн2 |
=1,11 В |
рН = 7 |
Е равнН2 |
= -0,42 В, |
Е равнО2 |
= 0,81 В |
рН =12 |
Е равнН2 = -0,72 В, |
Е равнО2 = 0,51 В |
||
Если проверить, когда выполняется соотношение Екор < Еохравн , то можно за-
метить, что при рН=2 коррозия протекает под действием обоих окислителей, а
при рН=7, и рН=12 в коррозионном процессе участвует только один окислитель
O2.
Далее нужно проанализировать, по какому пути пойдет анодная реакция кор-
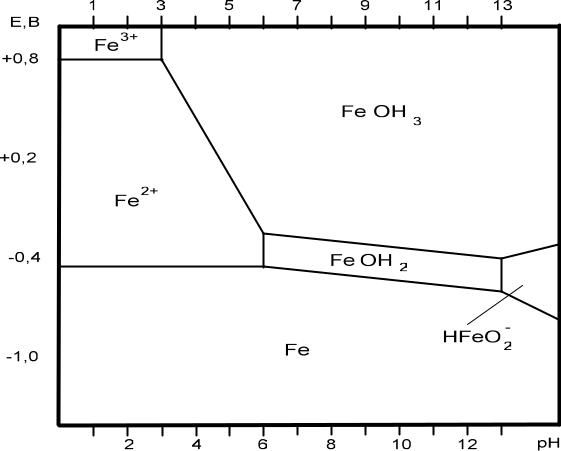
розионного процесса. В рассматриваемых растворах нет комплексообразователей и анионов, способных образовывать с железом труднорастворимые соли, поэтому можно сразу обратиться к диаграмме Пурбе для железа (рис. 2.2.).
Как видно из диаграммы, в растворах Na2S04 железо в зависимости от рН корродирует с образованием:
|
Fe2+, Fe3+ |
гидратированные катионы |
Fe – 2e |
Fe(OH)2, Fe(OH)3 |
гидроксиды |
|
FeO2- |
сложный анион металла |
Так, в растворе Na2SО4 с рН =2 (рис. 2.2) в качестве продукта коррозии по-
лучаются ионы Fe2+, которые в дальнейшем под действием кислорода, раство-
ренного в коррозионной среде, окисляются до ионов Fe3+ (т.е. коррозия идет с образованием растворимых солей железа). При этом продукты коррозии не ока-
зывают тормозящего влияния на скорость коррозии, поэтому в таких средах коррозия протекает быстро и тем быстрее, чем кислее коррозионная среда, так как количество основного окислителя ионов Н+ увеличивается.
17 |
|
|
( ) |
( |
) |
Рис. 2.2. Диаграмма Пурбе для железа |
|
В растворе Na2S04 с рН=7 в качестве продуктов коррозии образуется смесь нерастворимых гидроксидов (nFе(ОН)2·mFе(ОН)3·kH2O). Чтобы определить, на-
сколько сильно эти оксиды тормозят скорость коррозии, необходимо узнать, на-
сколько упорядоченными они получаются. Это можно выяснить, только поста-
вив опыт по коррозии железа в раствореNa2S04. Если такой опыт провести, то можно определить, что при таком рН оксиды получаются очень неупорядочен-
ные. Такие неупорядоченные оксиды на железе часто называют ржавчиной.
Ржавчина может снизить скорость коррозии только при достаточно большой толщине, в этой связи в раствореNa2S04 с рН=7 коррозия железа опасна и его необходимо защищать.
В щелочном раствореNa2S04 с рН=12, согласно диаграмме Пурбе, также получаются гидроксиды Fe(OH)2 и Fе(ОН)3, но, как показывает опыт, в данных условиях они получаются упорядоченными и хорошо защищают металл, поэто-
му в растворе Na2S04 с рН=12 железо пассивируется и становиться устойчивым.
