2579
.pdf
ее долю приходится менее 1 % всех |
10 % дисплазий. Часто она сосущест- |
|||||||
дисплазий. Чаще всего поражается |
вует с фибродисплазией медии. Боль- |
|||||||
основной ствол артерии. Изменения |
шинство больных с перимедиальной |
|||||||
наружного и внутреннего слоев арте- |
дисплазией — женщины в возрасте |
|||||||
рии отсутствуют, хотя при выражен- |
40—55 лет. Эти повреждения пред- |
|||||||
ном стенозе возможно развитие суб- |
ставляют |
собой |
концентрические |
|||||
эндотелиальной фиброплазии |
вто- |
или многочисленные стенозы, вов- |
||||||
ричного характера. |
|
лекающие основной ствол без интра- |
||||||
На долю |
фибродисплазии |
медии |
муральных аневризм. Отличительная |
|||||
приходится около 85 % дисплазий |
особенность |
перимедиальной дисп- |
||||||
почечных артерий. Больше чем 90 % |
лазий — чрезмерно плотная ткань |
|||||||
больных составляют женщины. На- |
при переходе медии в адвентицию. |
|||||||
иболее часто она диагностируется в |
Существует несколько подходов к |
|||||||
возрасте 30—35 лет. Хотя фибродис- |
классификации |
фибромускулярной |
||||||
плазии среднего слоя рассматрива- |
дисплазий. Исторически первой яв- |
|||||||
ются как системные артериопатии, |
ляется морфологическая классифи- |
|||||||
наиболее частая локализация прихо- |
кация поражений артерии на основа- |
|||||||
дится на почечные, экстракраниаль- |
нии вовлечения в процесс интимы, |
|||||||
ные отделы сонных артерий и наруж- |
медии или адвентиции сосудистой |
|||||||
ные подвздошные артерии. |
|
стенки. Все три вида поражения мо- |
||||||
Морфологически эта форма дисп- |
гут сочетаться, но всегда один из них |
|||||||
лазий может проявляться как еди- |
доминирующий [McCormac L. et al., |
|||||||
ничным концентрическим стенозом, |
1958; HuntG. et al., 1962]. |
|
||||||
так и множеством стенозов по типу |
В клинической практике наиболее |
|||||||
"четок бус", а также в виде аневриз- |
приемлемой является классификация |
|||||||
матического |
расширения сосудов. |
исходя |
из |
артериографических |
||||
Обычно поражается основной ствол, |
данных, примененная в отношении |
|||||||
но бывает, что поражение распро- |
поражений почечных артерий, на ос- |
|||||||
страняется и на дистальные отделы |
новании которой стенозы разделя- |
|||||||
приблизительно в 25 % случаев. |
ются на следующие виды: |
|
||||||
Перимедиальная дисплазия — до- |
• одиночные, или фокальные (ме- |
|||||||
минирующая патология, на долю ко- |
нее чем 1 см в длину); |
|
||||||
торой приходится приблизительно |
• множественные, или мультифо- |
|||||||
|
|
|
кальные, имеющие на ангиограмме |
|||||
|
|
|
вид "нитки бус"; |
|
|
|||
|
|
|
• концентрические, или тубуляр- |
|||||
|
|
|
ные, в виде цилиндрического суже- |
|||||
|
|
|
ния, охватывающего сосуд в виде |
|||||
|
|
|
ошейника [Мазо Е.Б., 1970; Покров- |
|||||
|
|
|
ский А. В., 1974]. |
|
|
|||
|
|
|
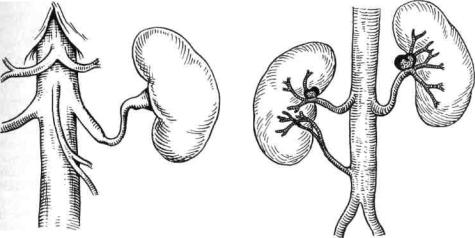
Преобладающая форма поражения |
|||||
|
|
|
почечных сосудов — множественные |
|||||
|
|
|
стенозы с преимущественной фиб- |
|||||
|
|
|
ромускулярной дисплазией медиаль- |
|||||
|
|
|
ного слоя сосудистой стенки. В этих |
|||||
|
|
|
случаях в процесс вовлекается также |
|||||
|
|
|
интима и адвентиция, но степень их |
|||||
|
|
|
повреждения |
значительно |
меньше |
|||
|
|
|
(рис. 7.101-7.103). |
|
||||
|
|
|
Этиопатогенетические механизмы |
|||||
|
|
|
фибромускулярной дисплазий окон- |
|||||
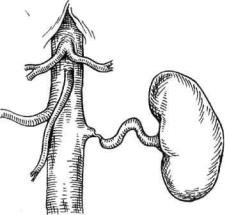
Рис. 7.101. Фокальное поражение почеч- |
чательно |
не |
установлены. |
Имеются |
||||
основания относить данное заболе- |
||||||||
ной артерии. |
|
|
||||||
446 |
|
|
|
|
|
|
|
|