
material / материаловеденье-1 / moi_otvety (2)
.docx1. Диффузия. Первый и второй законы Фика. Глубина диффузионного слоя в зависимости от времени и температуры
Диффузия – неравновесный процесс, частный случай явлений массопереноса, вызываемый тепловым молекулярным движением и приводящий к установлению равновесного распределения концентраций внутри фаз. Диффузия – процесс необратимый, приводящий к выравниванию химических потенциалов компонентов системы.
Главной характеристикой диффузии служит плотность диффузионного потока J - количество вещества, переносимого в единицу времени через единицу площади поверхности, перпендикулярной направлению переноса. Если в среде, где отсутствуют градиенты температуры, давления, электрического потенциала и др., имеется градиент концентрации с(х, t), характеризующий ее изменение на единицу длины в направлении х (одномерный случай) в момент времени t, то в изотропной покоящейся среде
J = -D(dс/dх), (1)
где D - коэффициент диффузии (м2/с); знак "минус" указывает на направление потока от больших концентраций к меньшим. Пространственно-временное распределение концентрации:
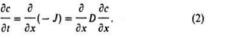
Уравнения (1) и (2) называются первым и вторым законами Фика.
Рассмотрим теперь диффузионные уравнения, связанные с законами Фика более подробно.
1.1 Однородная изотропная среда
В случае трехмерной диффузии первый закон Фика имеет вид:

Ур.1а дает скорость проникновения диффузанта через единицу поверхности некоторой среды при стационарном состоянии потока, выраженную через градиент концентрации и постоянную, называемую коэффициентом диффузии D. S- площадь поверхности, через которую проходит диффузионный поток. Второе уравнение определяет накопление диффузанта в определенной точке среды как функцию времени. Таким образом, это уравнение относится к нестационарному состоянию потока.

Необходимо учитывать, что при осложнении диффузии другими параллельно идущими процессами ход этого комплексного процесса должен описываться выражениями, отличными от вытекающих из решений «классических» уравнений диффузии. Предположение о постоянстве D оправдывается не всегда – часто коэффициент диффузии зависит от концентрации диффузанта, градиента концентрации, пространственной координаты и времени диффузионного эксперимента (а иногда – от всех этих параметров вместе). Несложно осуществить вывод уравнений диффузии, когда D не является постоянным. Уравнение первого закона Фика при этом остается неизменным, а при выводе уравнения второго закона D, как переменную величину не выносят за знак повторного дифференцирования.
35. Виды фаз в сплавах
Химические соединения образуются между компонентами, имеющими большое различие в электронном строении атомов и кристаллических решеток. Существуют устойчивые и неустойчивые химические соединения. У устойчивого строго определенная температура плавления, а у неустойчивого плавление происходит в интервале температур. Различают химические соединения с нормальной валентностью, электронные соединения и фазы внедрения.
Характерные особенности:
1 – кристаллическая решетка отличается от решеток компонентов, образующих соединение; обычно сложная кристаллическая решетка;
2 – в соединении всегда сохраняется простое кратное весовое соотношение элементов, АnВm где n и m простые числа;
3 – свойства соединения резко отличаются от свойств образующих его компонентов;
4 – температура плавления (диссоциации) постоянная;
5 – образование химического соединения сопровождается значительным тепловым эффектом.
Химические соединения с нормальной валентностью: Mg2Pb, MgS, Mg3Sb2 и др.
Соединения одних металлов с другими называются интерметаллидами. Химическая связь между атомами в интерметаллидах обычно металлическая. Пример: NiAl, Ni3Al,
Электронные соединения не подчиняются правилу валентности, но имеют определенную электронную концентрацию. Пример: - фаза СuZn с электронной концентрацией 3/2, -фаза Cu5Zn8 c электронной концентрацией 21/13 и - фаза CuZn3 с электронной концентрацией 7/4. Электронные соединения имеют также свою кристаллическую решетку, но в отличие от химических соединений с нормальной валентностью, имеют переменный состав.
Фазы внедрения – на основе химических соединений, фазы переменного состава. Образуют переходные металлы Fe, Mn, Cr, Mo с элементами, имеющими малый атомный радиус (углеродом, азотом, бором, водородом). При образовании фазы внедрения меняется решетка растворителя. Пример: TiC, Fe4N, W2C.
Фазы Лавеса имеют общую формулу АВ2, образуются между компонентами с соотношением атомных диаметров 1,2 (1,1 – 1,6). Имеют гексагональную или гранецентрированную кубическую решетки. Пример: CaAl2, AgBe2,TiCr2.
-фазы – образуют соединения переходных металлов, содержит примерно 50% каждого из образующих элементов. Обладает повышенной твердостью и хрупкостью, нежелательна в сплавах. Пример: FeCr, VMn, CoCr, FeMo.
Твердые кристаллические растворы. Твердыми растворами называют фазы переменного состава, в которых один из компонентов сохраняет свою кристаллическую решетку, а атомы другого располагаются в решетке первого, изменяя ее размеры.
Твердые растворы замещения образуются путем замены атомов растворителя атомами растворенного компонента.

Рисунок 1 – Кристаллические решетки твердого раствора замещения при неограниченной растворимости компонентов.
В зависимости от соотношения атомных радиусов растворяемого элемента и растворителя параметр решетки при образовании твердого раствора замещения может уменьшаться или увеличиваться. Твердые растворы замещения могут быть упорядоченными – атомы растворенного элемента занимают строго определенные узлы кристаллической решетки растворителя.
Твердые растворы внедрения образуются путем размещения атомов растворенного компонента в свободных промежутках между атомами решетки растворителя. Пример – твердый раствор углерода, азота, водорода и бора в - или -железе (т.е. растворяются элементы с малыми атомными радиусами с недостроенными внутренними электронными оболочками). Твердые растворы внедрения всегда имеют ограниченную растворимость, параметр кристаллической решетки увеличивается при образовании такого раствора. (рис.2)

Рисунок 2 – Схема твердого раствора внедрения
Твердые растворы вычитания (растворы с дефектной решеткой) образуются когда при добавлении растворяемого компонента узлы решетки, где должны быть атомы растворяемого компонента заполнены, а где атомы растворителя – свободны. Такие растворы образуются только на базе химических соединений. При образовании такого раствора происходит уменьшение параметра решетки.
В отличие от химических соединений при образовании твердых растворов:
1 – сохраняется тип кристаллической решетки растворяемого компонента;
2 – состав переменный;
3 – плавление происходит в интервале температур.
4 – для образования твердого раствора не требуется тепловой расход.
Общее :
1 – свойства образующих компонент меняются, но в значительно меньшей степени.
Взаимная растворимость компонентов.
Твердые растворы замещения с неограниченной растворимостью могу образовываться при соблюдении следующих условий:
1 – Кристаллические решетки компонентов должны быть одинаковы.
2 –Различие в атомных размерах компонентов должно быть незначительным и не превышать 8-15% (9 % для сплавов на основе железа).
3 – Компоненты должны принадлежать к одной и той же группе Периодической системы элементов или к смежным родственным группам и в связи с этим иметь близкое строение валентной оболочки электронов в атомах. Если не выполняется хотя бы одно из этих условий, растворимость ограничена.
Примеры твердых растворов с неограниченной растворимостью:
Ni-Cu, Ag-Au, Fe-Co, Fe-Cr и др.
48. Согласно ГОСТ 1412-85 серый чугун маркируют буквами «С» — серый и «Ч» — чугун. Число после буквенного обозначения показывает среднее значение предела прочности чугуна при растяжении. Например, СЧ 20 — чугун серый, предел прочности при растяжении 200 МПа.
Структура отливок определяется химическим составом чугуна и технологическими особенностями его термообработки. Механические свойства серого чугуна зависят от свойств металлической матрицы, формы и размеров графитовых включений. Свойства металлической матрицы чугунов близки к свойствам стали. Графит, имеющий невысокую прочность, снижает прочность чугуна. Чем меньше графитовых включений и выше их дисперсность, тем больше прочность чугуна. Графитовые включения вызывают уменьшение предела прочности чугуна при растяжении. На прочность при сжатии и твердость чугуна частицы графита практически не оказывают влияния. Свойство графита образовывать смазочные пленки обусловливает снижение коэффициента трения и увеличение износостойкости изделий из серого чугуна. Графит улучшает обрабатываемость резанием.
Серый чугун это сплав железа, кремния (от 1,2- 3,5 %) и углерода, содержащий также постоянные примеси Mn, P, S. В структуре таких чугунов большая часть или весь углерод находится в виде графита пластинчатой формы. Излом такого чугуна из-за наличия графита имеет серый цвет.
По свойствам серые чугуны можно условно распределить на следующие группы:
ферритные и ферритно-перлитные чугуны (марки СЧ 10, СЧ 15) применяют для изготовления малоответственных ненагруженных деталей машин;
перлитные чугуны (марки СЧ 20, СЧ 25, СЧ 30) используют для изготовления износостойких деталей, эксплуатируемых при больших нагрузках: поршней, цилиндров, блоков двигателей;
модифицированные чугуны (марки СЧ 35, СЧ 40, СЧ 45), получают добавлением перед разливкой в жидкий серый чугун присадок ферросилиция, такие чугуны имеют перлитную металлическую матрицу с небольшим количеством изолированных пластинок графита.
Чугун с вермикулярным графитом отличается от серого чугуна более высокой прочностью, повышенной теплопроводностью. Этот материал перспективен для изготовления ответственных отливок, работающих в условиях теплосмен (блоки двигателей, поршневые кольца).
21. Порог хладноломкости — температурный интервал изменения характера разрушения, является важным параметром конструкционной прочности. Чем ниже порог хладоломкости, тем менее чувствителен металл к концентраторам напряжений (резкие переходы, отверстия, риски), к скорости деформации.
Влияние различных факторов на хладноломкость металлов
Факторы, влияющие на хладноломкость металлов, можно разделить на 4 основные группы.
1. Внешние факторы: температура, условия и скорость нагружения.
2. Внутренние металлургические факторы: тип кристаллической решетки, химический состав, структура и размер зерна, загрязненность металла неметаллическими включениями, метод выплавки.
3. Конструктивные факторы: масштабный эффект, концентраторы напряжений.
4. Технологические факторы: состояние поверхности, остаточные напряжения, обусловленные технологией изготовления.
Внешние факторы
Помимо температуры, на сопротивление стали разрушению влияет характер приложения нагрузки. Как правило, повышение скорости нагружения способствует снижению сопротивления разрушению. При этом снижаются значения трещиностойкости и повышаются температуры вязко-хрупкого перехода. Известно, что аварии судов на море происходили при совместном действии низких температур и сильного волнения — штормовой погоды.
Внутренние металлургические факторы
Влияние структуры. Склонность к хрупкому разрушению при низких температурах зависит от кристаллической структуры металла.
Металлы с кристаллической решеткой объемноцентрированного куба (стали на основе α-железа, вольфрам, хром, молибден и др.), а также некоторые металлы с гексагональной плотноупакованной решеткой (цинк, кадмий, магний) относятся к хладноломким металлам. Титан, хотя и имеет решетку ГП, но сохраняет пластичность и при низких температурах. Металлы с решеткой гранецентрированного куба (аустенитные стали, медь, алюминий, никель) не склонны к хладноломкости.
Влияние легирующих элементов на механические свойства сталей с ОЦК-решеткой. Механические свойства и разрушение сталей зависят от структуры, которая в первую очередь определяется химическим составом, размером действительного зерна и состоянием его границ, видом и характером неметаллических включений.
Влияние легирующих элементов на свойства стали обусловлено их действием на измельчение зерна, упрочнение феррита за счет образования твердых растворов внедрения и замещения, упрочнением за счет выделения частиц второй фазы различной степени дисперсности и изменением прокаливаемости.
Углерод, как и азот, являющийся эффективным упрочнителем, образует с железом твердые растворы внедрения. Однако его растворимость в феррите невелика, что приводит к снижению упрочняющего эффекта. Вместе с тем высокая прочность мартенсита закалки сопровождается снижением вязкости и необходимостью проведения отпуска. При отпуске образуются карбиды, мартенсит обедняется углеродом и снижается действие твердорастворного механизма упрочнения. Образующиеся довольно крупные частицы цементитного типа в ферритной матрице более тверды и хрупки, чем матрица. Поэтому при нагружении на поверхности раздела создается объемно-напряженное состояние, которое может приводить к образованию микротрещин.
Углерод повышает порог хладноломкости сталей и уменьшает ударную вязкость при температурах выше критической температуры (рис. 13.5). Увеличение в отожженной и нормализованной стали содержания углерода на 0,1 % повышает порог хладноломкости на 20 °С.
Легирующие элементы оказывают влияние на свойства феррита, положение критических точек в стали, кинетику γ ↔ α-превращения и размер зерна.
Одновременное повышение твердости, прочности и ударной вязкости обеспечивает никель во всем диапазоне концентраций и марганец в количестве до 2,0 %. Хром мало влияет на твердость феррита, но при содержании до 1,5 % увеличивает его вязкость. Увеличение содержания кремния более 0,8 % приводит к резкому снижению ударной вязкости. Кремний и марганец во всем исследованном диапазоне концентраций значительно повышают твердость феррита. Введение в сталь марганца до 2 % и кремния до 0,8 % приводит к заметному упрочнению ферритной матрицы, почти не ухудшая ее пластичности и вязкости.
Влияние микролегирования и размеров зерен на хладостойкость. Большое влияние на характер разрушения оказывает размер зерна стали. При измельчении зерна растет предел текучести и одновременно снижается температура перехода в хрупкое состояние. Увеличение средних размеров зерен малоперлитной низколегированной стали от 15 до 50 мкм за счет изменения режима аустенитизации и скорости охлаждения приводит к повышению критической температуры на 60 °С и снижению ударной вязкости на 40–50 Дж/см2.
Влияние вредных примесей и газов.
Модифицирование
Резко отрицательное действие на хладостойкость оказывают вредные примеси: фосфор и сера. Растворяясь в феррите, фосфор заметно искажает кристаллическую решетку твердого раствора и повышает температуру перехода в твердое состояние. Охрупчивающее влияние фосфора усиливается при обогащении им межзеренных границ благодаря развитию ликвационных процессов. Обогащение фосфором границ аустенитных зерен может также явиться следствием перераспределения примесей из-за неодновременного протекания процессов превращения неравновесных структур. Обратимая отпускная хрупкость способствует не только абсолютному уменьшению уровня ударной вязкости, но и существенному повышению порога хладноломкости. Легирование молибденом снижает как склонность стали к отпускной хрупкости, так и порог хладноломкости. Повышение содержания фосфора на 0,01 % в литой стали 35Л увеличивает критическую температуру хрупкости на 20 °С.
В отличие от фосфора сера практически нерастворима в феррите и присутствует в стали в виде сульфидов. Сернистые включения могут иметь вид обособленных сульфидов и в виде строчек располагаются по границам зерен. Последний вид включений особенно вреден с точки зрения хладостойкой стали, так как приводит к ослаблению границ зерен и затрудняет пластическую деформацию. Введение марганца в жидкую сталь приводит к образованию сульфида марганца вместо сульфида железа, что несколько уменьшает вредное влияние серы. Однако сульфиды марганца пластичны при температурах горячего деформирования и не улучшают ударную вязкость в направлении, перпендикулярном направлению прокатки. Увеличение содержания серы в литой стали 25Л от 0,02 до 0,05 % более чем в два раза снижает ударную вязкость при –40 °С.
62. Отжиг – процесс термической обработки, заключающийся в нагреве стали до определенной температуры и последующее, как правило, медленное охлаждение с печью с целью получения более равновесной структуры.
Отжиг I рода – характерная особенность этого отжига состоит в том, что устранение неоднородности происходит независимо от того, протекают ли в сплавах при этой обработке фазовые превращения или нет, поэтому отжиг I рода можно производить при температурах выше или ниже температур фазовых превращений. К этому типу отжига относятся:
– гомогенизационный отжиг – применяют для слитков легированной стали с целью уменьшения дендритной или внутрикристаллитной ликвации, которая повышает склонность стали обрабатываемой давлением, к хрупкому разрушению, к анизотропии свойств и возникновению таких дефектов, как шиферность (слоистый излом) и флокены (тонкие внутренние трещины, наблюдаемые в изломе в виде белых овальных пятен); нагрев слитков до 1100-12000С, выдержка при этой температуре 8-15 часов, медленное охлаждение с печью до 2000С; процесс продолжается около 80 – 100 часов;
– рекристаллизационных отжиг – нагрев холоднодеформированной стали выше температур начала рекристаллизации, выдержку при этой температуре с последующим охлаждением; цель – устранить наклеп после деформации, привести структуру в равновесное состояние перед следующим этапом холодного деформирования;
– высокий отпуск – проводят для уменьшения твердости, нагрев до температуры ниже точки А1 (650-7000С) в течение 3-15 часов и медленное охлаждение; структура стали – феррит и зернистый или пластинчатый перлит; применяют для улучшения обработки резанием (структурно свободный феррит налипает на кромки режущего инструмента);
– отжиг для снятия остаточных напряжений – применяют для отливок, сварных изделий, деталей после обработки резанием и др., проводят при температуре 160-7000С с последующим медленным охлаждением; цель – снятие остаточных напряжений, возникших в результате неравномерного охлаждения, неоднородной пластической деформации и т.п. после сварки, обработки резанием и т.д.
Отжиг II рода (фазовая перекристаллизация) – нагрев стали до температур выше точек АС1 или АС3, выдержке и медленном охлаждении. При этом протекают фазовые α→γ превращения, определяющие структуру и свойства стали. Различают следующие виды отжига:
^ Полный отжиг – нагрев доэвтектоидной стали на 30-500С выше температуры АС3, выдержке при этой температуре до полного прогрева и завершения фазовых превращений в объеме металла и последующем медленном охлаждении (рис.2). при этом отжиге происходит полная фазовая перекристаллизация стали.
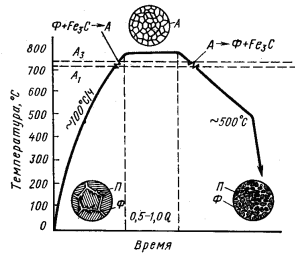
^ Рисунок 2 – Схема полного отжига доэвтектоидной стали
Изотермический отжиг – состоит обычно в нагреве легированной стали, как и для полного отжига, и в сравнительно быстром охлаждении до температуры, лежащей ниже точки А1 (обычно 660-6800С). При этой температуре проводят изотермическую выдержку 3-6 часов для полного распада аустенита, затем – охлаждение на воздухе (рис.3)
Изотермическому отжигу чаще подвергают поковки, штамповые заготовки, сортовой прокат из легированной цементуемой стали небольших размеров.
Патентирование – применяют для пружинной (канатной) проволоки, после изотермического отжига и полной аустенизации пропускают через расплавленную соль температуроц 450-5500С; в результате распада аустенита образуется тонкопластинчатый троостит или сорбит, на такой структуре возможны большие обжатия без обрывов при холодном волочении и прочность σв =2000-2250 Мпа.
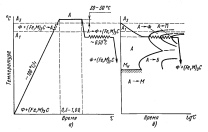
^ Рисунок 3 – Схема изотермического отжига:
а – график отжига; б – изотермическая диаграмма с кривой охлаждения при изотермическом отжиге
Неполный отжиг – сталь нагревают до более низкой температуры (немного выше А1). Для доэвтектоидных сталей такой отжиг улучшает обрабатываемость резанием. Для заэвтектоидных и легированных сталей такой отжиг называется сфероидизацией, поскольку приводит к образованию зернистого (сфероидального) перлита вместо пластинчатой. Температуры сфероидизации для заэвтектоидных углеродитсых сталей 770-7900С, для эвтектоидных – 750-7600С, для легированных заэвтектоидных – 770-8200С. Охлаждение при сфероидизации медленное.
Сфероидизации подвергают тонкие листы и прутки из низко- и среднеуглеродистой стали перед холодной штамповкой или волочением для повышения пластичности. Кроме того, для улучшения обработки резанием: повышения соростей резания и достижения наилучшей чистоты поверхности.
Нормализация – нагрев доэвтектоидной стали до температуры, превышающей точку АС3 на 40-500С, заэвтектоидной стали – выше точки АСТ на 40-500С, непродолжительная выдержка при этой температуре для прогрева садки и завершения фазовых превращений и охлаждение на воздухе. Происходит полная фазовая перерекристаллизация стали, устраняется крупнозернистая структура после литья или прокатки, ковки, штамповки. Охлаждение на воздухе (можно считать его ускоренным) приводит к распаду аустенита при более низких температурах с образованием дисперсной ферритно-цементитной структуры.
