
- •Стистическая физика
- •РАСПРЕДЕЛЕНИЕ ГИББСА
- •1. Каноническое распределение
- •2 Свободная энергия и статистическая сумма
- •3 Распределение Максвелла
- •4. Большое каноническое распределение
- •5. Свяь большого канонического распределения с каноническим
- •ИДЕАЛЬНЫЕ ГАЗЫ
- •1 Распределение Больцмана
- •2 Термодинамические функции и уравнение состояния идеального газа
- •3. Теорема о равномерном распределении кинетической энергии по степеням свободы и теорема о вириале
- •4 Многоатомные газы. Вращение молекул
- •5 Уравнение состояния и статистический интеграл двухатомного газа
- •Распределение Ферми-Дирака и Бозе-Энштейна
- •1. Общие свойства ферми- и бозе-газов
- •2. Статистика Бозе
- •3. Статистика Ферми
- •5. Ферми- и Бозе-газы элементарных частиц
- •6 Вырожденный электронный газ
- •7 Черное излучение
- •8. Вырожденный Бозе-газ. Конденсация Бозе - Эйнштейна
- •Реальный газ. Групповое разложение в теории газов
- •Уравнение Ван-дер-Ваальса
- •ФЛУКТУАЦИИ
- •1. Флуктуации энергии
- •2 Флуктуации числа частиц в заданном объеме
- •3. Функции распределения и моменты распределения случайной непрерывной величины. Нормальное распределение
- •4. Флуктуации основных термодинамических величин

Статфизика |
40 |
Реальный газ. Групповое разложение в теории газов
Ранее мы уже обсуждали, что энергия Е (р, q) в классическом распределении Гиббса представляет сумму кинетической энергии К и потенциальной энергии U:
Е (p, q) = K(p) + U (q); |
(1) |
Вероятность нахождения подсистемы в элементе dpdq ее фазового объема:
Статистическая сумма может быть рассчитана по формуле
Z N =Z N QN
где
Z N =∫exp[−KkT p ]d , которую легко рассчитать, что мы неоднократно делали, а QN - величина называемая конфигурационным интегралом.
QN =∫...∫exp |
[ |
−U N q1, .. ,qN |
] |
dq1 .. dqN |
(2) |
|
|
kT |
|||||
V V |
|
|
|
|||
F =−kT ln Z N =−kT ln Z N−kT ln QN
Вычисление конфигурационного интеграла для системы взаимодействующих частиц представляет собой сложную задачу.
Рассмотрим газ, в котором взаимодействие молекул описывается парным потенциалом взаимодействия, который быстро спадает с расстоянием. Эта задача была решена в 1937 г. Дж. Майером, развившим метод группового, или кластерного, разложения.
Кратко обсудим основные идеи этого метода.
Рассмотрим в объеме V газ из N одноатомных молекул, взаимодействующих посредством центральных сил, характеризуемых взаимным потенциалом
На больших расстояниях атомы притягиваются, а на достаточно малых — отталкиваются, так что график функции Ф(r) имеет вид, изображенный на рис. 45.
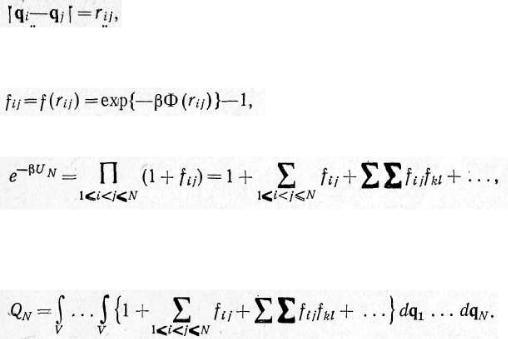
Статфизика |
41 |
Расстояние между центрами частиц - σ, при котором энергия отталкивания начинает резко увеличиваться, можно назвать их диаметром.
При расчетах в теории газов и жидкостей часто используется межмолекулярный потенциал Леннарда—Джонса:
Ф r =4 [ /r 12− /r 6 ]
где ε и σ — постоянные, имеющие размерность энергии и длины соответственно. σ — эффективный диаметр частицы, определяемый из равенства Ф(r)=0. Величина ε
определяет глубину потенциальной. Рассмотрим газ при температурах T>ε, когда устойчивый комплекс из двух молекул не образуется.
Потенциал Ф(r) настолько быстро убывает с расстоянием, что практически обращается в нуль при r = R~5σ.
Поскольку имеется только парное взаимодействие, то потенциальная энергия газа, равна
U N q1 , ... ,qN = |
∑ Ф qi−q j |
|
1 i j N |
так что подынтегральная функция в (2) превращается в произведение, в каждый множитель которого входят координаты двух молекул
e− U N q1 , ..., qN = ∏ |
exp − Ф qi −q j , |
= |
1 |
|
kT |
||||
1 i j N |
|
|
Для больших значений аргумента
при которых Ф (r) равен нулю, любой из множителей правой части равенства обращается в единицу. Поэтому для исследования конфигурационного интеграла Майер ввел функцию
которая обращается в нуль при больших значениях аргумента. Тогда произведение (15.7) может быть разложено в виде суммы
в которой каждое слагаемое соответствует распределению частиц на определенные группы и обращается в нуль, если аргумент функции Майера достаточно велик хотя бы для одной пары индексов.
С учетом этого можно получить групповое разложение конфигурационного интеграла
При вычислении вкладов в QN от взаимодействия различных групп используется
диаграммная техника: каждому члену разложения сопоставляется геометрический образ — диаграмма или граф: переменным q1,...,qN приводится в соответствие пронумерованный кружок, а множителям fij — линия, соединяющая i-ый и j-ый кружки. Например,
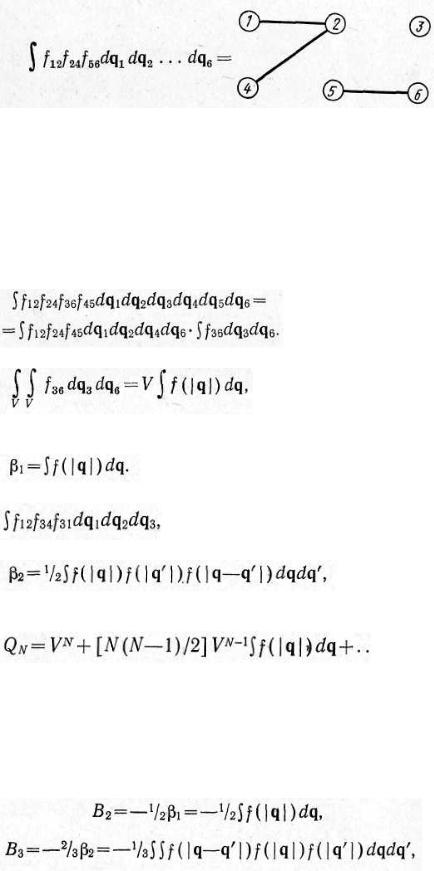
Статфизика |
42 |
Таким образом, выражение для конфигурационного интеграла представляет собой сумму всех различных графов из п кружков — n-частичных графов. При этом первому члену в соответствует граф без соединительных линий, второму члену — N (N—1)/2 графов с одной линией, третьему члену — графы с двумя линиями и т. д.
Графы называются связными, если все кружки прямо или косвенно (через другие кружки) связаны друг с другом, и несвязными, если в них имеются изолированные друг от друга группы (кружков или отдельные кружки. Сложный граф (интеграл) приводится к графам более простым, .(т. е. к далее неприводимым интегралам βi,). Например,
Взаимодействию одной пары частиц .соответствует вклад
и получающийся здесь интеграл называется первым неприводимым интегралом (неприводимой диаграммой или неприводимым графом):
Взаимодействие трех частиц определяется одним из интегралов вида
который выражается через второй неприводимый интеграл
Интегрируя по конфигурациям всей системы, получаем
В термодинамическом пределе (N→∞, V→∞, V=V/N=CONST) ряд удается формально просуммировать и свести к более простому ряду только связных диаграмм по. обратным степеням удельного объема v:
∞ |
1 Bi |
|
N |
||
|
|
||||
QN =[V exp i∑=2 |
|
|
|
] |
|
i−1 |
vi−1 |
|
|||
где Bi — вириальные коэффициенты:
Тогда находят вириальное разложение для энергии Гельмгольца реального газа:
Для идеального газа вириальные коэффициенты B2, B3 и т.д. равны нулю, т.е.

Статфизика |
43 |
QN =[V ]N
. И мы получали соотношение
тогда
где Fид— энергия Гельмгольца идеального газа. Вириальное уравнение состояния
P=− ∂∂VF
pV |
∞ |
1 Bi |
||||
=1 ∑ |
||||||
kT |
|
|
i |
−1 |
||
i=2 |
i−1 v |
|||||
В свое время считалось, что вириальное уравнение состояния может описать тройную точку и критические явления. Однако эти надежды не оправдались. При высокой плотности (жидкость) характер сходимости вириального ряда резко ухудшается, становится необходимым знание большего числа членов, а практический расчет вириальных коэффициентов ограничен трудностями вычисления многократных интегралов. В настоящее время проведен расчет семи вириальных коэффициентов системы твердых сфер и нескольких низших коэффициентов для более реалистических потенциалов. Поэтому важным является вопрос о повышении скорости сходимости рядов разложения термодинамических функций.
Уравнение Ван-дер-Ваальса
Если газ не очень плотный, то среднее расстояние между молекулами велико по сравнению с их размерами. Поэтому можно считать, что чаще всего сталкиваются только две молекулы, столкновение же трех, четырех и более частиц :Встречается редко, и 'ими можно пренебречь. В этом приближении из получаем уравнение состояния реального газа малой плотности
p= NkTV 1 Bv2
второй вириальный коэффициент
Θ=kT
4π появилось при переходе к сферическим координатам (поле имеет центральную симметрию).
Далее, разобьем на два интеграла

Статфизика |
44 |
В первом интеграле экспонента близка к нулю практически во всем интервале r.
а во втором разложим в ряд полагая, что kT>> ε (ε−глубина потенц. ямы см. Рис.), т.к. при сближении частицы сталкиваются и не образуют молекулу
Тогда B2
введем обозначение
b =b N =2 3 |
N |
|
1 |
3 |
|
|
|
|
величина
b ~∫r 2 dr - объему молекулы (σ - размеры молекулы), т.е. b1~ объему всех молекул
0
Второй коэффициент пропорционален энергии притяжения всех молекул
От уравнения состояния идеального газа это уравнение отличается двумя слагаемыми. Первоеобъем молекул реального газа, а второе характеризует уменьшение давления на стенки соссуда за счет притяжения молекул друг к другу.
