
- •РЕГУЛЯЦИЯ
- •Организация химических реакций в метаболические пути
- •В ряде случаев пространственная организация ферментов настолько сильно выражена, что продукт реакции ни
- •Органоспецифичность
- •Компартментализация
- •2. Структура метаболических путей
- •Принципы регуляции метаболических путей
- •Регуляция скорости ферментативных реакций осуществляется на 3 независимых уровнях:
- •1. Регуляция количества молекул фермента в клетке
- •2. Регуляция скорости ферментативной реакции доступностью молекул субстрата и коферментов
- •3. Регуляция каталитической активности ферментов
- •Изостерическая регуляция
- •Изостерическим ингибитором СДГ является также оксалоацетат, который регулирует, таким образом, заключительные этапы цикла
- •Аллостерическая регуляция
- •Роль аллостерических ферментов в метаболизме клетки.
- •- при катаболических процессах.
- •Аллостерические эффекторы.
- •Более редкий случай аллостерической регуляции, когда
- •Выявить ферменты с аллостерической регуляцией можно, изучая кинетику этих ферментов.
- •S-образная кривая зависимости скорости реакции от концентрации субстрата
- •Работа регуляторных субъединиц АКТ-азы
- •Кооперативное связывание
- •Коэффициент Хилла h – безразмерная величина, характеризующая кооперативность связывания лиганда ферментом
- •Графическое определение коэффициента Хилла
- ••Для изостерических ферментов, у которых кооперативного взаимодействия между активными
- •Особенности строения и функционирования аллостерических ферментов:
- •-аллостерические ферменты обладают свойством кооперативности: взаимодействие аллостерического эффектора с аллостерическим центром вызывает последовательное
- •Локализация аллостерических ферментов в метаболическом пути.
- •Фермент, катализирующий превращение субстрата А в продукт В, имеет аллостерический центр для отрицательного
- •В центральных метаболических путях исходные вещества могут быть активаторами ключевых ферментов метаболического пути.
- •В качестве примера можно рассмотреть принципы регуляции гликолиза - специфического (начального) пути распада
- •Регуляция каталитической активности ферментов белок-белковыми взаимодействиями.
- •Активация ферментов в результате присоединения регуляторных белков.
- •В мембране аденилатциклаза функционирует в комплексе с другими белками:
- •Регуляция каталитической активности ферментов ассоциацией/диссоциацией протомеров
- •Протеинкиназа А (цАМФ-зависимая) состоит из 4 субъединиц 2 типов: 2 регуляторных (R) и
- •Регуляция каталитической активности ферментов путём фосфорилирования/дефосфорилирования
- •Регуляция каталитической активности ферментов частичным (ограниченным) протеолизом
- •Частичный протеолиз - пример регуляции, когда активность фермента изменяется необратимо.
- •Рассмотрим механизм частичного протеолиза на примере активации протеолитического фермента трипсина.
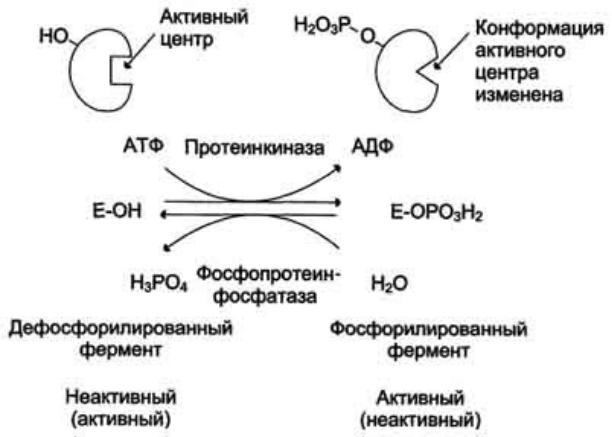
Регуляция каталитической активности ферментов путём фосфорилирования/дефосфорилирования
В биологических системах часто встречается механизм регуляции активности ферментов с помощью ковалентной модификации аминокислотных остатков. Быстрый и широко распространённый способ химической модификации ферментов - фосфорилирование/дефосфорилирование. Модификации подвергаются ОН-группы фермента. Фосфорилирование осуществляется ферментами протеинкиназами, а дефосфорилирование - фосфопротеинфосфатазами.
Присоединение остатка фосфорной кислоты приводит к изменению конформации активного центра и его каталитической активности. При этом результат может быть двояким: одни ферменты при фосфорилировании активируются, другие, напротив, становятся менее активными.
Регуляция каталитической активности ферментов частичным (ограниченным) протеолизом
Некоторые ферменты, функционирующие вне клеток (в ЖКТ или в плазме крови), синтезируются в виде неактивных предшественников и активируются только в результате гидролиза одной или нескольких определённых пептидных связей, что приводит к отщеплению части белковой молекулы предшественника.
В результате в оставшейся части белковой молекулы происходит конформационная перестройка и формируется активный центр фермента.
Частичный протеолиз - пример регуляции, когда активность фермента изменяется необратимо.
Такие ферменты функционируют, как правило, в течение короткого времени, определяемого временем жизни белковой молекулы.
Частичный протеолиз лежит в основе активации протеолитических ферментов, белков свёртывающей системы крови и фибринолиза.
Рассмотрим механизм частичного протеолиза на примере активации протеолитического фермента трипсина.
Трипсиноген, синтезируемый в поджелудочной железе, при пищеварении по протокам поджелудочной железы поступает в двенадцатиперстную кишку, где и активируется путём частичного протеолиза под действием фермента кишечника энтеропептидазы. В результате отщепления гексапептида с N-конца формируется активный центр в оставшейся части молекулы.

