
- •Лекция №4. Содержание белков в продовольственном сырье и пищевых продуктах, их основные функции и состав
- •3. Состав белков.
- •1. Концентрация белков в сырье и продуктах
- •2. Функции белков
- •3. Состав белков
- •4. Аминокислоты, их классификация
- •5 Свойства аминокислот
- •Х и м и ч е с к и е с в о й с т в а
5 Свойства аминокислот
Ф и з и ч е с к и е с в о й с т в а. Аминокислоты представляют собой бесцветные кристаллические вещества. Большинство из них легко растворяются в воде и 80%-ном этаноле. Многие -аминокислоты обладают сладким вкусом, иногда с некоторым неприятным привкусом.
О п т и ч е с к и е с в о й с т в а. Стереоспецифичность— это характерная особенность живых клеток. Она подтверждает, что трехмерная структура биомолекул имеет чрезвычайно важное значение для их биологических функций. Аминокислоты являются оптически активными соединениями, за исключением глицина. Это объясняется наличием в -положении асимметрического или хирального атома углерода.
Формы L и D относятся к абсолютной конфигурации аминокислот. Принадлежность к L- или D-ряду определяется взаимным расположением аминной и карбоксильной групп и радикала аминокислот. К L-ряду относят те аминокислоты, у которых атом водорода, карбоксильная и аминная группы находятся по отношению друг к другу по часовой стрелке. К D-ряду относят те аминокислоты, у которых атом водорода, карбоксильная и аминная группы находятся против часовой стрелки:
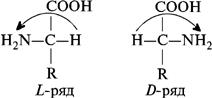
Синтетические аминокислоты являются рацематами, т. е. смесью, состоящей из 50 % L-аминокислот и 50 % D-аминокислот.
Молекулы, имеющие асимметрический атом углерода, способны вращать плоскость поляризованного луча вправо. В этом случае их обозначают знаком (+) или влево — знаком (-). Направление отклонения поляризованного луча зависит от природы растворителя, рН среды и других факторов.
Например: Все встречающиеся в растительных белках аминокислоты принадлежат к L-ряду. D-формы аминокислот не усваиваются организмом человека и животных. D-формы аминокислот встречаются у некоторых антибиотиков.
Изоэлектрическая точка. Аминокислоты представляют собой биполярные ионы (внутренние соли). Под действием электрического тока они мигрируют к катоду или аноду (в зависимости от рН среды). Значение рН среды, при которой устанавливается равенство положительных и отрицательных зарядов, называется изоэлектрической точкой. В изоэлектрической точке аминокислоты электрически нейтральны. Например:
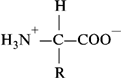
Х и м и ч е с к и е с в о й с т в а
В з а и м о д е й с т в и е с а з о т и с т о й к и с л о т о й
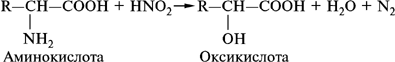
Эту реакцию используют для определения аминокислот по количеству выделившегося газообразного азота (метод Ван — Сляйка).
В з а и м о д е й с т в и е с ф о р м а л ь д е г и д о м. Реакция идет в щелочной среде:
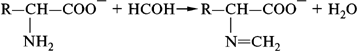
Реакция используется для определения аминокислот. Метод получил название метода формольного титрования, или метода Сёренсена.
Нингидриновая реакция. Нингидрин (трикетогидринден) — специфический реактив на -аминокислоты. По количеству выделившегося СО2 определяют содержание аминокислот. При рН > 5 реакция протекает с образованием соединений сине-фиолетового цвета, который дают аминокислоты, за исключением пролина и оксипролина, которые образуют с нингидрином продукты желтого цвета.
В з а и м о д е й с т в и е с о с п и р т а м и с образованием сложных эфиров.
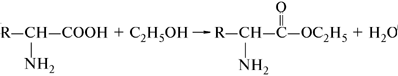
Эта реакция применяется для разделения и определения аминокислот путем фракционной перегонки их эфиров в вакууме.
М е л а н о и д и н о в а я р е а к ц и я. Аминокислоты могут вступать в реакцию с соединениями, содержащими свободную карбонильную группу = С = O. Частный случай этой реакции — взаимодействие аминокислот с восстанавливающими сахарами. В результате образуются продукты желто-коричневого цвета, так называемые меланоидины или сахароамины .
Растения могут синтезировать все аминокислоты, входящие в состав белков. Организм человека и животных не может синтезировать все аминокислоты, необходимые для синтеза белков. Аминокислоты, не синтезируемые организмами человека и животных, но входящие в состав их белков, получили название незаменимых или обязательных аминокислот .
Для человека такими незаменимыми аминокислотами являются 10 аминокислот:
- Валин;
- Треонин;
- Лейцин;
- Изолейцин;
- Метионин;
- Лизин;
- Аргинин;
- Гистидин;
- Фенилаланин;
- Триптофан.
Эти аминокислоты входят в состав белков, но могут также находиться в живых организмах и в свободном состоянии.
Остальные 10 аминокислот (заменимые аминокислоты), входящие в состав белка, могут синтезироваться организмами животных и человека из других соединений, в том числе и из незаменимых аминокислот.
