
ИВЛ - Сатишур
.pdf
18 Часть I. Общие вопросы вентиляции легких
Сопротивление дыхательных путей
Поток дыхательной смеси в легких дол жен преодолеть не только эластическое сопротивление самой ткани, но и резистивное сопротивление дыхательных путей Raw (аббревиатура от английского слова «resistance»). Поскольку трахеобронхиальное дерево представляет собой систему трубок различной длины и ширины, то сопротивление газотоку в легких можно определить по известным физическим законам. В целом сопро тивление потоку R зависит от градиен та давлений в начале и в конце трубки АР, а также величины самого потока V:
АР является своего рода «движущим» давлением, под действием которого и происходит газоток. Поток газа в лег ких может быть ламинарным, турбулен тным и переходным (9).
Для ламинарного потока характерно послойное поступательное движение газа с различной скоростью: скорость пото ка наиболее высока в центре и постепен но снижается к стенкам (рис. 1.21). Ла минарный поток газа преобладает при относительно низких скоростях и опи сывается законом Пуазейля:
где V — скорость потока, АР — градиент давлений, г — радиус трубки (бронха),
ц — вязкость газа, I —длина трубки (бронха).
Преобразуя оба уравнения, получаем:
7ГГ4
Как видно, сопротивление газотоку в наибольшей степени зависит от радиуса трубки (бронхов). Уменьшение радиуса в 2 раза приводит к возрастанию сопротив
ления в 16 раз. В связи с этим понятна важность выбора по возможности наибо лее широкой эндотрахеальной (трахеостомической) трубки и поддержания про ходимости трахеобронгхиального дерева во время ИВЛ. Сопротивление дыхательных путей газотоку значительно увеличивается при бронхоспазме, отеке слизистой обо лочки бронхов, скоплении слизи и вос палительного секрета — по причине су жения просвета бронхиального дерева.
На сопротивление влияют также ско рость потока и длина трубки (бронхов). С увеличением скорости потока (фор сирование вдоха или выдоха) и длины бронхов сопротивление дыхательных путей увеличивается.
Основные причины увеличения сопротивления дыхательных путей:
•бронхоспазм;
•отек слизистой оболочки бронхов (обострение бронхиальной астмы, бронхит, подсвязочный ларингит);

Глава 1. Физиология и патофизиология внешнего дыхания 19
•инородное тело, аспирация, новооб разования;
•скопление мокроты и воспалительно го секрета;
•эмфизема (динамическая компрессия воздухоносных путей).
Турбулентный поток характеризует ся хаотичным движением молекул газа вдоль трубки (бронхов). Он преобладает при высоких объемных скоростях пото ка. В случае турбулентного потока со противление дыхательных путей возра стает, так как при этом оно в еще большей степени зависит от скорости потока и радиуса бронхов. Турбулент ное движение возникает при высоких потоках, резких изменениях скорости потока, в местах изгибов и разветвле ний бронхов, при резком изменении ди аметра бронхов. Вот почему турбулент ный поток характерен для больных ХОЗЛ, когда даже в стадии ремиссии имеет место повышенное сопротивление дыхательных путей. Это же касается больных бронхиальной астмой.
Будет поток ламинарным или турбу лентным, можно определить, рассчитав число Рейнольдса (Re), которое связы вает среднюю скорость потока, плот ность и вязкость газа, а также радиус трубки (бронхов):
где V — средняя скорость потока,
D — плотность газа, г| — вязкость газа.
При Re > 2000 поток будет турбулен тным; при Re < 2000 — поток ламинар ный. Переходный поток характеризует ся «завихрениями», возникающими в местах разветвления трубки (трахеи, бронхов).
Сопротивление воздухоносных путей распределено в легких неравномерно. Наибольшее сопротивление создают бронхи среднего калибра (до 5—7-й ге нерации) (рис. 1.22), так как сопротив ление крупных бронхов невелико из-за их большого диаметра, а мелких брон хов — вследствие значительной суммар ной площади поперечного сечения.
Сопротивление дыхательных путей зависит также от объема легких (см. рис. 1.23). При большом объеме парен хима оказывает большее «растягивающее»
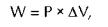
20 Часть I. Общие вопросы вентиляции легких
действие на дыхательные пути, и их со противление уменьшается. Применение ПДКВ (PEEP) способствует увеличению объема легких и, следовательно, сниже нию сопротивления дыхательных путей. Сопротивление дыхательных путей в норме составляет:
•у взрослых — 3—10 мм вод.ст./л/с;
•у детей — 15—20 мм вод.ст./л/с;
•у младенцев до 1 года — 20—30 мм вод.ст./л/с;
•у новорожденных — 30—50 мм вод.ст./л/с.
На выдохе сопротивление дыхатель ных путей на 2—4 мм вод.ст./л/с боль ше, чем на вдохе. Это связано с пассив ным характером выдоха, когда состояние стенки воздухоносных путей в большей мере влияет на газоток, чем при актив ном вдохе. Поэтому для полноценного выдоха требуется в 2—3 раза больше вре мени, чем для вдоха. В норме соотноше ние времени вдох/выдох (I: E) составляет для взрослых около 1 : 1,5. Полноцен ность выдоха у больного во время ИВЛ можно оценить при помощи монито ринга экспираторной временной кон станты (подробнее см. главу 8; стр. 220).
Работа дыхания
Работа дыхания совершается преимуще ственно инспираторными мышцами во время вдоха; выдох почти всегда пасси вен. В то же время в случае, например, острого бронхоспазма или отека слизи стой оболочки дыхательных путей вы дох также становится активным, что значительно увеличивает общую рабо ту внешней вентиляции.
Работу дыхания можно представить как произведение объема и давления:
где W — работа, Р — давление, AV — изменение объема легких (дыхательный объем).
Во время вдоха работа дыхания, в основном, тратится на преодоление эла стического сопротивления легочной ткани и резистивного сопротивления дыхательных путей, при этом около 50 % затраченной энергии накаплива ется в упругих структурах легких. Во время выдоха эта накопленная потенци альная энергия высвобождается, что позволяет преодолевать экспираторное сопротивление дыхательных путей.
Увеличение сопротивления вдоху или выдоху компенсируется дополнительной работой дыхательных мышц. Работа ды хания возрастает при снижении растяжи мости легких (рестриктивная патология), росте сопротивления дыхательных путей (обструктивная патология), тахипноэ (за счет вентиляции мертвого пространства).
На работу дыхательной мускулатуры в норме тратится только 2—3 % от все го потребляемого организмом кислоро да. При патологии (особенно рестриктивной) на работу дыхательных мышц может расходоваться более 30—40 % от всего поглощаемого кислорода. С како го-то момента весь дополнительный кислород, получаемый за счет увеличе ния вентиляции, идет на покрытие со ответствующего прироста работы дыха тельных мышц. Вот почему на определенном этапе существенное уве личение работы дыхания является пря мым показанием к началу ИВЛ (2, 23).
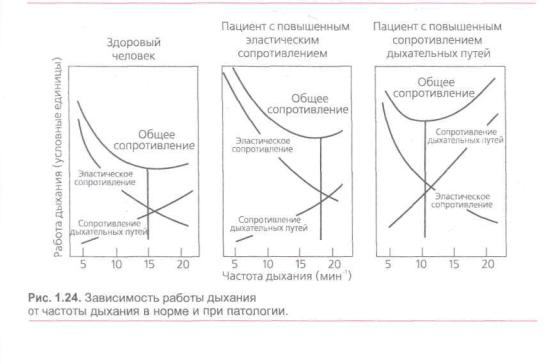
Работа дыхания, которая требуется для преодоления эластического сопротивле ния (податливости легких), возрастает по мере увеличения дыхательного объема. Работа, необходимая для преодоления резистивного сопротивления дыхатель ных путей, возрастает при увеличении частоты дыхания. Пациент стремится уменьшить работу дыхания, меняя час тоту дыхания и дыхательный объем в зависимости от преобладающей патоло гии (рис. 1.24). Для каждой ситуации существует оптимальная частота дыхания и дыхательный объем, при которых ра бота дыхания минимальна. Так, для
Глава 1. Физиология и патофизиология внешнего дыхания 21
больных со сниженной растяжимостью с точки зрения минимизации работы дыхания подходит более частое и повер хностное дыхание (малоподатливые лег кие трудно поддаются расправлению). С другой стороны, при увеличенном сопро тивлении дыхательных путей оптималь но глубокое и медленное дыхание. Это понятно: увеличение дыхательного объе ма позволяет «растянуть», расширить бронхи, уменьшить их сопротивление газотоку; с этой же целью больные с обструктивной патологией во время вы доха сжимают губы, создавая собствен ное «ПДКВ» (PEEP). Медленное и ред кое дыхание способствует удлинению выдоха, что важно для более полного удаления выдыхаемой газовой смеси в условиях повышенного экспираторного сопротивления дыхательных путей.
Диффузия и транспортировка газов
Важной составной частью процесса внеш него дыхания является диффузия основ ных газов (кислорода и углекислого газа):
1.в легких — между альвеолами и ле гочными капиллярами через альвеолокапиллярную мембрану;
2.в тканях — между клетками и пери ферическими капиллярами.
Согласно законам физики, главную роль в процессе диффузии играют гра диент парциальных давлений газа по обе стороны диффузионной мембраны и диффузионная способность газа, кото рая зависит от его физико-химических свойств.
Парциальное давление кислорода и углекислого газа очень неоднородно по всей цепочке их перемещения между атмосферным воздухом и тканями (см. таблицу 1.3).
В процессе продвижения воздуха от атмосферы к альвеолам вследствие ин тенсивного примешивания выдыхаемого углекислого газа и водяных паров пар циальное давление кислорода суще ственно снижается. Тем не менее, раз ница парциальных давлений кислорода между альвеолами и поступающей к легким венозной кровью очень большая (РА02—Pv02 = 60—65 мм рт.ст.). Такой

22 Часть I. Общие вопросы вентиляции легких
градиент очень важен для адекватной и быстрой оксигенации венозной крови, ведь диффузионная способность кисло рода относительно невелика. Диффузия кислорода через альвеолокапиллярную мембрану протекает преимущественно в первую половину времени контакта порции венозной крови с альвеолярным газом, в течение менее 0,4 с (общее вре мя контакта эритроцита с альвеолой со ставляет не более 0,7—0,75 с). Затем в процессе оксигенации градиент РА 02 — Pv02 уменьшается и диффузия кисло рода замедляется. В случае утолщения альвеолокапиллярной мембраны (воспа ление легочной ткани, отек легких кардиогенного или некардиогенного харак тера) диффузия кислорода также нарушается и замедляется. В такой си туации улучшить процесс оксигенации можно в том числе за счет увеличения РА 02 — путем дополнительной ингаля ции кислорода, т. е. за счет повышения Fi02. При этом увеличивается градиент РА02—Pv02, ускоряется диффузия кис лорода, растет Ра02. Вот почему кислородотерапия (Fi02 = 30 % и более) так широко применяется в процессе лечения различных форм дыхательной недоста точности. Приблизительно рассчитать РА 02 можно по простой формуле:
Так, если Fi02 составляет 40 %, то Рд 02 будет приблизительно равно 200 мм рт.ст.
В оксигенированной артериальной крови парциальное давление кислоро да Ра02 составляет 70—100 мм рт.ст. Для определения должной приемлемой вели чины Ра02 предложены различные фор мулы, например:
Ра02 = 1 1 0 - возраст/3, Ра02 = 100 - возраст/2 и другие
Уровень Ра02 очень важен, ведь впоследствии для оксигенации тканей необходим определенный градиент между парциальным напряжением кислорода артериальной капиллярной крови и парциальным напряжением кислорода тканей (Pa02 —Pt02 ). При снижении Ра02 менее 70 мм рт.ст. и особенно менее 60 мм рт.ст. процесс диффузии кислорода в ткани наруша ется. Ткани пытаются компенсировать снижение Ра02 путем увеличения ко эффициента экстракции кислорода из капиллярной крови, что проявляется снижением Pv02 ниже 30—35 мм рт.ст. До определенного момента такой ком пенсаторный механизм эффективен. В случае же снижения Ра02 менее 50 мм рт.ст., особенно у пациентов с сопут ствующими циркуляторными наруше ниями, тканевая гипоксия может при нять необратимый характер, и для ее коррекции необходимо предприни мать срочные меры.
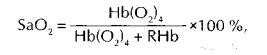
Глава 1. Физиология и патофизиология внешнего дыхания 23
Альвеолярно-артериальная разница по кислороду Р(А—а)07
В норме альвеолярно-артериальная раз ница по кислороду D(A—а)02 (РА 02 — Ра02) составляет 9—15 мм рт.ст. При дыхательной недостаточности разность РА02—Ра02 увеличивается более чем на 20—30 мм рт.ст. Эта разность характе ризует степень тяжести дыхательной не достаточности и гипоксии. Градиент РА0,—Ра02 зависит, в основном, от сте пени шунтирования венозной крови справа налево, от нарушения вентиля- ционно-перфузионных соотношений и напряжения кислорода в смешанной ве нозной крови. В свою очередь, Pv02 за висит от сердечного выброса, потребле ния кислорода и содержания гемоглобина, т. е. уменьшается при сни жении сердечного выброса, снижении содержания гемоглобина и при увели чении потребления кислорода.
В наибольшей степени градиент РА02—Ра02 зависит от шунтирования венозной крови (классический пример — блокада альвеол при ОРДС). На опреде ленной стадии патологического процес са (шунтирование > 30—35 %) увеличе ние Fi02 уже не приводит к заметному повышению Ра02, что сопровождается существенным ростом градиента РА02— Ра02 (> 100—200 мм рт.ст.). Например, при ОРДС исследование газов крови показывает Ра02 = 60 мм рт.ст. при Fi02 = 50 %. Отсюда РА 02 = 50 х 5 = 250 мм рт.ст. Градиент РА 02 —Ра02 = 250—60 = 190 мм рт.ст. свидетельствует о значи тельном венозном шунтировании и тя желой дыхательной недостаточности.
После поступления в сосудистое рус ло кислород проникает в эритроциты и транспортируется в виде оксигемоглобина. Кислородная емкость крови (КЕК) напрямую зависит от содержания гемог лобина, каждый грамм которого спосо бен связать максимально 1,34 мл 02:
КЕК = НЬх1,34
Например, у здорового человека при уровне НЬ = 150 г/л кислородная ем кость крови составляет около 200 мл 02/л крови.
Одна молекула гемоглобина способ на присоединять к себе четыре молеку лы кислорода:
Hb + 402 = Hb(02)4
Ключевым фактором, определяющим количество кислорода, связанного с ге моглобином, является показатель степе ни насыщения кислородом гемоглобина артериальной крови (Sa02). Показатель Sa02 довольно точно отражает отноше ние между оксигемоглобином и КЕК. Иными словами, Sa02 является отноше нием оксигемоглобина ко всему гемог лобину, потенциально способному пере носить кислород:
где RHb — так называемый «редуцированный» гемоглобин, который по каким-либо причинам не связан с кислородом, хотя готов к его транспорту. Гемоглобин, не способный к переносу кислорода (НЬСО, MetHb), в данном случае в расчет не принимается.
Уровень Sa02 является интегральным показателем газообмена и транспорта кислорода и довольно точно отражает степень дыхательной недостаточности различного генеза. SaO, легко опреде ляется и мониторируется неиивазивным способом (методом пульсоксиметрии) и в норме составляет у взрослых 96—98 %.
Взаимоотношение между РаО, и Sa02 определяется по кривой диссоциации оксигемоглобина (подробнее см. главу 12). По достижении Ра02 показателя 100 мм рт.ст. гемоглобин почти полностью насыщен кислородом (Sa02 98—99 %). Дальнейший рост Ра02 более 100 мм рт.ст. приводит только к увеличению

24 Часть I. Общие вопросы вентиляции легких
количества растворенного в крови кис лорода, так как весь гемоглобин, спо собный нести кислород, уже насыщен.
Уровень Ра02, при котором Sa02 ра вен 50 %, известен как показатель Р50. Это общепринятая мера оценки срод ства гемоглобина к кислороду; в норме она составляет 26—28 мм рт.ст. Сниже ние Р50 отражает увеличение сродства НЬ к (52, и наоборот.
Сродство гемоглобина к кислороду меняется в зависимости от метаболичес ких условий, влияющих на процесс свя зывания кислорода гемоглобином (под робнее см. главу 13; стр. 311).
Транспорт и диффузия СО2_
Образовавшийся в процессе тканевого метаболизма С02 легко диффундирует в кровь. Диффузионная способность С02 в 20 раз превышает таковую у кис лорода. Углекислый газ транспортиру ется к легким в трех основных формах:
1. В виде растворенного С02 |
|
2. В |
виде аниона бикарбоната: |
со2 |
+ н2 о -+ н2 со3 - н+ + нсо3 ~ |
Анион бикарбоната представляет собой самую большую фракцию С02 в крови.
3. В виде карбаминовых соединений
С0 2 с |
аминогруппами белков: |
R-NH2 |
+ С02 RNH - CO - + Н+ |
Доставленный к легким С02 легко диф фундирует в альвеолы и удаляется че
рез дыхательные пути. Градиент парци альных давлений С0 2 в легочных капиллярах (соответствует PvC02) и альвеолах (РАС02) невелик — не превы шает 5—6 мм рт.ст., однако С02 элими нируется благодаря своей высокой диф фузионной способности. Поэтому патологический рост С02 в крови отме чается только при выраженных венти- ляционно-перфузионных нарушениях (например, при длительном течении ХОЗЛ), а также при выраженной аль веолярной гиповентиляции (например,
при резком снижении минутного объе ма вентиляции в случае угнетения ды хательного центра).
Кислородный резерв
Запасы кислорода в организме весьма ограничены. Теоретически кислородный резерв у взрослого человека в среднем составляет 1500 мл. Он включает в себя кислород в легких, кислород в виде оксигемоглобина и кислород в раство ренном виде. Основным источником кислородного резерва является дыха тельная смесь, находящаяся в легких — функциональная остаточная емкость (ФОБ). Если дополнительное поступле ние кислорода отсутствует (апноэ, от ключение от аппарата ИВЛ и т.д.), то при предшествующем дыхании атмос ферным воздухом (FiO, = 21 %) и объе ме ФОЕ, равном 2300 мл, доступное резервное количество кислорода соста вит:
Fi02 х ФОЕ = 0,21 х 2300 = 480 мл.
Так как потребление кислорода до вольно высоко (3—4 мл/кг/мин), остав шийся в легких и крови кислород бы стро утилизируется, и уже через 2—3 минуты наступает тяжелая гипоксия. Развитие гипоксемии можно отсрочить, если перед прекращением вентиляции в течение 2—3 минут насытить организм 100 % кислородом. После дыхания чи стым кислородом легкие содержат уже около 2 л кислорода, что задерживает развитие гипоксемии после апноэ на 4— 5 минут. Данная концепция лежит в основе метода преоксигенации, приме няющегося перед вынужденным прекра щением вентиляции на некоторое вре мя (временное отключение пациента от аппарата ИВЛ при санации ТБД, брон хоскопии, перестилании, переинтуба ции и т. д.).
Глава 2
Острая дыхательная недостаточность
Классификация и патофизиология ОДН |
26 |
Основные внелегочные причины ОДН |
30 |
Основные клинические и лабораторные признаки ОДН |
31 |
Показания к ИВЛ (МВЛ) |
33 |
26 Часть I. Общие вопросы вентиляции легких
Общепринятого определения понятия «острая дыхательная недостаточность» (ОДН) до сих пор не существует, хотя и серьезных разногласий между специ алистами в понимании самой сути это го синдрома также не наблюдается. В
основе ОДН лежит остро развивающее ся несоответствие уровня газообмена (внешнего дыхания) метаболическим по требностям организма (9, 11, 23).
ОДН не обязательно проявляется се рьезными изменениями газового состава крови (гипоксемией и/или гиперкапнией), как отмечается в ряде определений. Некоторое время относительно «нор мальный» газовый состав поддержива ется за счет напряженной работы сис темы внешнего дыхания, в частности дыхательных мышц. Понимание данно го факта очень важно. Оно позволяет своевременно начать интенсивную рес пираторную терапию (например, МВЛ), не дожидаясь истощения компенсатор ных механизмов внешней вентиляции, истощения дыхательных мышц.
Классификация
ипатофизиология ОДН
Кнастоящему времени в литературе пред ложено много различных классификаций ОДН. Все они весьма справедливы и имеют право на существование; между отдельными классификациями и класси фикационными группами значимых от личий не отмечается. Хотя универсальной классификации ОДН не существует, не обходимость в академическом классифи цировании ОДН остается. Это помогает понять суть различных видов ОДН, их патофизиологическую основу. Из пони мания этиопатогенеза логически вытека ют основные принципы патогенетической интенсивной терапии того или иного вида ОДН. В связи с этим нам представляет ся целесообразным разделить виды ОДН именно по этиопатогенетическому прин
ципу и привести классификацию, моди фицированную автором на основании данных различных литературных источ ников (9, 11, 12, 13, 15, 23, 54, 187).
Центральная ОДН
Связана с угнетением, возбуждением либо дискоординацией работы дыха тельного центра:
•Угнетение дыхательного центра в ре зультате действия лекарственных пре паратов (опиоиды, снотворные, седативные и т. д.); нарушение мозгового кровообращения, тяжелая черепномозговая травма, острые нейроинфекции, опухоли головного мозга, по вреждение ствола головного мозга. Для тяжелой центральной ОДН, свя занной с угнетением дыхательного центра, характерна клиническая три ада: нарушение сознания, брадипноэ, тенденция к поверхностному дыха нию и апноэ.
•Перевозбуждение дыхательного цент ра (энцефалопатическая гипервенти ляция) может развиться в результате черепно-мозговой травмы, отека моз га, повреждения гипоталамуса, хро нической нейроинфекции и т. д. Эн цефалопатическая гипервентиляция приводит к чрезмерной работе дыха тельных мышц, вызывает их истоще ние, дыхательный алкалоз, гипокапнию и т. д.
•Дискоординация дыхательного центра
вызывает патологические ритмы ды хания и чаще всего является след ствием вторичного метаболического поражения головного мозга. В каче стве примеров можно назвать диабе тические комы, энцефалопатию при эндогенной интоксикации (почечной или печеночной недостаточности) и т.д.
С точки зрения клинической значимо сти именно угнетение системы цент ральной регуляции дыхания является классическим примером центральной
Глава 2.
ОДЫ. Быстро развивающаяся альвео лярная гиповентиляция приводит к выраженной гипоксемии и реально уг рожает жизни, если не предпринять срочных мер интенсивной терапии (ИВЛ). Поэтому, говоря о центральном характере ОДН, в основном понимают именно угнетение дыхательного центра.
Расстройства центральной регуляции дыхания в клинической практике почти никогда не бывают изолированными. К ним, как правило, присоединяются на рушения проходимости верхних дыха тельных путей (западение корня языка, скопление мокроты из-за угнетения кашлевого рефлекса), аспирация и т. д.
Нейромышечная ОДН
Связана с нарушением передачи нервно го импульса от дыхательного центра к респираторным мышцам либо с соб ственно патологией дыхательных мышц:
•Патология проведения импульса по нейропроводящей системе. Возникает при травмах и заболеваниях спинно го мозга (особенно шейного отдела)
иотводящих нервов: травматическом пересечении, опухолях, ишемизации, воспалении бактериально-вирусной природы, боковом амиотрофическом склерозе. То же относится к перифе рическим отводящим нервам, связан ным с дыхательными мышцами — травмы, демиелинизация, полиомие лит, полинейропатия (синдром Гий- ена—Барре). Особое место занимает повреждение п. phrenicus, иннервирующего диафрагму: развивающаяся вторичная слабость диафрагмы, как основной дыхательной мышцы, вы зывает прогрессирующую нейромышечную ОДН.
•Патология проведения импульса в нейромышечном соединении (синапсе). Развивается при аутоиммунном по вреждении синаптического медиаторного проведения (миастения), инток- сикационно-токсическом поражении
я дыхательная недостаточность |
27 |
синапса и медиаторов (ботулизм, столбняк, отравление ФОС) или его медикаментозном угнетении (миорелаксанты).
•Патология сократимости дыхательных мышц. Самые различные причины способны привести к слабости соб ственно дыхательных мышц. К ним относятся различные неспецифичес кие миопатии, миодистрофия, коллагенозы, общее истощение (кахексия). Тяжелые водно-электролитные нару шения (особенно гипокалиемия и гипомагниемия) также способствуют развитию слабости дыхательных мышц. Отдельно стоит отметить ат рофию дыхательных мышц, развива ющуюся при длительной ИВЛ в слу чае применения глубокой седации и/ или миорелаксантов, что значитель но затрудняет последующее «отучение» от ИВЛ. Истощение дыхатель ных мышц вследствие большой работы дыхания также на определен
ном этапе усугубляет течение ОДН. Центральную и нейромышечную ОДН еще принято относить к так называемой
вентиляционной, или гипоксически-гипер- капнической дыхательной недостаточно сти. Этим самым подчеркивается нару шение самого механического процесса внешней вентиляции. При этих формах быстро развивается выраженная альвео лярная гиповентиляция, резко снижается минутный объем дыхания, поэтому гипоксемия и гиперкапния прогрессируют одновременно, что характерно именно для вентиляционной ОДН. Выраженная вентиляционная ОДН является прямым показанием к экстренной ИВЛ (!) еще до выяснения причин ОДН и начала спе цифической терапии (если исключен на пряженный пневмоторакс).
Торакодиафрагмальная ОДН
Связана с нарушением целостности кар каса грудной клетки, повреждением диафрагмы, острым нарушением распре-
