
- •Лабораторные работы
- •1.3.2. Оформление лабораторного отчета и расчет результата
- •1.4. Контрольные вопросы
- •Лабораторная работа №2 Приготовление раствора гидроксида натрия заданной концентрации. Определение концентрации гидроксида натрия титрованием. Определение общей жесткости воды
- •Опыт 1. Приготовление раствора гидроксида натрия заданной концентрации.
- •Опыт 2. Определение концентрации гидроксида натрия методом кислотно-основного титрования
- •Контрольные вопросы
- •Лабораторная работа № 3. Закономерности химических процессов
- •3. Контрольные вопросы для защиты работы
- •Лабораторная работа №4
- •1. Исследование зависимости скорости протекания реакции от концентрации реагента
- •2. Исследование зависимости скорости химической реакции от температуры .
- •3. Смещение равновесия обратимой реакции
- •4. Контрольные вопросы для защиты работы
- •Лабораторная работа №5 диссоциация электролитов
- •1. Смещение равновесия диссоциации слабых электролитов
- •2. Характер диссоциации гидроксидов элементов (опыт 6.2.2)
- •3.Реакции ионного обмена
- •Окислительно-восстановительные реакции
- •Влияние среды на характер овр
- •Направление протекания овр
- •Лабораторная работа №7 электрохимические процессы
- •1. Электродные потенциалы и гальванические элементы
- •Опыт 1. Изготовление и изучение работы медно-цинкового гальванического элемента
- •Опыт 2. Изготовление и изучение работы свинцового аккумулятора
- •Контрольные вопросы
- •Лабораторная работа №8 «Электрохимические процессы» Электрохимическая коррозия металлов
- •Опыт 1. Электрохимическая коррозия при образовании гальванических пар
- •Опыт 2. Электролиз растворов солей
- •Контрольные вопросы
- •Библиографический список
- •Приложение
1.4. Контрольные вопросы
1. Чьи идеи лежат в основе атомно-молекулярного учения? В чем их суть? Что является основным принципом атомно-молекулярного учения?
2. Назовите основные положения атомно-молекулярного учения.
3. Перечислите основные количественные законы химии.
4. Сформулируйте закон эквивалентов, закон кратных отношений.
5. Что такое эквивалент, фактор эквивалентности?
6. Как рассчитать молярную массу эквивалентов оксида, кислоты, гидроксида металла, соли (нормальной, основной и кислой)?
7. Сформулируйте закон Авогадро.
8. Какое следствие из закона Авогадро используют в расчете результата данной работы?
Лабораторная работа №2 Приготовление раствора гидроксида натрия заданной концентрации. Определение концентрации гидроксида натрия титрованием. Определение общей жесткости воды
Цель работы:
1. Приготовить раствор гидроксида натрия заданной концентрации.
2. Определить концентрацию методом кислотно-основного титрования.
2. Определить общую жесткость водопроводной воды.
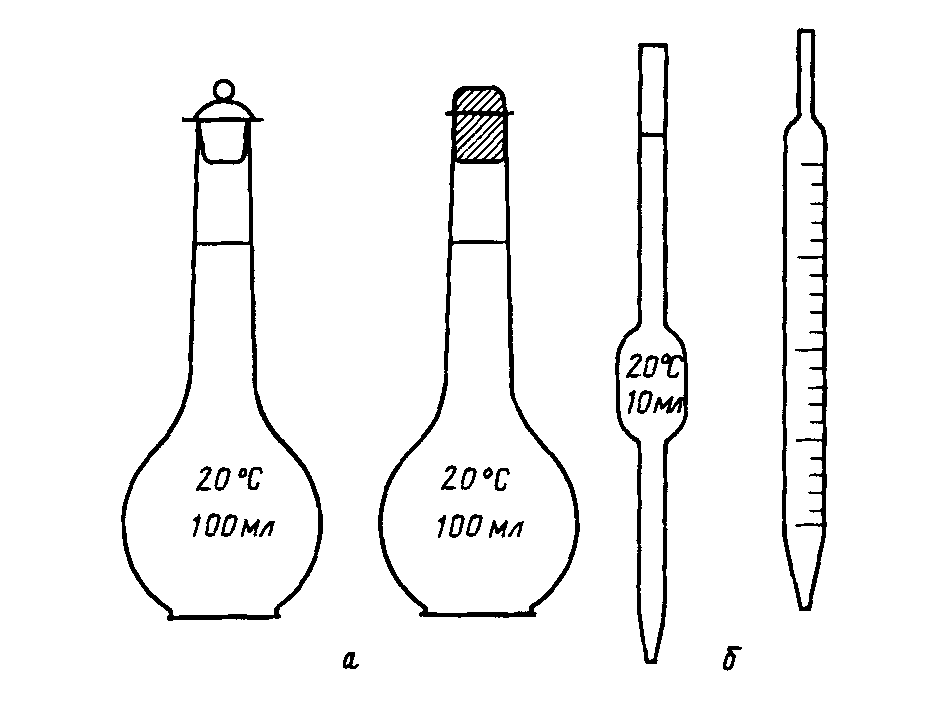

Рис. 2. Мерные колбы (а), пипетки (б), мерный цилиндр (в), мензурка (г)
Опыт 1. Приготовление раствора гидроксида натрия заданной концентрации.
Реактивы и оборудование.РастворNaOHС% = 5,0% (= 1,05 г/см3); пипетка с делениями на 10 см3; мерная колба на 100 см3.
Выполнение работы. Приготовить 100 см3раствораNaOHс заданной концентрацией (задание получить у преподавателя), из имеющегося раствора С% = 5,0% (= 1,05 г/см3).
Рассчитать какой объем концентрированного раствора нужно взять для приготовления 100 см3заданного раствора (см. Пример 4). Например, если дано задание приготовить 0,125 н раствор, то необходимо взять 9,52 см35% раствораNaOH.
В мерную колбу вместимостью 100 см3градуированной пипеткой на 10 см3(или из бюретки) пользуясь техникой, описанной в разделе 3, отмерить рассчитанный объем 5% раствораNaOH. Затем, добавляя дистиллированную воду, довести уровень жидкости до метки. Плотно закрыть колбу пробкой и перемешать раствор, переворачивая колбу дном вверх 10 – 15 раз.
Запись данных опыта и расчеты. Данные записать по приведенной ниже форме.
Массовая доля NaOHв исходном растворе, С% = …
Плотность исходного раствора, = …
Заданная молярная концентрация NaOHв растворе, СМ(NaOH) = …
Объем мерной колбы, V= …
Расчет объема исходного раствора:
Объем исходного раствора, V(р-р) = …
Опыт 2. Определение концентрации гидроксида натрия методом кислотно-основного титрования
Метод кислотно-основного титрования основан на реакциях кислотно-основного взаимодействия, которое в общем виде можно представить как
![]() ,
,
где НА – кислота; В – основание; НВ+- сопряженная кислота; В–– сопряженное основание.
В результате взаимодействия растворов сильных кислот и оснований раствор становится нейтральным, поэтому метод кислотно-основного титрования иногда называют методом нейтрализации.
В данной лабораторной работе используем титрование сильного основания сильной кислотой в соответствие с уравнением реакциии
2NaOH+H2SO4=Na2SO4+ 2Н2О.
Реактивы и оборудование. Титрант – стандартный растворH2SO4cконцентрациейC[1/2(H2SO4)] = 0,10 н; коническая колба для титрования объемом 250 см3; пипетка на 10,00 см3; бюретка объемом 25 см3; кислотно-основной индикатор метиловый оранжевый 1% раствор.
Выполнение работы.
Подготовка бюретки к титрованию.
Чистую бюретку, закрепленную в лапке лабораторного штатива, ополаскивают 2 – 3 раза раствором титранта, для чего через воронку наливают его каждый раз по 5 – 7 см3в бюретку и выливают через запорное устройство в коническую колбу или стакан.
Затем наливают в бюретку через воронку раствор титранта до уровня на 2 – 3 см выше отметки «0» и заполняют им носик бюретки.
После этого вынимают из бюретки воронку и выпускают через затвор по каплям титрант в посуду для слива до тех пор, пока нижний край мениска раствора не коснется нулевой отметки бюретки (глаза должны быть на уровне отметки).
Приготовление пробы для титрования:
Раствор NaOHиз мерной колбы переливают в чистый сухой химический стакан, пипеткой объемом 10,00 см3отбирают аликвотный объем раствора гидроксида натрия и переносят его в коническую колбу для титрования. Стенки колбы обмывают небольшим количеством дистиллированной воды, добавляют 2 капли индикатора метилового оранжевого и начинают титрование.
Титрование:
Коническую колбу с аликвотной частью титруемого раствора подставляют под носик бюретки и приподнимают за горло так, чтобы конец носика находился в конической части колбы. Кончиками большого и указательного пальцев другой руки, надавливая на запорный стеклянный шарик, приливают раствор титранта в колбу, регулируя скорость приливания силой давления пальцев на шарик.
Прекращают приливать раствор титранта в момент, указанный в методике. Во время титрования раствор в колбе непрерывно перемешивают легким круговым движением колбы.
Расход титранта отсчитывают по нижнему краю мениска титранта в бюретке, определяя на глаз сотые доли миллилитра. Последние порции кислоты приливать по каплям. Титрование останавливают в тот момент, когда произойдет резкий переход окраски от желтой к оранжево-красной. Записывают объем раствора кислоты, пошедший на титрование. Повторяют титрование еще 3 раза. Перед каждым титрованием коническую колбу моют и ополаскивают дистиллированной водой.
Результат титрования записывают в рабочий журнал. Параллельно титруют 4 – 5 проб и находят средний расход титранта, при этом разность любых двух титрований не должна превышать 0,2 см3.
Перед каждым титрованием, необходимо заполнять бюретку раствором титранта до нулевой отметки.
Запись данных опыта и расчеты. Данные записать по приведенной ниже форме.
Объем мерной колбы V= 100,00 см3
Концентрация титранта Cн[1/2(H2SO4)] = 0,10 н
Индикатор – метиловый оранжевый
|
№ п/п |
Объем аликвоты V(NaOH), см3 |
Эквивалентный объем титранта V(H2SO4), см3 |
|
1 |
|
|
|
2 |
|
|
|
3 |
|
|
|
Ср.значение |
|
|
По результатам
титрования найти средний объем титранта
![]() =
=
Рассчитать эквивалентную концентрацию NaOH. На основании закона эквивалентов
![]()
рассчитывают эквивалентную концентрацию гидроксида натрия
![]()
