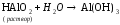- •Методы разложения алюминатных растворов
- •Разложение алюминатного раствора методом выкручивания (декомпозиция)
- •Факторы, влияющие на процесс декомпозиции
- •Устройство и принцип действия декомпозера
- •Карбонизация алюминатных растворов.
- •Влияние различных факторов на карбонизацию
- •Способы карбонизации
- •Устройство и принцип действия карбонизатора
- •Контрольные вопросы:
Устройство и принцип действия декомпозера
Для разложения алюминатного раствора используются декомпозеры двух видов: с воздушным перемешиванием и с механическим перемешиванием.
Декомпозер представляет собой стальной цилиндрический сосуд большой высоты с коническим, сферическим или плоским днищем. Во внутреннем пространстве декомпозера размещены один или два аэролифта.
В
аппарате с воздушным перемешиванием –
два аэролифта: транспортный и
циркуляционный.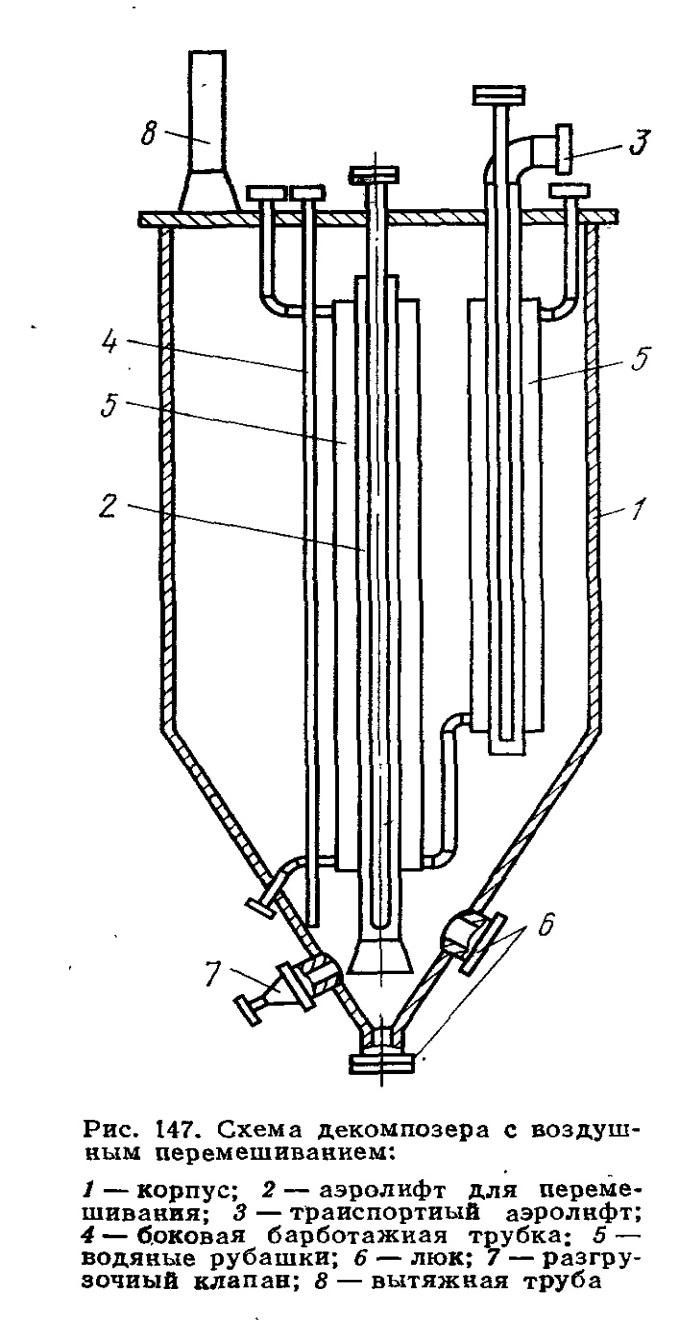
Рис 147. Декомпозер с воздушным перемешиванием.
Он представляет собой стальной бак с коническим дном. Для циркуляции затравки в таком декомпозере служит аэролифт, состоящий из двух труб, вставленных одна в другую. По внутренней трубе в коническую часть декомпозера, где оседающая гидроокись алюминия стекает к вершине конуса, подается сжатый воздух, который, выходя из трубы, образует воздушно-пульповую смесь, которая обладает значительно меньшей плотностью, устремляется в кольцевой зазор аэролифта и, поднимаясь сливается через верхний открытый конец наружной трубы. С помощью транспортного аэролифта осуществляется переток пульпы из одного декомпозера в другой.
В непрерывно работающей серии декомпозеров работают 16 - 28 аппаратов.
Рис 2. Декомпозер с механическим перемешиванием.
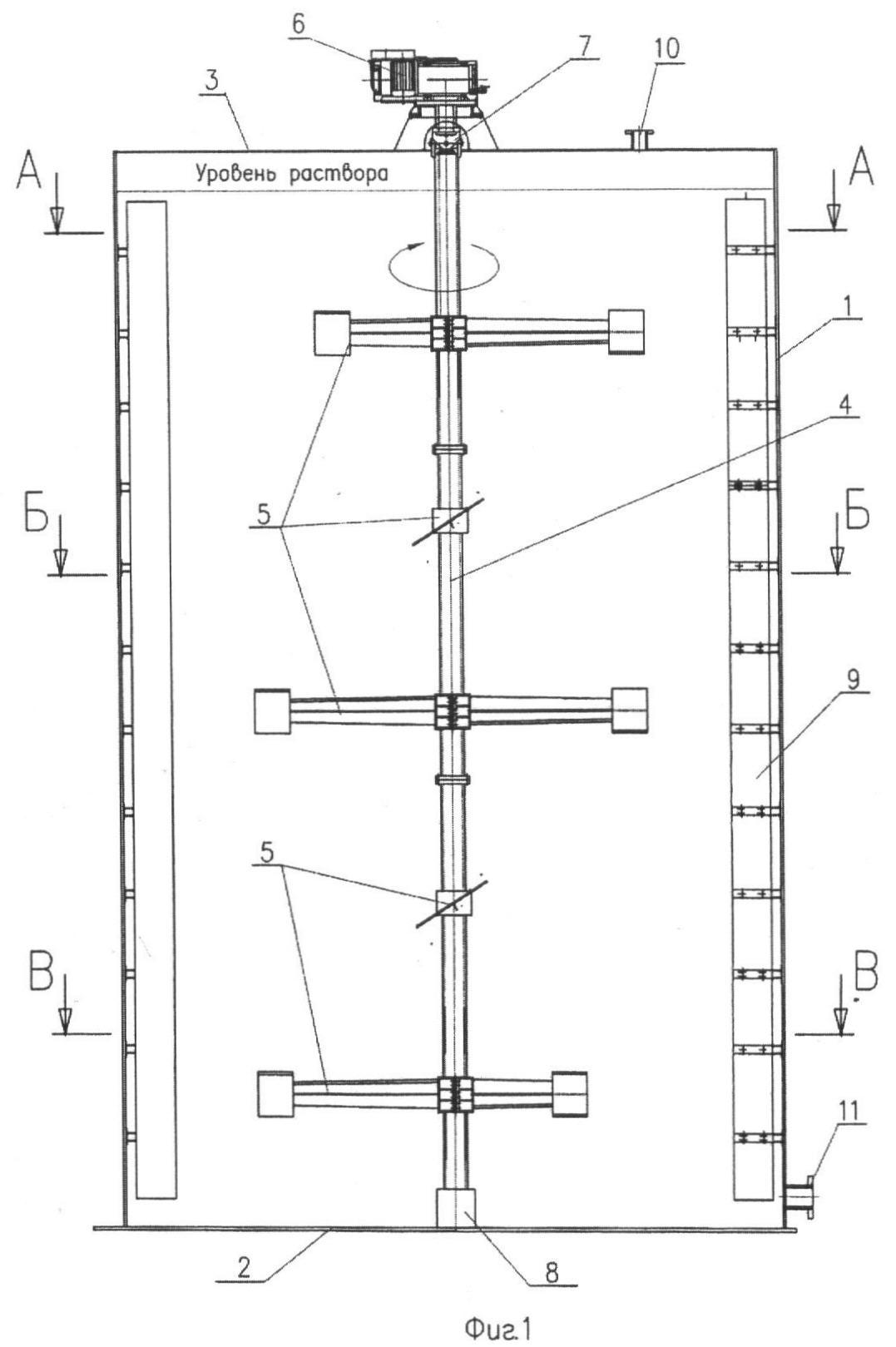
В аппарате с механическим перемешиванием – один транспортный аэролифт.
Он включает в себя цилиндрический корпус 1 с плоским днищем 2 и крышкой 3, многоярусное перемешивающее устройство, установленное по оси корпуса с приводом, размещенным на крышке, патрубки для подачи суспензии 10 и ее отбора 11, вертикальные перегородки 9, установленные радиально и закрепленные на внутренней поверхности корпуса. Перемешивающее устройство состоит из вертикального вала 4, на котором в несколько ярусов закреплены лопасти 5.
Карбонизация алюминатных растворов.
Карбонизация - обработка алюминатного раствора газами, содержащими двуокись углерода.
При насыщении углекислым газом алюминатного раствора из него, как известно, выпадает Al(OH)3. Причину этого многие видят в усреднении едкой щелочи:
2NaOH + CO2 = Na2CO3 + H2O.
При уменьшении каустического модуля алюминатный раствор становится не стойким и разлагается, как при выкручивании:
NaAlO2 + 2H2O Al(OH)3 + NaOH.
Существуют несколько мнений, отражающих суть процесса карбонизации:
По Мазелю, в конце карбонизации растворенный алюминат непосредственно взаимодействует с углекислым газом:
2NaAlO2 + CO2 + 3H2O = 2Al(OH)3 + Na2CO3.
По Лилееву, углекислый газ, растворяясь, образует углекислоту, которая действует одновременно на растворенные едкую щелочь и алюминат:
2NaOH + H2CO3 + H2O = Na2CO3 + H2O;
2NaAlO2 + H2CO3 + H2O = 2Al(OH)3 + Na2CO3 + H2O.
Реакция сопровождается образованием изотропной гидроокиси алюминия, условно обозначенной через Al(OH)3. Она обычно выделяется при подкислении алюминатного раствора. Изотропная гидроокись, весьма активная в момент выделения, вступает во взаимодействие со свободной едкой щелочью и снова растворяется:
Al(OH)3 (изотр) + NaOH + H2O NaAlO2 + H2O.
Поэтому при пропускании СО2 гидроокись сначала не выделяется, а лишь уменьшается концентрация Na2OК и увеличивается концентрация Na2Oу. Это приводит к гидролизу алюмината, в результате которого накапливается алюминиевая кислота:
NaAlO2 + H2O NaOH + НAlO2 + H2O.
Затем наступает кристаллизация гидроокиси алюминия:
В
заводских карбонизаторах каустическое
отношение поддерживается обычно на
уровне 1,5, но выделение гидроокиси
алюминия идет даже при
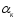 =
1,7. Лишь в конце карбонизации, когда в
растворе остается всего 3-4 г/лAl2O3,
каустическое отношение быстро убывает
до величины, меньшей единицы.
=
1,7. Лишь в конце карбонизации, когда в
растворе остается всего 3-4 г/лAl2O3,
каустическое отношение быстро убывает
до величины, меньшей единицы.