
Надпочечники_Kardio_2013_01_048
.pdf
АРТЕРИАЛЬНАЯ ГИПЕРТЕНЗИЯ
Некоторые вопросы клиники, диагностики и хирургического лечения новообразований надпочечников
Чл.-корр. АМН МЗ Республики Таджикистан, д.м.м., проф. А.Д. ГАИБОВ, д.м.м., проф. Ш.С. АНВАРОВА, А.Х. ТУРАКУЛОВ, О.Н. САДРИЕВ
Several questions of clinical presentation, diagnostics and surgical treatment of adrenal tumors
A.D. GAIBOV, SH.S. ANVAROVA, A.KH. TURAKULOV , O.N. SADRIEV
Кафедра хирургических болезней №2, кафедра эндокринологии Таджикского государственного медицинского университета
им. Абуали ибни Сино, Душанбе, Республика Таджикистан
Проанализированы результаты лечения 43 больных с различными новообразованиями надпочечников. Определены необходимый объем диагностических мероприятий и хирургического лечения патологии надпочечников в зависимости от характера и размеров опухоли. Выбор оперативного доступа при хирургическом лечении больных с опухолями надпочечника зависел от размера новообразования. При образованиях размером меньше 5 см авторы отдают предпочтение миниинвазивным доступам без вскрытия плевральной полости, для удаления более массивных опухолей оптимальным считают тораколюмботомные доступы. Все больные, за исключением одного, выписаны с хорошими непосредственными результатами. Умер один больной с двусторонней гигантской феохромоцитомой накануне второго этапа операции. С учетом топографо-анатомических особенностей авторами обоснована необходимость выполнения подобных операций в специализированных сосудистых центрах.
Ключевые слова: опухоли надпочечников, симптоматическая артериальная гипертензия, хирургическое лечение, адреналэктомия, феохромоцитома.
Results of treatment were analyzed in 43 patients with various types of adrenal malignancy. Amount of diagnostic procedures and surgical tactics for treatment of adrenal pathology were determined depending on type and size of tumor. All patients were operated, 1 patient with bilateral pheochromocytoma died from acute cardiovascular failure. Selection of surgical approach for adrenal neoplasm depended on its size. Authors prioritize mini-invasive approach for tumors lesser than 5 cm, while thoracolumbotomy is suggested optimal for more solid tumors. Authors justify that these operations must be carried out in specialized vascular centers taking into account topographic and anatomic specifics.
Key words: adrenal tumors, symptomatic arterial hypertension, surgical treatment, adrenalectomy, pheochromocytoma.
За последние два десятилетия значительно возрос интерес хирургов к опухолям надпочечников. Это связано со значительным увеличением числа больных с заболеваниями надпочечников, совершенствованием высококачественных методов визуализации и лабораторных методов диагностики, позволяющих среди большого числа больных с артериальной гипертензией (АГ) выявить ее надпочечниковую форму [2, 5, 13].
По данным ряда авторов [5], частота развития опухоли надпочечников составляет от 1—5 на 10 000 до 1 на 200 000 населения. Эти цифры существенно меняются при изучении распространенности новообразований надпочечников у лиц, страдающих АГ. Наиболее часто опухоли надпочечников встречаются в возрасте 20— 50 лет [2, 5], хотя описаны случаи, когда они встречались в более раннем возрасте [5]. В 80—85% наблюдений опухоли располагаются в одном из надпочечников, чаще в правом [2, 5]. Примерно в 10% случаев выявляют злокачественную опухоль, способную метастазировать в поджелудочную железу, регионарные лимфатические узлы, щитовидную железу, в кости, мышцы и брюшину [5, 10, 14, 15, 19, 24].
Согласно данным ряда авторов [1—3], симптоматическая АГ, вызванная новообразованиями надпочечников, достигает 2,6% случаев от общего числа заболеваний АГ. Как отмечают большинство исследователей [1, 2, 4], лечение гипертонических кризов, вызванных гормональными опухолями надпочечников, является сложным, в связи с чем в ряде случаев допускаются серьезные диагностические и тактические ошибки. Так, по данным Y. Katsube и соавт. [17], кризы при феохромоцитоме могут сопровождаться геморрагическим инсультом, отеком легких, острой сердечной недостаточностью, инфарктом миокарда, расслоением аорты и другими угрожающими жизни состояниями.
В настоящее время основным методом лечения АГ надпочечниковой этиологии считается хирургический [2, 4, 6, 8, 19]. Наличие новообразования надпочечника служит прямым показанием к хирургическому лечению. Противопоказаниями к операции являются злокачественные опухоли с множественными отдаленными метастазами и тяжелые сопутствующие заболевания, при которых противопоказано любое хирургическое вмешательство [24]. Цель предоперационной подготовки у данной
© Коллектив авторов, 2013 |
e-mail: Gaibov_A.D@mail.ru |
48 |
1, 2013 |

категории больных состоит в поддержании нормального уровня артериального давления (АД) в течение 2—3 нед до операции и устранении последствий повышенного содержания катехоламинов в крови. Препаратами выбора являются α-адреноблокаторы, среди которых предпочтение отдается феноксибензамину.
В последние годы описано более 60 хирургических доступов к надпочечникам, каждый из которых имеет свои преимущества и недостатки [2]. При больших опухолях надпочечников (более 5 см) применяют торакофренолюмботомию в девятом—десятом межреберье. При размерах опухоли менее 5 см методом выбора является минилюмботомия. Вместе с тем до настоящего времени нет строго определенных показаний к выбору того или иного доступа. В конце ХХ века появился новый метод хирургического лечения новообразований надпочечников — лапароскопическая адреналэктомия [22, 23, 25]. Существует несколько вариантов эндовидеохирургических доступов к надпочечникам: ретроперитонеальный, трансторакальный и трансабдоминальный. Несмотря на преимущество лапароскопической адреналэктомии, существуют некоторые ограничения к ее применению: отсутствие признаков злокачественного роста, размер опухоли надпочечника не более 5 см, глубина расположения надпочечника не более 10 см. Кроме феохромоцитомы нередко встречаются гор- монально-активная опухоль коры надпочечника, продуцирующая избыточное количество андрогенов (андростерома), кортикоэстерома, вырабатывающая эстрогены и приводящая к феминизации, и болезнь, и синдром Ицен- ко—Кушинга, возникаюшие вследствие гиперкортицизма на почве гиперплазии или аденомы надпочечников [7, 8, 10, 16, 21].
Материал и методы
В период с 2000 по 2012 г. в Республиканском научном центре сердечно-сосудистой хирургии, являющемся базой кафедры хирургической болезни №2, хирургическое лечение осуществлено у 43 больных (17 мужчин, 26 женщин, в возрасте 17—71 года, средний возраст 24±0,5 года) с различными опухолями надпочечников. Двустороннее поражение отмечено у 4 больных. Опухоли надпочечников были представлены следующими нозологическими формами: феохромоцитома — у 24 больных, андростерома — у 8 и синдром Иценко—Кушинга (гиперкортицизм) наблюдали у 5. В 6 случаях по данным гистологического исследования выявлена банальная или узелковая гиперплазия ткани надпочечника, течение которых сопровождалось периодическими гипертоническими кризами. Длительность АГ колебалась от 2 до 7 лет.
Основными методами дооперационной диагностики опухолей надпочечников явились ультразвуковое исследование (УЗИ) и компьютерная томография (КТ). Всем больным до операции проводилось определение уровня кортизола и катехоламинов в венозной крови. Все удаленные новообразования надпочечников подвергались морфологическому исследованию.
Результаты
Диагностика опухолей надпочечников основывалась на изучении клинической картины заболевания и резуль-
татов дополнительных исследований. Основными клиническими признаками при феохромоцитоме явились периодическое резкое повышение уровня АД, доходившее до 280/160 мм рт.ст., сопровождающееся сердцебиением, одышкой, болями в животе, рвотой, нарушениями сознания и зрения, побледнением или покраснением кожных покровов и чувством страха смерти. Во время криза отмечались сужение зрачков, набухание вен шеи, резкая потливость и повышение температуры тела до 37,5 °С. Приступы продолжались от нескольких минут до 1,5 ч. В межкризовые периоды АД оставалось в пределах нормы. В некоторых случаях гипертонические кризы наблюдались до 2—3 раз в день.
У больных с синдромом Иценко—Кушинга отмечались характерное для данного заболевания «лунообразное лицо» (n=4), «бизоний горб» (n=2) и «колосс на глиняных ногах» (n=1). Симптомы нарушения углеводного обмена проявлялись по типу стероидного диабета или снижением толерантности к глюкозе с быстро нарастающей гипергликемией и/или глюкозурией. Отмечались также нарушения белкового обмена и мышечная слабость (стероидная миопатия). У всех этих больных отмечались полосы растяжения (стрии) красно-фиолетового цвета на коже живота, груди, бедер и на местах естественных складок. Остеопороз и расстройства гормональной регуляции половой системы (дисменорея, аменорея, вторичное мужское бесплодие) имелись у 3 из них.
Всем больным при поступлении выполняли УЗИ почек и надпочечников. Нами установлено, что опухоли надпочечников диаметром 2,5 см и более достаточно хорошо визуализируются при помощи УЗИ (специфичность — 80%, чувствительность — 82%), однако при гиперплазии надпочечников визуализация новообразования оказалось невозможной, так как гиперплазированная ткань надпочечника и забрюшинная клетчатка имели почти одинаковую эхоплотность. В 24 случаях УЗИ не позволяло достоверно определить размеры опухоли, что было обусловлено небольшой ее величиной или гиперплазией ткани надпочечника. Этим больным выполняли КТ, позволившую в 100% случаев выявить новообразования надпочечника, их размеры, локализацию и взаимоотношение с окружающими органами. Вместе с тем считаем, что УЗИ является основным диагностическим методом на начальном этапе исследования у больных с опухолями надпочечников, которое имеет ряд преимуществ: дешевизна (по сравнению с КТ), высокая информативность, неинвазивность, отсутствие лучевой нагрузки и широкая доступность, что позволяет повсеместно использовать данный метод.
Во всех случаях больным определяли уровень кортизола, инсулина, адренокортикотропного гормона, адреналина и норадреналина в суточной моче и венозной крови. Венозную кровь для исследования брали перед кризами и во время криза. У всех обследованных больных отмечалось повышение уровня перечисленных гормонов.
Во всех случаях при выявлении опухоли надпочечника больным проводили коррекцию основных показателей гемо- и гомеостаза, а также мероприятия по стабилизации АД.
По данным эхо- и электрокардиографии у всех больных отмечалась гипертрофия миокарда желудочков сердца, обусловленная перегрузкой левых отделов, при этом
1, 2013 |
49 |
АРТЕРИАЛЬНАЯ ГИПЕРТЕНЗИЯ
фракция выброса в большинстве случаев оставалась в пределах нормы.
Все больные оперированы в плановом порядке после предоперационной подготовки. Оптимальным доступом при удалении средних и больших опухолей надпочечников явилась торакофренолюмботомия со стороны поражения. Несмотря на высокую травматичность данного доступа, мы считаем его абсолютно показанным у больных с глубоко расположенными опухолями и при больших размерах образования. Однако даже при данном доступе отмечаются значительные трудности в случае удаления большой опухоли, особенно справа. Опыт хирургического лечения больных с различными новообразованиями надпочечников позволил нам разработать показания к адреналэктомии из минидоступа. Критериями отбора пациентов для операции с использованием минидоступа явились отсутствие признаков злокачественного роста, размер опухоли надпочечника не более 5 см, глубина расположения надпочечника не более 10 см. В остальных случаях при новообразованиях более 6 см выполняли торакофренолюмботомию. Адреналэктомия из минидоступа без вскрытия плевральной полости выполнена в 6 случаях, широкая люмботомия без вскрытия плеврального синуса — в 5. Еще в 5 случаях при опухоли средних размеров торакотомия производилась с частичным вскрытием синуса без последующего дренирования плевральной полости.
Когда поражения надпочечника сопровождались стойкой АГ, после наложения зажима на сосудистую ножку ее пересечение сразу не проводили во избежание острой надпочечниковой недостаточности и снижения АД. Сосудистую ножку пережимали на 10—15 мин, следя за АД, а затем выполняли адреналэктомию. После перевязки собственной вены надпочечника с целью профилактики гипотензии проводили интраоперационную гиперволемическую гемодилюцию.
Удаление опухоли во всех случаях выполняли в объеме расширенной адреналэктомии с прилегающей забрюшинной клетчаткой, не оставляя даже неизмененную часть органа. Подобную тактику считаем оправданной в отсутствие экспресс-диагностики морфологии опухоли. При гистологическом изучении макропрепарата признаки малигнизации обнаружены у 4 больных.
Ввиду сложности и вариабельности ангиоархитектоники надпочечников, а также изменений топографических взаимоотношений анатомических образований при больших опухолях хирургическое вмешательство представляет технические трудности и нередко сопровождается кровопотерей и опасностью развития ятрогенных повреждений. Наибольший риск представляют случаи отрыва центральной вены правого надпочечника от стенки нижней полой вены, которые, как правило, сопровождаются обильным кровотечением.
Традиционно хирургическое лечение заболеваний надпочечников выполняется в отделениях сосудистой хирургии. Это связано, во-первых, с риском возникновения ятрогенных травм магистральных сосудов, особенно при больших размерах образования, кровотечением из сосудов надпочечника, а в ряде случаев необходимостью мобилизации аорты, нижней полой вены, почки и почечных сосудов перед радикальным удалением опухоли. Так, при объемных образованиях надпочечника почка, как прави-
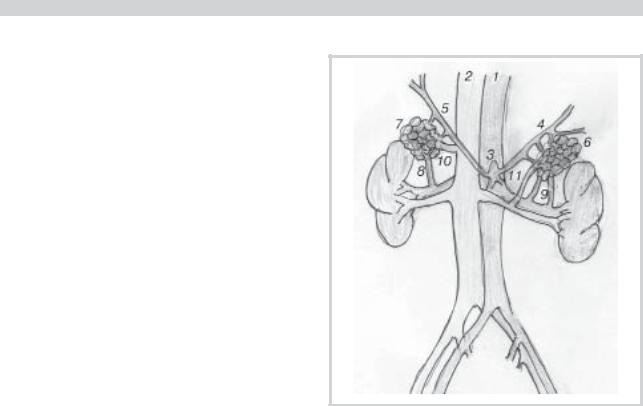
Схема кровоснабжения надпочечников.
1 — аорта; 2 — нижняя полая вена; 3 — чревный ствол; 4—5 — диафрагмальные артерии; 6—7 — надпочечники; 8—9 — надпочечниковые артерии; 10—11 — центральные вены надпочечников.
ло, значительно опускается вниз, тогда ее сосудистая ножка перегибается и оказывается позади нижнего полюса опухоли и соответственно может быть принята за надпочечниковую артерию, отходящую от почечной артерии.
Такое топографо-анатомическое изменение в одном из наших наблюдений стало причиной пересечения и перевязки основного ствола левой почечной артерии. Изменение цвета декапсулированной почки позволило обнаружить данную техническую ошибку на этапе осуществления контрольного гемостаза. Магистральный почечный кровоток восстановлен путем формирования анастомоза конец в конец.
Артерии, кровоснабжающие надпочечники, отходят непосредственно из аорты или диафрагмальной ветви чревного ствола и от почечной артерии (см. рисунок). Венозный отток крови справа всегда происходит в нижнюю полую вену, причем через короткую центральную вену надпочечника длиной не более 1,0—1,5 см. Другие надпочечниковые вены могут впадать в собственные почечные вены и при опухолевых поражениях, как правило, значительно расширяются в диаметре. В некоторых случаях встречаются также варианты аномалии кровоснабжения надпочечников. Такая ангиоархитектоника органа, несомненно, представляет технические трудности во время операции и нередко сопровождается дополнительной кровопотерей.
Имеются многочисленные сообщения о тяжелых последствиях при технически неверных попытках остановки кровотечения, приводящих к увеличению масштаба травмы. Мы согласны с некоторыми авторами, что наличие навыков по сосудистой хирургии позволяет в подобных
50 |
1, 2013 |

случаях предварительно выделить и лигировать отводящие и приводящие сосуды, дифференцировать другие сосуды жизненно важных органов, а затем удалить опухоль [9, 20].
В4 наблюдениях при двустороннем поражении надпочечников операции выполнялись поэтапно, с интервалом 4—6 мес.
Средняя продолжительность пребывания больных в реанимационном отделении после миниинвазивной адреналэктомии составила 1,0±0,2 дня. У пациентов, перенесших адреналэктомию из традиционного доступа, это время было значительно больше и составило 2,8±0,2 сут. Следует также отметить, что интенсивность болевого синдрома после операций из минидоступа была меньше, и это позволило применять в послеоперационном периоде обычные обезболивающие средства. Наркотические анальгетики использовались у больных, перенесших адреналэктомию через торакофренолапаротомный доступ.
Впослеоперационном периоде раневых осложнений не было.
Один летальный исход отмечен у одной больной с двусторонним поражением надпочечника. Смерть наступила от острой сердечно-сосудистой недостаточности перед вторым этапом операции.
Стойкий гипотензивный эффект после операции получен у 25 пациентов. 8 больных после операции продолжали принимать антигипертензивные препараты, но в минимальных дозах.
У больных с синдромом Иценко—Кушинга после операции, начиная от 6 мес до 2 лет, отмечался постепенный регресс симптомов заболевания. Рецидивов заболевания за 9-летний период наблюдений не выявлено.
В4 наблюдениях при гистологическом исследовании опухоли верифицирован ее злокачественный характер, в связи с чем дальнейшее лечение больные получали в онкологическом диспансере.
Обсуждение
Лечение больных с заболеваниями надпочечников — одна из наиболее сложных проблем медицины, что обусловлено генетическими факторами, низкой распространенностью, сложностями диагностики и хирургического лечения.
Как отмечают П.С. Ветшев и соавт. [6], ультразвуковой метод диагностики опухоли надпочечников является одним из наиболее эффективных, чувствительность которого по данным авторов составляет 94,3%. При этом дополнительное использование дуплексного сканирования позволяет определить степень кровоснабжения опухоли, состояние и отношение аорты и нижней полой вены к опу-
холи. Вместе с тем КТ и магнитно-резонансная томография с контрастированием, несомненно, имеют более высокую чувствительность (97,7%), а при условии возможности воссоздания трехмерного изображения позволяют дополнить и уточнить топографо-анатомические взаимоотношения опухоли с окружающими тканями [1, 2, 6].
Изучение состояния и функции надпочечников, на наш взгляд, должно явиться основным компонентом программы обследования пациентов с высоким АД.
Основной и наиболее эффективный метод лечения больных с опухолями надпочечников — хирургический. Для адекватности выполняемых операций на надпочечниках, минимизации операционной травмы, способствующей ранней активизации больных, предложено большое количество хирургических доступов [2]. Операции с применением эндовидеотехнологий и из минидоступа наиболее предпочтительны в связи с малой травматичностью и прецизионностью манипуляций.
Авторы, обладающие наибольшим опытом использования лапароскопических технологий удаления опухолей надпочечников, считают данный метод высокоэффективным [22, 25]. По данным W. Shen и соавт. [22], при выполнении лапароскопической операции по удалению опухолей надпочечников лишь в 4 случаях была осуществлена конверсия в открытое вмешательство и в одном наблюдении дополнительно использовали ручную ассистенцию. Вместе с тем высокий процент злокачественного перерождения феохромоцитом и большие размеры образования обусловливают необходимость более радикальной хирургической операции, что достигается путем применения традиционных методов [14, 20, 22]. Возможности использования других малоинвазивных методик, в частности операций из «малых» доступов, в хирургии надпочечников мало изучены. Разработка же новых, более эффективных способов хирургических вмешательств, сохраняющих принцип малоинвазивности, представляется актуальной [3, 13, 25].
Несмотря на множество преимуществ минидоступов и лапароскопических технологий, отсутствие стандартизированных подходов к их выполнению приводит к некоторым существенным недостаткам. Так, по данным С.В. Сергийко [11], конверсия минидоступа в более широкий была проведена у 6,8% пациентов, в том числе с целью ликвидации осложнений, а при лапароскопической адреналэктомии необходимость в изменении способа операции возникла в 33,3% случаев.
Непосредственная близость магистральных сосудов забрюшинного пространства к опухолям надпочечников и необходимость в ряде случаев манипуляции на них обусловливают целесообразность выполнения подобных операций в отделениях сосудистой хирургии.
ЛИТЕРАТУРА
1. Бельцевич Д.Г., Кузнецов Н.С. Причины рецидивов у больных |
3. Бондаренко В.О., Луцевич О.Э. Топографическая диагности- |
с опухолями хромаффинной ткани. Хирургия 2002; 8: 19— |
ка и хирургические вмешательства при гигантских феохро- |
23. |
моцитомах надпочечника. Хирургия 2011; 3: 13—18. |
2.Бокерия Л.А., Абдулгасанов Р.А. Феохромоцитомы: современ- 4. Васютков В.Я. Повреждения магистральных сосудов во вре-
ные методы диагностики и хирургического лечения. Анналы |
мя хирургических вмешательств у онкологических больных. |
хир 2011; 2: 5—9. |
Вопр онкол 1988; 12: 1485—1489. |
1, 2013 |
51 |

АРТЕРИАЛЬНАЯ ГИПЕРТЕНЗИЯ
5. |
Ветшев П.С., Полунин Г.В. Спорные и нерешенные вопросы |
16. |
Hong-chao He, Jun Dai., Zhou-jun Shen. et al. Retroperitoneal |
|
в диагностике и хирургическом лечении первичного гипер- |
|
Adrenal-Sparing Surgery for the Treatment of Cushing’s Syn- |
|
альдостеронизма (к 50-летию описания синдрома Конна). |
|
drome Caused by Adrenocortical Adenoma: 8-Year Experience |
|
Хирургия 2006; 1: 17—21. |
|
With 87 Patients. World J Surg 2012; 36: 5: 1182—1188. |
6. |
Ветшев П.С., Симоненко В.Б., Ипполитов Л.И. и др. Опухоли |
17. |
Katsube Y., Saro H., Naka M. Decreased baroreflex sensitivity in |
|
хромаффинной ткани (клиника, диагностика, хирургиче- |
|
patients with stable artery disease is correlated wire the severity of |
|
ское лечение). Хирургия 2002; 8: 11—18. |
|
coronary narrowing. Am J Cardiol 1996; 78: 1007—1010. |
7.Высоцкий В.Ф. Дифференциальная диагностика и хирурги18. Kirkby-Bott J., Brunaud L., Mathonet M. et al. Ectopic Hormone-
ческая тактика при новообразованиях надпочечников: Автореф. дис. … канд. мед. наук. Иркутск 2012; 26.
8.Калинин А.П., Майстренко Н.А., Ветшев П.С. Хирургическая эндокринология. СПб: Питер 2004; 941.
9.Камолов Т. Профилактика и хирургическое лечение ятрогенных повреждений магистральных сосудов и их последствий: Автореф. дис. ... канд. мед. наук. М 1984; 28.
10.Полякова Г.А., Калинин А.П., Безуглова Т.В., Шумский В.И.
Надпочечниковые и вненадпочечниковые феохромоцитомы: сравнительная оценка иммуногистохимического прогностического маркера тенасцина С и гистологических градаций малигнизации. Анналы хир 2009; 5: 70—73.
11.Сергийко С.В. Операции «малых» доступов и оптимизация тактики хирургического лечения новообразований надпочечников: Автореф. дис. … д-ра мед. наук. Челябинск 2010; 43.
12.Сергийко С.В., Привалов В.А., Лукьянов С.А. Хирургическая тактика при случайно выявленных опухолях надпочечников. Анналы хир 2009; 1: 49—53.
13.Цуканов Ю.Т., Цуканов А.Ю. Боковой внебрюшинный минидоступ для адреналэктомии. Хирургия 2003; 9: 7—10.
14.Gaibov A.D., Usmanov N.U., Sultanov D.D. Sustantiation of surgery on epinephriums in the management of vasorenal hypertension. 2th international congress of cardiologists of Turkish-speak- ing countries. Turkish 2000; 138—139.
15.Grogan R.H., Mitmaker E.J., Quan-Yang Duh. Changing paradigms in the treatment of malignant pheochromocytoma. Cancer Control 2011; 18: 2: 104—112.
Secreting Pheohromacytoma: A Francofone Observational Study. World J Surg 2012; 36: 6: 1382—1388.
19.Muth A., Abel F., Jansson S. et al. Prevalence of Germline Mutations in Patients with Pheohromacytoma or Abdominal Paraganglioma and Sporadic Presentation: A Population-Based Study in Western Sweden. World J Surg 2012; 36: 6: 1389—1394.
20.Park J. Predictive characteristics of malignant pheochromocytoma. Korean J Urol 2011; 52: 241—246.
21.Powell A.C. Surgical management of cushing syndrome secondary tomicronodular adrenal hyperplasia. Surgery 2008; 143: 6: 750— 758.
22.Shen W.T. One hundred two patients with pheochromocytoma treated at a single institution since the introduction of laparoscopic adrenalectomy. Arch Surg 2010; 145: 9: 893—897.
23.Simforoosh N. Laparoscopic adrenalectomy ten-year experience, 67 procedures. Urol J 2008; 5: 1: 50—54.
24.Vazcuez B.J., Richards M.L., Lohse C.M. et al. Adrenalectomy Improves Outcomes of Selected Patients with Metastic Carcinoma. World J Surg 2012; 36: 6: 1400—1405.
25.Vidal O., Astudillo E., Valentini M. et al. Single-Incision Transperitoneal Laparoscopic Left Adrenalectomy. World J Surg 2012; 36: 6: 1395—1399.
26.Waldmann J. Microarray analysis reveals differential expression of benign and malignant pheochromocytoma. Endocrine-Related Cancer 2010; 17: 743—756.
Поступила 15.08.12
52 |
1, 2013 |
