
975741
.pdfА натомо-фізіологічні особливості
Удітей ферментний склад шлункового соку не відрізняється від дорослих.
Вньому містяться соляна кислота, пепсин, гастриксин, ліпаза, хімозин (сичуговий фермент, лабфермент) та ін. Проте у дітей першого року життя протеолітична активність шлункового соку низька. Активність пепсину на 3050% нижча, ніж у дорослих. Зокрема, активність пепсину у дітей першого року життя становить 2-16 од., у дітей старшого віку — 16-32 од. Це пов'язано з малою кількістю в слизовій оболонці клітин, які виробляють пепсин, а також з лужною реакцією рН шлункового соку. Відомо, що пепсин проявляє максимальну активність при рН шлункового соку 1-1,5, тоді як у новонародже ного відразу після народження вміст шлунка лужний (рН 6,5-8). З віком величина рН шлункового соку зміщується в кислу сторону (табл.25).
Протягом першого року життя протеолітична активність шлункового соку зростає в 3 рази, а у дорослих вона в 2 рази вища, ніж у дітей наприкінці першого року життя.
Об'єм секреції шлункового соку у дітей також нижчий. У новонароджених і дітей перших місяців життя він становить лише 1/10 об'єму секреції дорослих (див. табл. 25).
У дітей також нижча загальна кислотність шлункового соку. У новонарод жених вона становить 3-6 титр.од., тоді як у дорослих — 40-60 титр.од., і з віком загальна кислотність у дітей зростає (табл. 41).
|
|
|
|
|
Таблиця 41 |
Характеристика шлункового соку у дітей різного віку |
|||||
|
|
|
|
|
|
Вік |
Об'єм, |
рН |
Вільна кислотність, |
Загальна кислотність, |
|
|
мл/хв |
|
титр. од. |
титр. од. |
|
Новонароджені |
0,1-0,3 |
6,5-8 |
0-0,5 |
3-6 |
|
1 рік |
0,2-1 |
1,5-3 |
5-10 |
10 |
-15 |
2-7 років |
0,5-1,5 |
1-2 |
1015 |
20 |
-25 |
8-10 років |
1-2 |
1-2 |
1215 |
25 |
-30 |
11-14 років |
1-5 |
1-2 |
1520 |
30-35 |
|
У дитячому віці значно знижена концентрація вільної соляної кислоти в Шлунковому секреті. У новонароджених цей показник становить 0,5 титр. од. 1 в міру росту дітей він збільшується, але не досягає величин дорослих (див. табл. 25).
Знання показників шлункового соку необхідні лікарям-педіатрам для правильної інтерпретації результатів фракційного зондування шлунка.
Тонка і товста кишки у дітей раннього віку відносно довші, ніж у дорослих. Дітей грудного віку їх довжина в 6 разів перевищує довжину тіла, тоді як у Дорослих — тільки в 4 рази. У дітей кишки більш рухливі, в них виражені не Тиіьки перистальтичні, але й антиперистальтичнгрухи. Все це сприяє можливій 'Пвагінації кишок у дітей. Більша довжина і рухливість стосуються також сліпої
191
РоздМА
кишки та апендикса, який легко зміщується, і тому діагностувати апендицит у дітей значно важче, оскільки можливе нетипове його положення.
Крім того, пряма кишка теж довша, має слабко фіксовані слизову і підслизову оболонки, що сприяє випадінню її при патологічних процесах.
Процеси розщеплення і всмоктування харчових речовин у кишках дітей відбуваються досить активно.
Печінка у новонародженого є одним з найбільших органів і становить 4,38% його маси тіла. Вона займає майже половину об'єму черевної порожнини. У дітей до 6 міс. життя печінка виступає з-під краю реберної дуги на рівні серединно-ключичної лінії на 2-3 см, у дітей віком 6 міс. - 2 роки — на 1,5 см, 3- 7 років — на 0,5-1 см. У дітей, старших 7-річного віку, печінка, як правило, не виступає з-під краю реберної дуги.
Структура печінки у дітей не має закінченої будови, вона функціонально незріла, що зумовлює досить часте її ураження патологічним процесом при інтоксикації та інфекції. В першу чергу це пов'язано з тим, що дезінтоксикаційна функція печінка недостатньо розвинена.
Підшлункова залоза у дітей раннього віку більш рухлива, поверхня її гладка, гістоструктура бідна на сполучну тканину і не досить диференційована. Секреторна та інкреторна функції підшлункової залози виражені, але активність ферментів зростає тільки з віком дитини.
Вказані особливості функціонування травного каналу у дітей потрібно враховувати при організації раціонального харчування і клініко-лаборатор- ному їх обстеженні.
8.10. Імунна система
Функціональна активність імунної системи у дітей різних вікових груп має значні відмінності, які визначають їх чутливість до інфекційних агентів і впливають на захворюваність.
Особливості імунної системи у плода можна розподілити на дві групи. До першої з них належать особливості розвитку (онтогенезу) імунної системи, до другої — особливості її функціонування.
Вонтогенезі імунної системи виділяють такі особливості:
1)розвиток клітин і органів імунної системи відбувається незалежно, з різних ембріональних закладок і спочатку функціонально вони не взаємодіють;
2)утворення материнських клітин лімфопоезу відбувається не в спеціалізованих органах імунної системи, які не виконують своєї специфічної функції, а спочатку в жовтковому мішку (на 3-6-му тижні внутрішньоутробного періоду), а потім в ембріональній печінці (на 6-15-му тижні внутрішньо утробного періоду);
192

А натомо-фізіологічні особливості
3)характерна міграція стволових клітин в центральні органи імуногенезу і їх ізольоване дозрівання в зрілі Т- і В-лімфоцити (на 12-16-му тижні внуТ|рішньоутробного періоду);
4)характерна послідовність синтезу імуноглобулінів, що проявляється
більш раннім синтезом і (на 20-му тижні внутрішньоутробного періоду), тоді як синтез І§А дещо запізнюється, і ця властивість імунокомпетентних клітин з'являється після 30-го тижня внутрішньоутробного періоду.
Клінічне значення наведених даних полягає в тому, що вони є основою для розуміння патогенезу вроджених імунодефіцитних станів . Механізм виникнення найбільш поширених вроджених імунодефіцитів у дитячому віці представлений в табл. 42.
|
|
Таблиця 42 |
|
Становлення основних імунних реакцій в онтогенезі |
|
|
і формування вроджених імунодефіцитних станів |
|
|
|
|
Тиждень |
Імунні реакції |
Вроджений імунодефіцит |
гестації |
|
|
6-8 |
Формування тимусу |
Синдром Ді Джорджа |
|
|
Синдром Незелофа |
8-9 |
Початок диференціювання лімфоцитів у |
Лімфоцитофтиз |
|
загрудинній залозі |
|
10-12 |
Початок синтезу імуноглобулінів (І§ М, |
Хвороба Брутона |
11-12 |
Початок функціонування кісткового |
Ретикулярна дисгенезія |
|
мозку |
|
12-15 |
Заселення лімфатичних вузлів |
Синдром Луї-Бара |
|
лімфоцитами |
|
ЗО |
Синтез ^ А |
Селективний дефіцит їй А |
Наприкінці першої половини вагітності, як правило, закінчується формування імунної системи, диференціювання Т- і В-лімфоцитів як основних клітин імунної системи і їх субпопуляцій, а також відбувається становлення Функціональної активності імунної системи. Протягом другої половини вагітності імунна система плода досить активна, але як морфологічно, так і Функціонально вона незріла.
По-перше, у другій половині вагітності Т-система імунітету недосконала, Що проявляється меншим числом Т-лімфоцитів, кількість яких навіть на момент народження нижча (до 50%), ніж у дітей в постнатальному періоді та дорослих (60-70%). Але із збільшенням строку вагітності кількість Т-лімфоцитів в периферичній крові поступово зростає з 25 до 50%>. Цитотоксична функція Т- л|мф0цитів-кіллерів значно нижча, тоді як їх проліферативна активність у Одповідь на дію мітогену фітогемаглютиніну (ФГА) досить висока і не ВіДрізняється від показників у дорослих.
25~747 |
193 |
|
Розділі
Недостатньо повноцінна активність Т-системи імунітету у плода обумовлює високу чутливість до протозойних і вірусних інфекцій, наприклад, таких як краснуха, герпес, вірусний гепатит, токсоплазмоз, лістеріоз та ін.
По-друге, кількість В-лімфоцитів у плода найбільш висока до 28-го тижня вагітності і в подальшому їх число знижується з 35 до 25% на момент народження.
По-третє, В-лімфоцити у плода не можуть перетворюватись в плазматичні клітини і ця здатність з'являється вже після народження, починаючи з 1,5- місячного віку. Ця особливість пояснює той факт, що у плода відзначається дуже низький рівень ^ М і ^ А, які синтезуються, а не проникають через плаценту. У плода рівень (менше 0,1 г/л) становить приблизно 8-10% його концентрації у дорослих, а рівень ^А (0,03-0,05 г/л) — тільки 0,4% рівня дорослих.
Визначення рівня імуноглобулінів вказаних класів може бути показником внутрішньоутробного інфікування плода. Вважають, що якщо рівень І§М
перевищує 0,2 г/л, а концентрація |
вища 0,1 г/л, то це свідчить про перенесену |
внутрішньоутробну інфекцію. |
|
Концентрація ^ О у плода досягає 99% його рівня у дорослих. Це зумовлено не власним синтезом цього класу імуноглобуліну, а його трансплацентарною передачею від вагітної. Материнські проникають через плаценту протягом вагітності, але особливо активно цей процес відбувається між 22-26-м тижнями
внутрішньоутробного періоду. Трансплацентарний транспорт |
забезпе |
|
чується Бс-рецепторами, які знаходяться на плаценті. |
|
|
Трансплацентарне проникнення материнських |
забезпечує захист плода |
|
і організму дітей в перші місяці життя від інфікування патогенними мікроорганізмами, проти яких використовується гуморальний тип імунітету. Завдяки цьому діти в першому півріччі не хворіють на кір, вітряну віспу, скарлатину, дифтерію та деякі інші інфекції.
У постнатальному періоді життя відбувається подальше становлення і дозрівання імунної системи.
Тимус (загрудинна залоза) є центральним органом імуногенезу. Він знаходиться за грудиною на рівні ІІ-ГУ ребра. У новонароджених маса загрудинної залози становить у середньому 12 г і поступово збільшується, досягаючи в період статевого дозрівання 35-40 г, а потім починає зменшуватись за рахунок епітеліального компонента строми органа. П р и оцінці гістоструктури залози звертає увагу те, що у дітей переважає кіркова речовина, шо містить велику кількість лімфоцитів (тимоцитів) . Тимус забезпечує проліферацію і дозрівання клітин в активно функціонуючі Т-лімфоцити. Ие відбувається під впливом ряду факторів, які активно синтезуються в тимусі, так званих тимічних гормонів — тимозину, тимопоетину, тималіну та ін.
Селезінка відіграє важливу роль в імунних реакціях організму. В ній відбувається накопичення плазматичних клітин із В-лімфоцитів, які потії*1
194

А натомо-фізіологічні особливості
синтезують антитіла до мікробних і тканинних антигенів. У дітей перекладки селезінки ніжніші і багатші на клітинні елементи, ніж у дорослих, її будова ще не закінчена і цей процес спостерігається протягом 7-8 років життя.
Лімфатичні вузли у новонароджених і дітей раннього віку мають дещо більші розміри, тонку і ніжну капсулу, м'які, мало містять сполучної тканини і трабекул, але досить багаті на лімфоїдні елементи. їх синуси широкі, однак крайовий синус не виражений.
Лімфатичні вузли виконують бар'єрно-фільтраційну функцію, затримуючи корпускулярні антигени, та захисну функцію, синтезуючи імуноглобуліни. Проте вказані функції лімфатичних вузлів у дітей першого року життя недосконалі, що може сприяти генералізації інфекційного процесу.
Характеризуючи стан Т-системи імунітету у дітей раннього віку, не можна вважати його дефіцитним, оскільки, незважаючи на низький процент Т- лімфоцитів (45-53%), їх абсолютна кількість значно більша, ніж у дорослих. З віком відносна кількість Т-лімфоцитів зростає, а абсолютна зменшується, оскільки зменшується загальна кількість лімфоцитів в периферичній крові. Як правило, до 7-8 років відносна і абсолютна кількість Т-лімфоцитів в периферичній крові дітей досягає величин дорослих людей (табл. 43).
Крім того, Т-лімфоцити у новонароджених мають високу здатність до проліферації і трансформації в бластні клітини під дією ФГА.
У популяції Т-клітин співвідношення Т-лімфоцитів-хелперів і супресорів у новонароджених значно відрізняється від дорослих. У новонароджених в периферичній крові співвідношення Т-хелперів і Т-супресорів дорівнює 3,1- 3,3, у дорослих — 2-2,5.
Цитотоксична активність Т-лімфоцитів у дітей раннього віку знижена, що обумовлює високу чутливість дітей до вірусів, які розмножуються в клітинах, а їх лізис забезпечують саме Т-лімфоцити-кіллери.
Таблиця 43
Показники клітинної ланки імунної системи у дітей різних вікових груп
|
Вік |
Т-лімфоцити |
В-лімфоцити |
||
|
|
•10»в1л |
% |
•10»в 1 л |
% |
Новонароджені |
2,9-3,3 |
48-53 |
0,5-1,1 |
20-25 |
|
1-12 |
міс. |
2,5-2,7 |
55-60 |
0,4-0,6 |
18-23 |
2-7 років |
1,9-2,1 |
60-65 |
0,3-0,5 |
17-20 |
|
8-14 |
років |
1,5-1,8 |
65-70 |
0,3-0,4 |
18-25 |
|
|
|
|
|
|
Відносна кількість В-лімфоцитів в периферичній крові дітей раннього віку також дещо нижча, але їх абсолютне число більше, ніж у дітей старшого віку (табл. 43).
Концентрація імуноглобулінів в сироватці крові залежить від віку дітей і ці Чані наведені в табл. 44
25« |
195 |
|
РрзділЛ
|
|
|
|
|
|
|
Таблиця 44 |
|
Середня концентрація імуноглобулінів у сироватці крові дітей |
||||||
|
|
|
залежно від віку |
|
|
||
|
|
|
|
|
|||
|
Вік |
І8 О, г/л |
І£ А, г/л |
І£ М, г/л |
|||
1-7 днів |
11,6(8,8-15,5) |
0,14(0-0,27) |
0,19(0,06-0,33) |
||||
1 |
міс. |
10,9 |
(5,8-15,6) |
0,09 (0-0,26) |
0,23 |
(0,07-0,54) |
|
3 |
міс. |
4,3(1,7- 7) |
0,37 |
(0,09-0,66) |
0,51 |
(0,24-0,78) |
|
5 |
міс. |
5,1(1,8- 8,3) |
0,37 (0-0,90) |
0,6 |
(0,11-1,10) |
||
7 |
міс. |
7(3-11,0) |
0,44 |
(0,05-0,82) |
0,71 |
(0,36-1,08) |
|
10 міс. |
8,2 |
(3,4-12,9) |
0,46 (0-0,88) |
0,8 |
(0,13-1,47) |
||
12 міс. |
9(4,6-13,4) |
0,49 |
(0,12-0,86) |
0,82(0,36-1,24) |
|||
2 роки |
9,1 |
(5,4-12,9) |
0,63 |
(0,24-1,03) |
0,87(0,48-1,35) |
||
3 роки |
9,5 |
(4,6-14,6) |
0,78 |
(0,26-1,32) |
0,9 |
(0,48-1,33) |
|
4 роки |
10 |
(5,7-14,3) |
0,87 |
(0,27-1,46) |
0,95 (0,4-1,5) |
||
5 років |
10,4 |
(4,8-15,9) |
0,94(0,12-1,73) |
0,97 |
(0,51-1,44) |
||
6-10 років |
12,2(5,4-17) |
1,14(0,37-1,9) |
1,03 |
(0,51-1,55) |
|||
11-15 років |
11,7 |
(5,3-18,1) |
1,24 |
(0,58-1,9) |
1,15(0,44-2,14) |
||
|
|
|
|
|
|
|
|
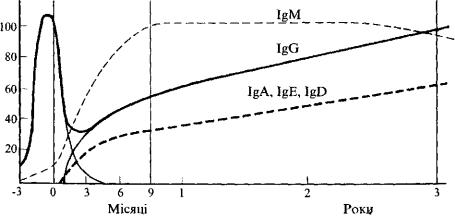
Для дітей віком 3-6 міс. характерна транзиторна гіпоімуноглобулінемія. Концентрація імуноглобулінів в цей період мінімальна і становить лише 33-
37% рівня дорослих. Це відбувається тому, що материнські |
катаболі- |
зуються, а власний синтез імуноглобулінів ще недостатній (рис. 45). |
|
У подальшому, починаючи з 6-місячного віку, концентрація |
поступово |
наростає, але до 12-16 років досягає лише 90% рівня дорослих. Що стосується 1% А і \% М, то їх рівень відразу після народження поступово зростає і до 12-16 років досягає 80-85% рівня дорослих людей (рис. 45).
Рис. 45. Динаміка рівня імуноглобулінів у сироватці крові у дітей першого року життя (в %).
196

Анатомо-фізіологічні особливості
Слід також відзначити, що у новонароджених, особливо в перші дні життя, значно знижений рівень секреторного І^А (в слині, сечі, шлунковому соку та ін.), ІД° сприяє колонізації слизових оболонок верхніх дихальних шляхів, сечових шляхів і травного каналу патогенними бактеріями. Але вже через 6-8 тиж. після народження у дітей спостерігається інтенсивний синтез секреторного
8.11.Ендокринна система
Залози внутрішньої секреції, або ендокринні, є особливою системою органів, що виділяють біологічно активні речовини — г о р м о н и . До ендокринних залоз належать: гіпофіз, передній гіпоталамус, епіфіз, щитовидна і паращитовидні, підгрудинна, надниркові, острівцевий апарат підшлункової залози, статеві.
Ендокринні залози мають великий вплив на обмін речовин, на фізичний і психічний розвиток організму дитини. В дитячому віці значення ендокринних залоз особливо велике, оскільки вони беруть участь в регуляції таких важливих для організму процесів, як ріст і розвиток (диференціювання). Тому при розладах функцій залоз внутрішньої секреції у дітей виникає своєрідна клінічна картина, яка не зустрічається у дорослих. Одна й та ж аномалія залоз, яка у дорослих викликає оборотні зміни, у дитячому віці може призвести до формування невиліковного психічного і фізичного дефекту.
Крім того, усі види обміну речовин — водний, мінеральний, вуглеводний, білковий і жировий — відбуваються за участю гормонів. Порушення діяльності ендокринних залоз призводить нерідко до різких змін в обміні речовин, що в свою чергу є причиною серйозних захворювань у дітей.
Розглянемо особливості функціонування ендокринних залоз в дитячому віці.
Щитовидна залоза — одна з найактивніших залоз внутрішньої секреції, гормональна функція якої значною мірою визначає інтенсивність обміну речовин, а в структурі ендокринної патології дитячого віку захворювання Щитовидної залози посідають одне з основних місць. Особливо це актуально Для зон, забруднених радіонуклідами.
Про важливе функціональне значення щитовидної залози для розвитку Дитини свідчить перш за все рання її закладка у ембріона. Вже в кінці 3-4-го тижня ембріонального періоду щитовидна залоза закладається у вигляді невеликого валика з вентральної стінки глоткового відділу кишечника. У Подальшому щитовидна залоза дуже швидко розвивається і вже до 4-го місяця ВнУтрішньоутробного життя має цілком сформовану структуру. Вже в цьому Періоді вона складається з двох часточок і перешийка.
197
Розділ 8
До кінця 2-го місяця внутрішньоутробного розвитку щитовидна залоза функціонально неактивна, оскільки ще не має фолікулярної структури, х а р а к т е р н о ї для зрілого життя . Але п о ч и н а ю ч и з кінця 2-го місяця внутрішньоутробного розвитку, з'являються фолікули, і в їх порожнинах накопичується тиреоглобулін, який спочатку не містить йоду і не бере участі в синтезі тиреоїдних гормонів. Через декілька днів тиреоглобулін здатний захоплювати неорганічний йод, що надходить з кров'ю від матері. В кінці 3-го місяця внутрішньоутробного розвитку починається синтез тироксину і трийодтироніну. Але спочатку в крові вони циркулюють у зв'язаному стані не з тироксинзв'язуючим глобуліном, а з альбумінами, оскільки синтез тироксинзв'язуючого глобуліну відсутній. Він спостерігається з кінця 5-го місяця внутрішньоутробного розвитку і відмічається його інтенсивне зв'язування з тироксином.
У крові сліди тироксину виявляються з кінця 3-го місяця внутрішньо утробного періоду, а потім концентрація його швидко підвищується, становлячи до кінця 6-го місяця 50% величини концентрації у крові дорослої людини — відповідно 26±3 нг/мл і 69± 1,3 нг/мл, а на 8-9-му місяці перевищує в 1,5 раза цифри у дорослого — 99±11) нг/мл.
Підтвердженням високої концентрації тироксину і високої функціональної активності щитовидної залози може бути факт покращення загального стану і зменшення вираженості симптомів гіпотиреозу у вагітних, у яких знижена функція щитовидної залози.
Крім екскреції тироксину і трийодтироніну, в стінці фолікулів щитовидної залози, а також парафолікулярно зустрічаються С-клітини, що виробляють гормон — кальцитонін, який знижує рівень кальцію в крові. Під його впливом гальмується резорбція оксіапатиту кісток і підсилюється його відкладання в органічному матриксі кісткової тканини. Тому кальцитонін має важливе значення в процесах регуляції остеогенезу і скелетоутворення. Кальцитонін є антагоністом паратгормону. Кальцитонінпродукуючі клітини виявляються в щитовидній залозі на 14-му тижні внутрішньоутробного розвитку, і в цей час визначається продукуючий кальцитонін.
Під час пологів після відокремлення дитини від матері відмічається високий вміст кальцитоніну в крові. Це розцінюється як його участь в родовому стресі. Висока концентрація кальцитоніну сприяє зниженню рівня кальцію в крові, що обмежує надмірну активацію ряду ендокринних залоз, для яких іон кальцію служить стимулятором секреції. До таких залоз належать гіпофіз, кора наднирників, Р-клітини апарату підшлункової залози.
При народженні щитовидна залоза у дитини відносно більша, ніж в наступні роки життя. Протягом першого року життя вираженого росту паренхіми щитовидної залози не відбувається, але потім починається бурхливе збільшення маси залози до 5-6-річного віку. У подальшому темп росту уповільнюється а*
198

А натомо-фізіологічні особливості
до передпубертатного періоду. Але у віці 12-15 років відмічається особливо бурхливий ріст щитовидної залози, причому вона настільки збільшується в розмірах, що можна відмітити деяку припухлість залози і це викликає турботу у батьків. В нормі залоза не пальпується і не помітна при зовнішньому огляді. Важливо підкреслити, що розміри щитовидної залози суттєво залежать від кровонаповнення.
Збільшення розмірів залози корелює з підсиленням її функціональної активності, яке спостерігається у віці від 6 міс до 2 років. Найбільш виражена активність щитовидної залози спостерігається в передпубертатному періоді (у хлопчиків — в 10-12 років, у дівчаток — дещо раніше) і досягає максимального рівня у представників обох статей у віці 14-15 років.
Гістологічна структура щитовидної залози в період новонародженості вказує на незавершеність її будови: фолікули ще погано виражені і в їх просвіті немає або майже немає колоїду; епітелій фолікулів циліндричний; мають місце скупчення епітеліальних клітин, які розділені ніжними сполучнотканинними прошарками.
З віком в залозі збільшується кількість фолікулів і вміст колоїду, зникає циліндричний епітелій і з'являється плоский. Остаточна гістологічна структура залози завершується після 15 років.
Основними гормонами щитовидної залози є тироксин, трийодтиронін і тиреокальцитонін. Гормони щитовидної залози, як відмічалося раніше, значно впливають на обмінні процеси. Зокрема, показано, що гормони щитовидної залози підсилюють газообмін і перш за все — поглинання кисню тканинами і виділення вуглекислого газу, впливають на білковий обмін, посилюючи як асимілятивні, так і дисимілятивні процеси. Крім того, гормони щитовидної залози значно впливають на процеси обміну жирів і вуглеводів, посилюють виділення води і беруть участь в обміні хлоридів, впливаючи на мінеральний обмін і розвиненість скелета, а також визначають обмін калію і кальцію в організмі.
Таким чином, ці гормони є універсальними стимуляторами метаболізму, росту і розвитку. Природно, що недостатня або надмірна продукція гормонів Щитовидної залози викликає різноманітні і значні порушення життєдіяльності Дитячого організму.
Вклінічній практиці може спостерігатися як підвищення (гіперфункція),
так і зниження (гіпофункція) активності щитовидної залози, які мають ряд специфічних клінічних ознак.
Паращитовидні залози з'являються на ранніх стадіях ембріонального Розвитку. їх можна виявити у ембріона на 6-му тижні внутрішньоутробного Розвитку. У цей період починається секреція паратгормону. Концентрація Царатгормону в крові пупкових судин близька до такої в крові матері (0,07- ' -> нг/мл), але підтримуються ці концентрації незалежно.
199
РрзділЛ
Паращитовидні залози функціонують найбільш активно до 4-7 років. Клітинний склад залоз представлений в основному світлими головними клітинами, які дуже активно синтезують і секретують паратгормон. Після 6-7- річного віку появляються більш темні оксифільні клітини, які розцінюють як ознаку інволюції головних клітин. Концентрація паратгормону в крові в цей час становить в середньому 0,3-0,8 нг/мл.
Кількість оксифільних клітин до 10 років значно збільшується. До 12 років в паренхімі залози з'являється жирова тканина, яку розглядають як подальший прояв інволюції цих залоз.
Фізіологічне значення паратгормону полягає в тому, що він стимулює реабсорбцію кальцію в дистальних канальцях нирок, інгібує реабсорбцію фосфату в проксимальних і дистальних канальцях нирок, викликаючи фосфатурію і знижуючи к о н ц е н т р а ц і ю фосфору в крові . Крім того, паратгормон стимулює процес гідроксилювання неактивного вітаміну Б в його активний метаболіт Б3 (1,25-дигідроксикальциферол), що призводить до підсилення всмоктування кальцію в кишечнику. Паратгормон стимулює кількість остеокластів, а потім сприяє збільшенню кількості остеобластів, які є кісткоутворюючими клітинами.
Механізм дії паратгормону на організм обумовлює клінічну симптоматику, яка спостерігається при гіперабо гіпофункції паращитовидних залоз.
Гіпофіз в системі ендокринних залоз посідає особливе місце і його називають головною ендокринною залозою, оскільки він виробляє тропні гормони, які мають стимулюючий вплив на інші залози внутрішньої секреції.
Гіпофіз розташований в так званому турецькому сідлі, що представляє собою кісткове заглиблення у підвалині черепа. Тонкою ніжкою гіпофіз зв'язаний з гіпоталамусом.
Гіпофіз закладається на 4-му тижні внутрішньоутробного життя з двох окремих зачатків: ектодермального епітелію, з якого формуються передня (аденогіпофіз) і середня частки, а з другого зачатка — виросту проміжного мозку — утворюється задня частка (нейрогіпофіз).
Починає функціонувати гіпофіз дуже рано, і на 9-10-му тижні внутрішньо утробного життя виявляється синтез адренокортикотропного гормону (АКТГ; рис. 46).
Передня частка гіпофізу, що становить 75% усієї маси залози, складається з еозинофільних, базофільних і хромофобних клітин. У новонароджених в передній частці переважають базофільні гранулоцити, які дуже часто дегранульовані, що вказує на їх високу функціональну активність. Клітини передньої частки гіпофізу виробляють і виділяють в кров шість гормонів: АКТГ, соматотропний (СТГ), тиреотропний (ТТГ) і три гонадотропних фолікулостимулюючий, лютеїнизуючий, лактогеннийі Виділення СТҐ пов'язують з функцією еозинофільних, а гонадотропних гормонів базофільних клітин.
200
