
- •Лекция по теме: «Защита металлов от коррозии» Учебные вопросы
- •1. Коррозия в естественных условиях
- •Основные способы защиты металлов от коррозии
- •Механизм реакции имеет сложный характер. Электродная реакция протекает в несколько стадий. Наряду с образование оксида происходит его частичное растворение в кислоте:
- •3. Электрохимическая защита
Лекция по теме: «Защита металлов от коррозии» Учебные вопросы
Коррозия в естественных условиях
Основные способы защиты металлов от коррозии
Электрохимическая защита
1. Коррозия в естественных условиях
К данному виду коррозии относится атмосферная, подземная и морская. Атмосферная коррозия – это разрушение поверхности металлов во влажных средах при температуре окружающей среды. Атмосферная коррозия протекает, в основном, с кислородной деполяризацией. В условиях промышленной атмосферы (загрязненной CO2, SO2, NO2 HCl и др.) она может протекать и с водородной деполяризацией.
Коррозионное разрушение металлических конструкций в почвах и грунтах называют подземной коррозией. Ей подвержены различные трубопроводы, кабели, опоры и др. Почва и грунты представляют одну из наиболее сложных по химическому составу и структуре коррозионных сред. К характеристикам почв и грунта относятся влажность, пористость, кислотность, солевой состав и др. Поры занимают электролиты, содержащие минеральные соли и растворенные газы (O2, CO2, N2). Для подземной коррозии характерны язвенные и точечные разрушения. Пористые грунты агрессивнее глинистых, так как легко аэрируются и сохраняют влагу в течение длительного времени. Повышение влажности грунтов до 20 % уменьшает сопротивление, а следовательно, способствует увеличение скорости коррозии.
Максимальные
значения наблюдаются при влажности
15…25 %. Дальнейшее увеличение влажности
затрудняет доступ кислорода. На скорость
коррозии влияет и рН почвы. Особенно
велика коррозия в торфяных и болотистых
грунтах, имеющих рН![]() 3,
в которых она протекает с водородной
деполяризацией. Как правило, скорость
коррозии возрастает с увеличением
глубины залегания металлических
конструкций и разрушению подвергаются
те участки, к которым затруднен доступ
кислорода (рис. 7.). Борьбу с подземной
коррозией осуществляют либо нанесением
защитных и изолирующих покрытий, либо
электрохимической (катодной, протекторной)
защитой.
3,
в которых она протекает с водородной
деполяризацией. Как правило, скорость
коррозии возрастает с увеличением
глубины залегания металлических
конструкций и разрушению подвергаются
те участки, к которым затруднен доступ
кислорода (рис. 7.). Борьбу с подземной
коррозией осуществляют либо нанесением
защитных и изолирующих покрытий, либо
электрохимической (катодной, протекторной)
защитой.
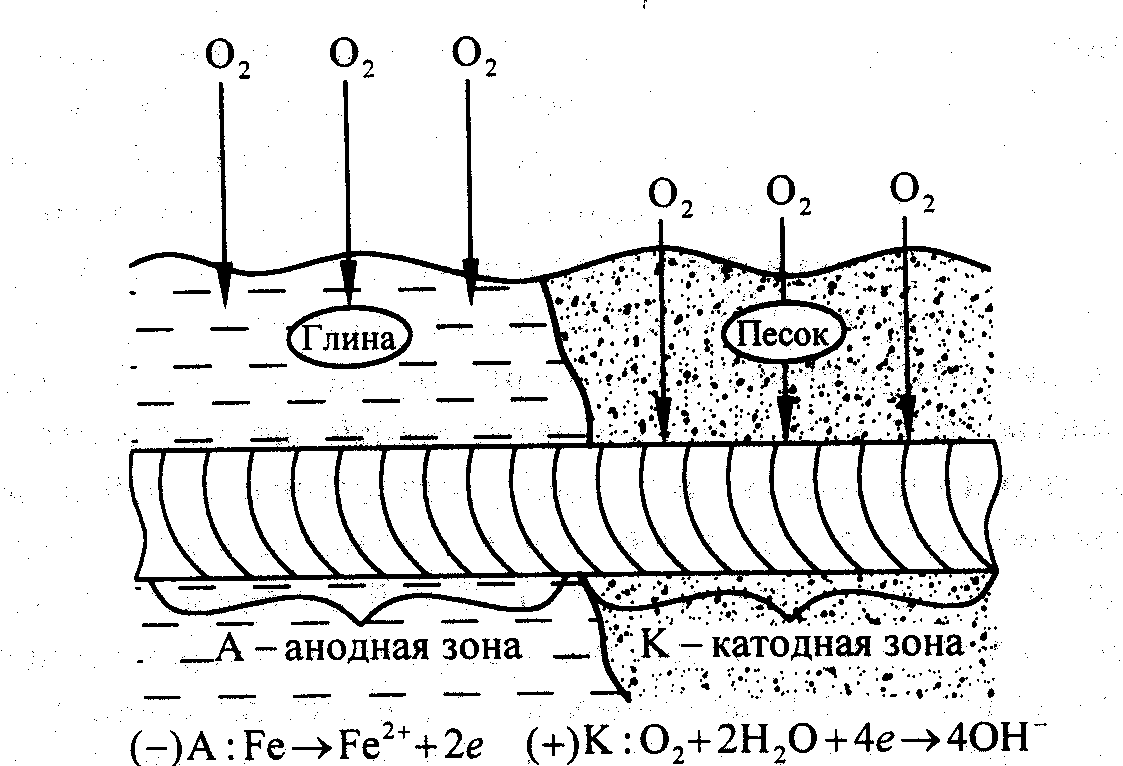
Рис. 1. Схема подземной коррозии при неравномерной аэрации почвы различной пористости.
Коррозия
в морской воде.
Морская вода обладает хорошей электрической
проводимостью из-за содержания в ней
растворенных солей и газов; рН морской
воды изменяется в пределах 7,2…8,6.
Концентрация растворенного кислорода
достигает до 8 мг/л. В ней содержится
большое количество микроорганизмов,
способствующих ускорению коррозии.
Наиболее опасным является то, что морская
вода содержит значительное количество
Cl-
-
ионов, являющихся ионами-активаторами,
препятствующими образованию пассивных
пленок на поверхности металла. Коррозия
на аэрируемых участках протекает с
поглощением кислорода на катодных
участках (2Н2О
+ О2
+
4![]()
![]() 4ОН-),
а на деаэрированных - с водородной
деполяризацией (2Н2О
+ 2
4ОН-),
а на деаэрированных - с водородной
деполяризацией (2Н2О
+ 2![]()
![]() Н2
Н2![]() +
2 ОН-).
Коррозия в морской воде наиболее
интенсивно развивается в зоне,
располагающейся выше ватерлинии, где
происходит периодическое смачивание
поверхности металла.
+
2 ОН-).
Коррозия в морской воде наиболее
интенсивно развивается в зоне,
располагающейся выше ватерлинии, где
происходит периодическое смачивание
поверхности металла.
Для защиты корпусов морских судов применяют лакокрасочные покрытия на виниловой, фенолформальдегидной, каменноугольной и битумной основах. Подводную часть судов защищают специальными покрытиями, в состав которых входят токсичные для микроорганизмов вещества (CuO, HgO и др. соединения). Для борьбы с морской коррозией используют также протекторную и катодную защиты.
Защита от коррозии – это комплекс мер, закладывающихся на стадии конструирования, осуществляемых в процессе изготовления и проводимых в ходе эксплуатации различных конструкций. В связи с этим защиту можно осуществить путем воздействия либо на материал, либо на конструкцию, либо на коррозионную среду.
