
- •Введение в обмен веществ
- •Основные особенности разных фаз метаболизма
- •Глава I. Энергетический обмен
- •1.1. Свободная энергия и законы термодинамики
- •1.1. Макроэргические соединения
- •Стандартная свободная энергия гидролиза органических фосфатов
- •1.1.2. Пути синтеза атф и его роль
- •1.1.3. Окислительно – восстановительное равновесие, окислительно –восстановительный потенциал
- •Стандартные потенциалы некоторых окислительно- восстановительных систем
- •1.2. Биологическое окисление
- •1.2.1. Характеристика биологического окисления
- •Строение комплексов полиферментного ансамбля дыхательной цепи митохондрий
- •1.2.2. Сопряжение биологического окисления и окислительного фосфорилирования
- •1.2.3. Регуляция скорости дыхания митохондрий
- •1.2.4. Разобщение дыхания и фосфорилирования
- •Краткая характеристика некоторых ионо(протоно)форов
- •1.2.5. Патология биоэнергетических процессов
- •II. Наследственные и приобретенные дефекты в работе промежуточных переносчиков этц:
- •III. Недостаток кислорода (гипоксия):
- •IV. Наличие разобщителей биологического окисления и фосфорилирования.
- •1.2.6. Механизмы защиты от токсического действия кислорода
- •А) Антиоксиданты ферментативной природы
- •Б) Антиоксиданты неферментативной природы
- •Роль катионов металлов с переменной валентностью в свободно-радикальных реакциях
- •В) Антиоксиданты внеклеточных жидкостей
- •1.3. Микросомальное окисление
- •Глава II
- •2.1.2. Регуляция процесса окисления пирувата
- •2.1.3. Патология декарбоксилирования пирувата
- •2.2. Цикл трикарбоновых кислот
- •2.2.1. Последовательность реакций цтк
- •2.2.2. Энергетическая ценность процесса
- •Образование макроэргических соединений в цтк
- •2.2.3. Участие витаминов в цтк
- •2.2.4. Биологические функции цикла Кребса
- •2.2.5. Регуляция превращений цитрата
1.1.2. Пути синтеза атф и его роль
Как видно из рис. 1, в живых клетках главным высокоэнергетическим продуктом служит аденозинтрифосфат, который обеспечивает передачу свободной энергии от экзэргонических процессов к эндэргоническим.
АТФ - это мононуклеотид, содержащий аденин, рибозу и три остатка фосфорной кислоты. В реакциях, протекающих внутри клетки, это соединение участвует в виде Mg2+-комплекса (рис.4).
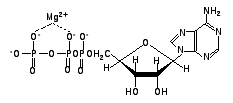
Рис. 4. Магниевая соль АТФ
Данное вещество лабильно, средняя продолжительность его существования не превышает 1 минуты.
В настоящее время известны три пути синтеза АТФ.
I. Окислительное фосфорилирование. Это наиболее важный в количественном отношении источник АТФ у аэробных организмов. Свободная энергия, необходимая для образования макроэргической связи АТФ, генерируется в дыхательной цепи. Схематически это можно выразить следующим образом:
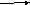 nАДФ
+ nФн
+ Ебио.ок.
nАТФ,
где n=2
или 3.
nАДФ
+ nФн
+ Ебио.ок.
nАТФ,
где n=2
или 3.
Процесс синтеза АТФ из АДФ и Фн с использованием энергии биологического окисления и называется окислительным фосфорилированием (рис. 11, стр. 25).
I I.
Субстратное фосфорилирование
– синтез АТФ при взаимодействии
АДФ и другого макроэрга (субстрата:
S~Ф):
S~Ф
+ АДФ S
+ АТФ.
I.
Субстратное фосфорилирование
– синтез АТФ при взаимодействии
АДФ и другого макроэрга (субстрата:
S~Ф):
S~Ф
+ АДФ S
+ АТФ.

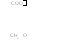
С
ОН
+
3-фосфоглицерат
АДФ
+
СООН
СН2
О
АДФ
Фосфоглицераткиназа
Mg2+ Н
С ОН
Фосфоенолпируват
Енолпируват
Пируваткиназа
АТФ
СН2 2) 1)
АТФ
















1,3-дифосфоглицерат
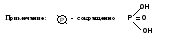
Процесс катализируется соответствующими киназами. Основными источниками АТФ в этих случаях являются макроэрги, свободная энергия которых превышает подобный показатель АТФ.
В этом процессе синтезируется не так много молекул АТФ, как в окислительном фосфорилировании, но зато он не угнетается в условиях гипоксии, так как не сопряжен с биологическим окислением и не зависит от наличия О2.
I II.Трансфосфорилирование
(«путь спасения») - синтез АТФ из
двух молекул АДФ: АДФ
+ АДФ Аденилаткиназа
АТФ + АМФ.
II.Трансфосфорилирование
(«путь спасения») - синтез АТФ из
двух молекул АДФ: АДФ
+ АДФ Аденилаткиназа
АТФ + АМФ.
Подобный механизм включается в энергооборот, когда в клетке исчерпаны возможности первых двух. В результате трансфосфорилирования повышается концентрация АМФ, что служит аллостерическим сигналом к повышению скорости катаболических реакций, приводящих, в свою очередь, к росту генерации АТФ.
1.1.3. Окислительно – восстановительное равновесие, окислительно –восстановительный потенциал
О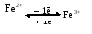 кисление
определяется как удаление электронов
или протонов, авосстановление
- как их присоединение.
кисление
определяется как удаление электронов
или протонов, авосстановление
- как их присоединение.
Например:
Отсюда следует, что окисление всегда сопровождается восстановлением акцептора электронов. Изменение свободной энергии, характеризующее реакции окисления и восстановления, пропорционально способности реагентов отдавать или принимать электроны. Отсюда, еще один параметр может служить характеристикой окислительно-восстановительного процесса – редокс (окислительно- восстановительный) потенциал (Е0). В таблице 3 приведены величины этих показателей некоторых систем, имеющих особое значение в жизнедеятельности организма.
Таблица 3
