
Раздел 2
Физико-химические процессы,
происходящие в пищевых продуктах при технологической обработке
2.1. Изменение свойств белков
в процессе технологической обработки пищевых продуктов
Белки - наиболее сложная и биологически важная состав-ная часть пищевых продуктов. Они являются неустойчивыми вы-сокомолекулярными азотистыми веществами, состоящими из аминокислот. Согласно научной теории структура белка обу-словлена первичной - основной (пептидной -СО-NH-), вторич-ной, третичной и четвертичной связями. Полипептидная цепочка как бы закручивается по спирали и возникает спиралевидная структура белковой молекулы (называется вторичной структу-рой, или α-структурой, в которой на каждые три оборота прихо-дится одиннадцать аминокислот). Стабильность этой структуры обусловлена наличием водородных связей (-О-Н) между амино-кислотным остатком и группой (-СО-NH-) одной и той же цепи. В молекуле белка, кроме пептидных, имеется еще один вид кова-лентных связей - дисульфидные (-S-S-), которые либо скрепля-ют между собой отдельные полипептидные цепочки, либо стяги-вают одну и ту же полипептидную цепочку.
Установлено, что свойства белков во многом зависят от вторичной и третичной структуры, а эти структуры - от порядка и характера чередования аминокислот. Вторичная и третичная структуры определяют специфический характер белковой моле-кулы - видовую специфичность (первоначальную, нативную).
По форме макромолекулы белков делятся на глобулярные и фибриллярные; по свойствам - на простые и сложные; по спо-собности растворяться - на растворимые и нерастворимые.
Свойства белков. Растворимость и осаждаемость белков связана с гидратационной способностью, т.е. они способны по-
21
глощать и сравнительно прочно удерживать достаточно много воды. Для белковых веществ характерны три основные связи с во-дой: адсорбционная, осмотическая и механическая. Молекулы нативного белка содержат на своей поверхности полярные груп-пы; молекулы воды также обладают полярностью, их можно представить в виде диполей, имеющих на концах заряды, равные по величине, но разные по знаку (+, -). При контакте белка с во-дой диполи воды (диссоциируют ионы Н-О-Н) адсорбируются поверхностью белковой молекулы, ориентируясь вокруг поляр-ных групп, поэтому их называют гидрофильными.
На поверхности белковой молекулы постоянно имеются два вида полярных групп: свободные и связанные. Свободные полярные группы (аминогруппы диаминокислот, карбоксильные группы дикарбоновых кислот, концевые группы полипептидных цепей) диссоциируют в растворе, определяя ве-личину суммарного заряда белковой молекулы. Адсорбирование воды ионизированными свободными полярными группами назы-вают ионной адсорбцией.
Связанные полярные группы (пептидные группы главных полярных цепей, гидроксильные, сульфогидрильные и амидные) не диссоциируют в растворе, а присоединяют молекулы воды за счет так называемой молярной адсорбции. Величина молярной адсорбции воды постоянна для каждого вида белка, величина ионной адсорбции изменяется с изменением реакции среды и степени диссоциации молекулы белка. Таким образом, основ-ная часть воды (более или менее прочно связанная белками) яв-ляется адсорбционной.
Адсорбционная вода удерживается белками за счет образо-вания (между молекулами белка и водой) водородных связей (между атомом водорода одной молекулы и атомом кислорода другой). Водородные связи относятся к разряду слабых, однако это свойство компенсируется количеством связей: каждая моле-кула воды способна образовывать четыре водородных связи, ко-торые распределяются между полярными группами белка и со-седними молекулами воды (-О- -Н-О-Н- -О-). В результате этого адсорбционная вода оказывается в белке прочно связанной. Она не отделяется от белков самопроизвольно и не может слу-жить растворителем для других веществ.
22
Растворение белков связано с гидратацией молекулы белка (образование водных оболочек из ориентированных молярных связей). Одни белки легко растворяются в воде, другие - в рас-творах солей, водно-спиртовых, водно-кислотных и водно-ще-лочных смесях. Неодинаковое отношение белков к различным растворителям используется для их разделения. Нейтральные со-ли в зависимости от концентрации оказывают двоякое и взаимо-противоположное действие на растворимость белков: малые кон-центрации увеличивают растворимость белков, а большие - оса-ждают белки из растворов (происходит «высаливание» белков).
В изоэлектрической точке, когда заряд белковой молекулы близок к нулю, способность белка связывать воду наименьшая. Белки в изоэлектрической точке проявляют ряд особенностей: может меняться форма белковой молекулы, обнаруживается склонность к агрегации (образование мицелл), выпадению белка в осадок. Сдвиг pH среды в ту или иную сторону от изоэлектри-ческой точки приводит к усилению диссоциации основных или кислотных групп белка, увеличению заряда белковых молекул и улучшению гидратации белка.
В технологических процессах эти свойства белков исполь-зуются для увеличения водосвязывающей способности. Физико-химические и коллоидные состояния белков в пище-вых продуктах. Белки характеризуются амфотерными свойства-ми. По своим свойствам белки - гидрофильные коллоиды, при определенных условиях способные давать золи, гели, студни. Способность белка образовывать гель в большей степени обу-словлена конфигурацией его белковых молекул, а концентрация белка в системе имеет второстепенное значение.
Растворы белков обладают рядом свойств, характерных для лиофильных коллоидных растворов. Наличие на поверхности белков многочисленных полярных групп обусловливает их зна-чительную гидратацию. В определенных условиях белки образу-ют гели (студни). Частицами дисперсных фаз в коллоидных сис-темах являются мицеллы.
Белковые золи - это жидкие коллоидные системы, содер-жащие частицы дисперсной фазы (мицеллы) размером от 10-5 до 10-7м. Мицеллы любого гидрофильного коллоида состоят из ди-польных молекул, т.е. молекул, имеющих полярные группы
23
(-ОН, -СООН, -NH2, S-S) и гидрофобных групп - углеводород-ный радикал (-СН). Полярные группы имеют сродство к воде и расположены на поверхности мицелл, последние способны удерживать молекулы воды, образующей вокруг сольватную оболочку.
В студне молекулы белка с помощью межмолекулярных связей разной природы образуют пространственную сетку, в ячей-ках которой удерживается вполне определенное для данного бел-ка количество воды (гель). Способность белка образовывать студень обусловлена конфигурацией его белковых молекул. Чем больше асимметрия молекул белка (отношение длины к толщине или диаметру), тем меньше концентрация белка необходима для образования студня. Вода в ячейках пространственной сетки студня участвует в образовании структуры, приближающейся к структуре твердого тела. Студни способны сохранять форму, механическую прочность, упругость, пластичность.
В пищевых продуктах белки содержатся в разных концен-трациях и в различных коллоидных состояниях: золей и гелей. Белковый золь - коллоидный раствор, содержащий в каче-стве дисперсной фазы агрегаты молекул белка. Золи могут быть различной концентрации: малоконцетрированный (0,1-4,0%), концентрированный (8-25%) (например, белки молока и яйца). Белковый гель - структурированная система, образованная молекулами полимеров белка с межмолекулярными силами сцеп-ления: обводненные гели - белки миофибрилл мышечного во-локна мяса, простокваши, теста; высохших гелей (ксерогелей) -зерно, мука, крупа, бобовые.
Глубина физико-химических изменений белковых веществ при технологической обработке продуктов определяется их при-родными свойствами, коллоидным состоянием и характером внешних воздействий.
Наиболее значительные изменения белков связаны с гидра-тацией, дегидратацией, денатурацией и деструкцией. Гидратация белков. Процесс гидратации белков состоит из накладывающихся один на другой процессов растворения и на-бухания их с образованием студней. В белковых растворах не-большой концентрации (молока) молекулы белка полностью гид-ратированы в виду наличия избыточного количества воды. В кон-
24
центрированных растворах белковых золей (яйца) и обводненных гелей (мышечные волокна мяса) при добавлении воды происхо-дит дополнительная их гидратация в известных пределах и уве-личивается водосвязывающая способность (при изготовлении котлет, кнелей и других изделий из измельченного мяса). При до-бавлении молока к смеси яйца и последующей тепловой обработ-ке образуется гель, удерживающий всю воду в коллоидной сис-теме. Эффективность дополнительной гидратации в случае при-веденных примеров состоит в улучшении реологических показа-телей геля - снижение его механической прочности, повышение пластичности, нежности и сочности продукции.
Белки высохших гелей находятся в состоянии высохшей протоплазмы и алейроновых зерен и при контакте с водой набу-хают, образуя более или менее обводненный сплошной гель (при приготовлении теста, замачивании круп и бобовых и варке круп и бобовых - в начале варки). При этом происходит набухание белков с образованием структурированной коллоидной системы, удерживающей определенное количество воды (классическим примером гидратации такого типа является приготовление теста из муки - белки муки набухают, образуя клейковину). В этом случае набухание при избытке воды не переходит в процесс рас-творения.
Белки, находящиеся в продуктах в состоянии обводненных гелей, в ряде случаев способны к дополнительной гидратации. Молекулы белка в гелях с помощью межмолекулярных связей разной природы образуют пространственную сетку, в ячейках ко-торой удерживается большое количество воды, строго опреде-ленное для данного вида белка. Поэтому белковые гели большин-ства продуктов и полуфабрикатов более обводнены по сравнению с концентрированными растворами. Например, в мышечных во-локнах мяса теплокровных животных миофибриллы содержат 15-20% белка (гель), а саркоплазма - 25-30% белка (золь).
При оценке роли гидратационных процессов необходимо иметь в виду, что в продуктах, наряду с адсорбционной водой, связанной белками, содержится большее или меньшее количество осмотически и капиллярно связанной воды.
При перемешивании и взбивании компонентов (например, фаршевых изделий) вследствие гидратации белков (накладываю-
25
щихся процессов растворения и набухания) повышается липкость массы, изделия хорошо формуются, увеличивается водосвязы-вающаяся способность изделия. От степени гидратации в значи-тельной мере зависят такие важнейшие органолептические пока-затели качества готовой продукции, как нежность, сочность кон-систенции, вкус.
Дегидратация белков сопровождается потерей белками свя-занной воды под влиянием внешних воздействий. Различают об-ратимую и необратимую дегидратацию белков.
Обратимая дегидратация может являться составной частью целенаправленных технологических процессов. Например, при сублимационной сушке из продукта удаляется большая часть связанной белками воды. Высушенный продукт сохраняет свой естественный внешний вид, внутреннюю структуру и пищевую ценность.
Необратимая дегидратация белков сопровождается выделе-нием в окружающую среду воды вместе с растворимыми вещест-вами - экстрактивными, минеральными, витаминами и пр. Необ-ратимая дегидратация может происходить при замораживании, хранении, а также при тепловой обработке продуктов.
Дегидратация белков является причиной уменьшения мас-сы продукта, снижения его пищевой ценности и органолептиче-ских показателей.
Денатурация белков - это нарушение нативной простран-ственной структуры белковой молекулы под влиянием внешних факторов: высоких температур (тепловая денатурация), кислот, щелочей, дубильных веществ, ультразвука, механических воздей-ствий (поверхностная денатурация). Денатурирующий эффект внешних воздействий тем сильнее, чем выше гидратация белков и меньше их концентрация в коллоидной системе.
Денатурация сопровождается изменением важнейших свойств белка: гидратации (растворения и набухания), коллоид-ного состояния (коагуляция, свертывание), потерей биологиче-ской активности, улучшением атакуемости протеолитическими ферментами.
Сущность тепловой денатурации заключается в том, что когда молекуле белка сообщается тепловая энергия, полипептид-ные цепочки испытывают колебательное движение (чем больше
26
сообщается энергии, тем сильнее колебание), и на определенном этапе колебательные движения приводят к тому, что часть связей разрушается. В момент, когда связей разрушается столько, что оставшиеся не могут удержать белковую молекулу в прежнем со-стоянии, изменяется ее форма (способ укладки в пространстве). Эти изменения происходят на молекулярном уровне.
Скорость и степень тепловой денатурации белков находят-ся в прямо пропорциональной зависимости от температуры, про-должительности нагревания и pH среды.
Следствием тепловой денатурации является коагуляция белков (изменение коллоидного состояния - свертывание). Коа-гуляция белков проявляется различно в зависимости от концен-трации белковых веществ и их коллоидного состояния.
В зависимости от того, в каком коллоидном состоянии на-ходятся белки в пищевых продуктах, по-разному изменяется их коллоидное состояние при тепловой денатурации.
Основные типы свертывания (коагуляции) белков.
1. В малоконцентрированных белковых растворах при теп-ловой денатурации агрегация молекул белка происходит за счет образования межмолекулярных связей как прочных (например, дисульфидных), так и слабых (многочисленных - водородных). В результате образуются частицы более крупных размеров. Даль-нейшая агрегация частиц приводит к расслоению коллоидной системы, образованию хлопьев белка, выпадающих в осадок или всплывающих на поверхности жидкости, часто с образованием пены. Концентрация белков в таких растворах не превышает 1,0%.
2. В более концентрированных белковых растворах при де-натурации белков образуется сплошной гель, удерживающий всю воду, содержащуюся в коллоидной системе. В результате агрега-ции денатурированных молекул белка образуется структуриро-ванная белковая система. Точные концентрации белков, при ко-торых их растворы при нагревании образуют сплошной гель, не-известны. Учитывая, что способность к гелеобразованию белков зависит от конфигурации (ассиметрии) молекул и характера об-разующихся при этом межмолекулярных связей, следует пола-гать, что для белков различной концентрации к способности ге-леобразования различны.
27
3. Белки, представляющие собой более или менее обвод-ненные гели, при тепловой денатурации уплотняются, происхо-дит их дегидратация с отделением жидкости в окружающую сре-ду. Белковый гель после нагревания характеризуется уменьшени-ем объема, массы, пластичности, повышением механической прочности и большей упругостью по сравнению с исходным ге-лем нативного белка.
В фибриллярных белках (коллаген) тепловая денатурация вызывает изменения другого характера и приводит к:
1) сокращению в длину вытянутых аминокислотных цепо-чек за счет разрыва внутренних связей (сваривания), при этом длина их сокращается примерно на 1/3 от первоначальной;
2) распаду фибрилл (волокон) на отдельные цепочки ами-нокислот (дезагрегация - распад больших молекулярных агрега-тов - плавление), так как в результате разрушения большого чис-ла поперечных связей между полипептидными цепями фибрил-лярная структура исчезает, коллагеновые волокна превращаются в сплошную стекловидную массу - глютин.
Таким образом, тепловая денатурация оказывает большое влияние на показатели качества готовой продукции: глобулярные белки в зависимости от изменения коллоидного состояния удер-живают воду, образуя нежный гель (лиогель), или уплотняются, отделяя воду, образуют плотный гель (каогель); фибриллярные белки, разрушаясь, превращаются в глютин.
Деструкция белков. При тепловой обработке продуктов из-менение белков не ограничивается только денатурацией. Доведе-ние продукта до полной кулинарной готовности вызывает необ-ходимости нагревать денатурированные белки при температурах, близких к 100ºС, более или менее продолжительное время. В этих условиях белки подвергаются дальнейшим изменениям, связан-ным с разрушением их макромолекул. Вследствие таких измене-ний от белковой молекулы могут отщепляться функциональные группы с образованием таких летучих веществ, как аммиак (NH3), сероводород (H2S), фосфористый водород (РН3), углекислый газ (СО2), сернистый газ (SО2) и др. Накапливаясь в продукте и ок-ружающей среде, эти вещества участвуют в образовании вкуса и запаха готовой продукции. Так, при длительной варке яиц (вкрутую) вследствие разрушения S-содержащих аминокислот
28
(цистина, метионина) отщепляется сера (S) и образуется серово-дород (H2S), который при соприкосновении с железом (Fe) желт-ка образует новое соединение - сернистое железо (FeS) - соеди-нение сине-зеленого цвета, сконцентрированное на поверхности желтка. Этот процесс не только ухудшает внешний вид, но и зна-чительно снижает пищевую (биологическую) ценность.
Примером деструкции фибриллярных белков является пре-вращение коллагена в глютин.
Таким образом, основные изменения, происходящие в бел-ках в процессе тепловой обработки продуктов, можно предста-вить следующей схемой: белки глобулярные → гидратация → де-гидратация → денатурация → коагуляция (выпадение хлопьев, образование геля, уплотнение геля) → деструкция (образование NH3, H2S, SО2, СО2); белки фибриллярные → денатурация → сва-ривание, дезагрегация → деструкция (глютин).
Вопросы для самоподготовки
1. В каких концентрациях и коллоидных состояниях нахо-дятся белки в пищевых продуктах?
2. Какие факторы внешней среды вызывают гидратацию, дегидратацию, денатурацию белков? В чем сущность этих изме-нений? Как изменяются при этом свойства белков и их коллоид-ное состояние?
3. Как изменяется денатурированный белок при длитель-ном действии денатурирующего фактора?
4. В чем сущность деструкции белков при тепловой и ме-ханической денатурации?
5. Какое влияние физико-химические изменения белков при тепловом и механическом воздействии оказывают на качест-во продукции?
29
Работа 1
Типы коагуляции глобулярных белков
Коагуляция белков в пищевых продуктах в зависимости от их содержания и коллоидного состояния может быть следующей:
1) в малоконцентрированных белковых растворах денату-рированные белки образуют гель (хлопья свернувшихся белков овощей, мясных и рыбных бульонов и пр.);
2) в концентрированных белковых растворах денатуриро-ванные белки образуют сплошную студнеобразную массу - гель (уплотнение белков миофибрилл мышечного волокна мяса, рыбы, яйца при варке и пр.);
3) в обводненных белковых гелях денатурация приводит к уплотнению геля и выделению содержащейся в нем жидкости (уплотнение белков миофибрилл мышечного волокна мяса, рыбы при варке, при получении творога из простокваши, а также варке круп, бобовых, выпечке изделий из теста).
Для демонстрации различных типов коагуляции белков мож-но использовать сырое куриное яйцо, простоквашу и мясной сок. Цель работы - показать типы коагуляции глобулярных белков при тепловой денатурации в зависимости от их коллоид-ного состояния и концентрации.
Оборудование, посуда. Четыре химических стакана емко-стью 150 см3; четыре пробирки диаметром 2 см; четыре термо-метра на 100°С; четыре стеклянные палочки, пипетки емко-стью10 см3.
Техника выполнения работы. Сырое куриное яйцо разбить и отделить белок от желтка. В стакан внести 10 см3 белка и 90 cм3 дистиллированной воды, перемешать.
В пробирки внести по 5 см3 мясного сока, простокваши, белка натурального и разведенного водой, опустить в них термо-метры.
В стаканы емкостью 150 см3 налить 50 см3 воды, опустить в воду пробирки с белковыми продуктами и, нагревая стаканы с пробирками, отметить: температуру, при которой происходит начало коагуляции белков; полное загустение и уплотнение сгу-стка с выделением жидкости, образованием хлопьев.
30
Воду в стаканах довести до кипения, кипятить 2 мин, затем пробирки вынуть и дать оценку внешнего вида гелей белков. Данные наблюдений свести в табл. 1.
Таблица 1
Типы коагуляции белков
Показатель
Мясной
Яйцо Простокваша разведенное
сок натуральное
водой
Примерная концентрация, %
Исходное коллоидное состояние белков
Температура начала коагуляции, °С Температура полной коагуляции, °С Вид белковых гелей после кипячения
Полученные данные проанализировать и сделать выводы. Порядок выполнения работы следует отразить в виде схемы экс-перимента в рабочей тетради (см. приложение)1.
Работа 2
Изменение растворимости белков растительного происхождения при тепловой обработке продуктов
Растворимость белков зависит, главным образом, от вели-чины заряда и групп атомов, которые образуют поверхность мак-ромолекул, и в особенности - от распределения свободных и свя-занных полярных групп между поверхностью и внутренней ча-стью белковых частиц. При тепловой обработке вследствие разры-ва непрочных связей (водородных, гидрофобных) изменяется рас-положение полипептидных цепей в макромолекуле белка, а также ориентация групп, вследствие чего сродство к воде белковой мо-лекулы уменьшается, что можно обнаружить по снижению рас-творимости.
1 Все последующие работы следует также оформлять в виде схемы экс-перимента в рабочей тетради.
31

















Цель работы - показать влияние тепловой обработки на растворимость белков растительного происхождения. Оборудование, приборы, посуда. Весы технические; аппарат для встряхивания; центрифуга; рефрактометр; две выпаритель-ные чашки; две конические колбы емкостью 250 см3; мерный ци-линдр емкостью 100 см3; часы песочные на 5 мин; восемь цен-трифужных пробирок; две мерные колбы емкостью 100 см3; две градуированные пробирки; пипетки емкостью 2 см3, 5 см3; палоч-ки стеклянные.
Реактивы. 7%-ный раствор поваренной соли; 20%-ный рас-твор сульфосалициловой кислоты (или 40%-ный трихлоруксус-ной); 30%-ный раствор едкого натра; 2%-ный раствор сернокис-лой меди.
Техника выполнения работы. На технических весах отве-сить в две выпарительные чашки по 15 г муки. Одну навеску про-греть в сушильном шкафу при 160ºС в течение 40 мин для дена-турации белков.
Навески непрогретой и прогретой муки перенести в колбы емкостью 250 см3 и залить десятикратным количеством 7%-ного раствора поваренной соли. Колбы закрыть пробками и поставить на 10 мин. в аппарат для встряхивания. После перемешивания от-центрифугировать вытяжки для осаждения крахмала в течение
5 мин при скорости 1000 об./мин.
Центрифугат из пробирок слить в мерные колбы емкостью 100 см3. Колбы довести до метки дистиллированной водой, за-крыть пробками и перемешать содержимое.
Об изменении растворимости белков в процессе тепловой обработки можно судить по объему осадка, образованного при осаждении его 20%-ной сульфосалициловой кислотой (40%-ной трихлоруксусной), или по интенсивности биуретовой реакции.
При использовании для осаждения белков сульфосалици-ловой кислоты в градуированные пробирки налить по 5 см3 цен-трифугата из непрогретой и прогретой муки. В каждую пробирку внести пипеткой по 2 см3 20%-ной сульфосалициловой кислоты, закрыть пробирки пробками, перемешать их содержимое и оста-вить на 20 мин. Сравнить объемы полученных осадков.
Для биуретовой реакции в две пробирки налить по 3 см3 центрифугата вытяжек из непрогретой и прогретой муки, приба-
32
вить равный объем 30%-ного раствора едкого натра и 2-3 капли 2%-ного раствора сернокислой меди. Отметить интенсивность биуретовой реакции.
Для определения коэффициента преломления центрифуга-тов из непрогретой и прогретой муки следует использовать реф-рактометр. При рефрактометрическом определении количества растворимых белков в центрифугатах условно исходят из того, что изменение коэффициентов преломления центрифугатов обу-словлено только белками.
После установки прибора на нуль одну-две капли центри-фугата нанести на призму рефрактометра и снять показания по правой шкале. Замер провести 2-3 раза и подсчитать среднее арифметическое значение.
Результаты работы представить в табл. 2. Сделать выводы по работе.
Таблица 2
Растворимость белков растительного происхождения
Объект исследования Объем осадка, см3
Интенсивность биуретовой реакции
Количество растворимых
веществ, %
Центрифугат из муки: непрогретой
прогретой при 160°С
Работа 3
Влияние температуры на растворимость мышечных белков мяса и рыбы
В зависимости от приема тепловой обработки (варки, при-пускания, жарки) мясо прогревается до разной температуры. Так, при варке внутри куска мяса в течение продолжительного време-ни поддерживается температура в пределах 94-96°С, в процессе припускания рыбы температура внутри кусков достигает 80-82°С, а при жарке мясо внутри куска имеет температуру 80°С.
Денатурационные изменения мышечных белков в разных температурных условиях протекают с неодинаковой интенсивно-
33












стью, о чем может свидетельствовать изменение их растворимо-сти.
Цель работы - показать влияние температуры нагревания на изменение растворимости белков мяса и рыбы. Приборы, оборудование, посуда. Рефрактометр; микроиз-мельчитель тканей; мясорубка; шесть пробирок емкостью 20 см3; шесть воронок; два термометра на 100°С; три водяные бани; три конические колбы емкостью 250 см3; три конические колбы ем-костью 100 см3; три стаканчика емкостью 100 см3; цилиндр емко-стью 50 см3; пипетка емкостью 5 см3; градуированная пипетка емкостью 2 см3.
Реактивы. 20%-ный раствор сульфосалициловой кислоты или 40%-ный трихлоруксусной; 30%-ный раствор едкого натра; 2%-ный раствор сернокислой меди.
Техника выполнения работы. Мясо, освобожденное от по-верхностных отложений жира и плотных соединительно-тканных образований, или филе рыбы дважды измельчить на мясорубке и тщательно перемешать.
Поместить три навески фарша по 10 г в стаканчики емко-стью 100 см3 , которые пронумеровать карандашом по стеклу. Пробу № 1 оставить в качестве контрольной. Пробы № 2 и № 3 прогреть на водяной бане в течение 10 мин при 60º и 96°С соот-ветственно. Каждую пробу прогретого фарша и контрольную из-мельчить в микроизмельчителе.
При помощи стеклянной палочки перенести каждую пробу фарша в сосуд микроизмельчителя, смывая остатки фарша 50 см3 дистиллированной воды. Сосуд установить в контейнер и укре-пить зажимным кольцом. Измельчить фарш в течение 1 мин
Затем образцы перенести в колбы емкостью 250 см3. Колбы закрыть резиновыми пробками и поставить на 10 мин в аппарат для встряхивания, чтобы полнее экстрагировать белки.
Пробы оставить на 10 мин для осаждения взвешенных час-тиц, после чего растворы белка отфильтровать через бумажный фильтр в конические колбы емкостью 100 или 50 см3.
Количество белка в фильтрате определить по рефрактомет-ру. При рефрактометрическом определении количества белка в вы-тяжках из фарша следует исходить из того, что изменение коэф-фициентов преломления вытяжек обусловлено только белками,
34
хотя из фарша в воду, кроме белков, извлекаются экстрактивные и минеральные вещества (количество двух последних при тепло-вой обработке почти одинаково).
Количество водорастворимых белков, извлеченных из об-разцов фарша, можно сравнить, используя реакцию осаждения белков сульфосалициловой кислотой.
Для реакции осаждения в градуированные пробирки налить по 5 см3 раствора белка, добавить к ним по 2 см3 20%-ной суль-фосалициловой кислоты, пробирки закрыть пробками, переме-шать содержимое и оставить на 20 мин. Отметить объемы вы-павших осадков.
Количество белка в вытяжках можно сравнить по биурето-вой реакции, для чего к 5 см3 каждого фильтрата прилить по 5 см3 30%-ного раствора едкого натра и осторожно по стенке 2-3 капли 2%-ного раствора сернокислой меди. Интенсивность окраски за-писать по результатам визуальных наблюдений.
Результаты представить в табл. 3.
Сделать выводы по работе.
Таблица 3
Растворимость мышечных белков
Интенсивность
Объект окраски
исследования биуретовой
реакции
Коэффициент Количество преломления растворимых
раствора веществ, %
Объем
осадка после осаждения,
см3
Вытяжка из фарша:
прогретого при 60ºС прогретого при 96°С
Работа 4
Выделение летучих соединений
при тепловой обработке пищевых продуктов
При тепловой обработке пищевых продуктов глобулярные белки коагулируют вследствие денатурации. Если коагулянт бел-ка продолжать нагревать, могут наступить вторичные явления, характеризующиеся отщеплением от белковой молекулы некото-рых соединений, например сероводорода, фосфористого водорода.
35










Наличие сероводорода можно определить с помощью фильт-ровальной бумаги, смоченной раствором уксуснокислого свинца. В результате взаимодействия этих соединений на фильтровальной бумаге образуется пятно сернистого свинца, окрашенное в цвет от бурого до черного в зависимости от количества выделяющегося сероводорода:
H2S + Рb(СН3СООH)2 = PbS + 2CH3COOH.
Для повышения чувствительности реакции применяют рас-твор свинцовой соли. При этом с сероводородом реагирует обра-зующийся плюмбит натрия:
Рb(СН3СОО)2 + 4NaOH = Na2РbО2 + 2СН3СООNa + 2H2O Na2PbО2 + H2S = PbS + 2NaOH.
При кулинарной обработке пищевых продуктов, в составе которых в значительных количествах содержатся фосфопротеи-ды, происходит не только денатурация последних, но и отщепле-ние фосфористого водорода вследствие денатурационных про-цессов.
Фосфористый водород (PH3), или фосфин, может взаимо-действовать с азотнокислым серебром, образуя при этом окра-шенные соединения (от желтого до красно-бурого цвета):
PH3 + AgNO3=H2AgP + HNO3
H2AgP + AgNO3 = Hag2P + HNO3 Hag2P + AgNO3=Ag3P + HNO3.
Цель работы - продемонстрировать выделение сероводо-рода и фосфористого водорода вследствие деструкции белков. Приборы, посуда. Прибор для качественного определения сероводорода, стеклянная палочка.
Реактивы. Щелочной раствор уксуснокислого свинца; 4%-ный водный раствор азотнокислого серебра. Техника выполнения работы. Качественное определение сероводорода и фосфористого водорода рекомендуется прово-дить на приборе, состоящем из штатива (1), укрепленной на нем
36
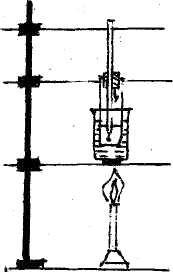
широкогорлой центрифужной пробирки (2) и химического стака-на под ней (3), выполняющего роль водяной бани (рис. 1).
2
3
1
Рис. 1. Схема прибора для качественного определения летучих соединений
Нагревание производится с помощью электроплитки. Про-бирку закрыть пробкой с отверстием для термометра и крючком из проволоки, на который подвесить две полоски фильтровальной бумаги размером 1,0×2,5 см.
В пробирку внести исследуемый сырой продукт (смесь белка и желтка куриного яйца). На один конец полоски фильтро-вальной бумаги нанести стеклянной палочкой каплю щелочного раствора уксуснокислого свинца, другим концом фильтроваль-ную бумагу подвесить на крючок. На полоску другой фильтро-вальной бумаги на один конец нанести каплю водного раствора АgNO3 и подвесить на крючок другим концом.
В химический стакан налить холодной воды. Закрыть про-бирку пробкой и укрепить на штативе так, чтобы часть пробирки, содержащая исследуемый продукт, была погружена в воду, но не касалась дна стакана. Термометр погрузить концом в продукт. Нагревание водяной бани вести с таким расчетом, чтобы повы-шение температуры исследуемого продукта составляло не более 4-5°С в минуту.
При нагревании белков куриного яйца заметить, при какой температуре начнет загустевать белок. Особое внимание следует обратить на температуру, при которой появится потемнение (сна-
37



чала в виде кольца) на смоченных концах фильтровальной бума-ги, проследить и ответить, как усиливается окраска пятен по мере нагревания.
Сделать выводы о влиянии тепловой обработки на выделе-ние летучих соединений из продуктов.
По теме «Изменения свойств белков» обобщить материал и сделать заключение.
2.2. Изменение свойств углеводов в процессе технологической обработки продуктов
Углеводы, содержащиеся в пищевых продуктах, делят на три класса: моносахариды, олигосахариды и полисахариды. Эти соединения с общей формулой СnН2nОn отличаются по молеку-лярной массе.
Изменения углеводов при технологической обработке пи-щевых продуктов весьма разнообразны. Дисахариды гидролизу-ются (кислотный и ферментативный гидролиз), превращаются в несахарные компоненты (брожение, карамелизация и меланоиди-нообразование). Технологическая обработка крахмалосодержа-щих продуктов сопровождается изменением крахмала: клейсте-ризация в процессе влажного нагрева, деструкция в условиях су-хого нагрева (декстринизация) и ферментативное расщепление крахмала, ретроградация крахмала (старение) при хранении гото-вых кулинарных изделий.
Физико-химические и биохимические изменения, происхо-дящие с углеводами в процессе технологической обработки про-дуктов, приводят к изменению функционально-технологических свойств углеводов и существенно влияют на качество готовых изделий.
Вопросы для самоподготовки
1. В каких технологических процессах производства про-дукции происходит кислотный и ферментативный гидролиз саха-ров? От каких факторов зависит интенсивность этих процессов?
2. Каковы основные стадии процессов карамелизации и ме-ланоидинообразования, в чем их аналогия? Положительные и от-
38
рицательные стороны этих процессов, оказывающих влияние на качество продукции.
3. В чем сущность процесса клейстеризации крахмала? Ка-кие факторы влияют на вязкость клейстеров?
4. Что такое «ретроградация крахмала»? Какие факторы влияют на интенсивность этого процесса и в каких случаях этот процесс имеет место?
5. В каких случаях обработки продуктов происходит про-цесс деструкции крахмала и как изменяется качество крахмало-содержащих продуктов вследствие деструкции?
6. Какие физико-химические показатели крахмала влияют на технологические свойства различных продуктов?
7. Каков коэффициент замены картофельного крахмала, используемого в качестве загустителя, другими видами (кукуруз-ным, маисовым)?
8. В каких технологических процессах производства про-дукции происходит ферментативный гидролиз крахмала?
Работа 5
Влияние различных факторов на гидролиз сахарозы
При тепловой обработке продуктов, в состав которых вхо-дит или добавляется при изготовлении кулинарных изделий саха-роза, происходит ее кислотный гидролиз с образованием инверт-ного сахара. Сахароза в водных растворах под влиянием кислот присоединяет молекулу воды и расщепляется на равные количе-ства глюкозы и фруктозы. При этом ион водорода кислоты дей-ствует как катализатор. Полученная смесь глюкозы и фруктозы вращает плоскость поляризации не вправо, как сахароза, а влево. Такое преобразование правовращающей сахарозы в левовра-щающую смесь моносахаридов называется инверсией, а эквимо-лекулярная смесь глюкозы и фруктозы - инвертным сахаром. Последний имеет более сладкий вкус, чем сахароза. Инвертный сахар образуется, например, при варке киселей, компотов, при запекании яблок с сахаром.
Количество образующегося инвертного сахара зависит от концентрации сахарозы и кислоты, степени диссоциации кисло-
39
ты, температуры и продолжительности нагревания. Различные кислоты обладают неодинаковой инверсионной способностью. Высокой инверсионной способностью обладает щавелевая кисло-та, в 10 раз меньшей - лимонная, в 15 - яблочная, в 17 - молоч-ная, в 45 раз - уксусная кислота.
Цель работы - изучить влияние различных факторов на степень инверсии сахарозы, что можно выполнить в одном из ва-риантов: продолжительности нагревания, концентрации кислоты, степени диссоциации кислоты (вида кислоты).
Приборы, оборудование, посуда. Бюретка для горячего титро-вания; термометр; три химических стакана емкостью 200-250 см3; три конические колбы емкостью 100-250 см3; часы песочные на
1 и 5 мин.; воронки; шпатель.
Реактивы. Основной реактив (щелочной раствор гексациа-ноферрата калия - 8 г К3[Fe(CN)6]+20 г NaOH или 28 г КОН на 1000 см3 раствора);
стандартный раствор глюкозы (1,6 г глюкозы + 150 г NaCl на 1 000 см3 раствора); 1%-ный водный раствор метиленового си-него; 6%-ный раствор лимонной кислоты; 6%-ный раствор ук-сусной и щавелевой кислот.
Техника выполнения роботы. При изучении влияния от-дельных факторов на инверсию сахарозы готовят сиропы по ре-цептурам, приведенным в табл. 4.
Таблица 4
Рецептуры приготовления сиропов
Номер
рецептуры
Сахар, г Кислота, см3
Дистиллированная Продолжительность
вода, см3 кипячения, мин
1 1 Лимонная - 5 40 1
2 1 Лимонная - 5 40 5
3 1 Лимонная - 10 35 5
4 1 Щавелевая - 5 40 1
5 1 Щавелевая - 5 40 5
6 1 Щавелевая -10 35 5
7 1 Уксусная - 5 40 1
8 1 Уксусная - 5 40 5
9 1 Уксусная - 10 35 5
40










Могут быть предложены другие рецептуры, вид и концен-трация кислоты и продолжительность нагревания. Для сиропа на технических весах взять навеску сахарозы в химический стакан емкостью 100 см3, налить воду, кислоту и смесь кипятить 1 или 5 мин. Общий объем сиропа должен быть одинаковым во всех стаканах. После приготовления сиропы охла-дить и количественно перенести в мерные колбы емкостью 200-250 см3. Содержимое колб довести до метки дистиллированной водой, перемешать и использовать для определения сахара циа-нидным методом. При большой концентрации инвертного сахара, обнаруженной при титровании, следует сделать разведение. Сущность метода заключается в восстановлении избыточ-ного феррицианида калия стандартным раствором глюкозы или инвертного сахара в присутствии индикатора метиленового сине-го до полного обесцвечивания,
при этом железосинеродистый калий (красная кровяная соль) восстанавливается в железистосинеродистый калий (желтая кровяная соль) при нагревании в щелочной среде по уравнению:
C6H12O6 + 6K3 [Fe(CN)6] + 6KON =
=6K4 [Fe(CN)6] + (CHOH)4 × (COOH)2 + 4H2O.
Практически этот метод осуществляется путем титрования с применением в качестве индикатора раствора метиленового си-него. Метиленовый синий в щелочной среде переводится избыт-ком редуцирующего сахара в бесцветное лейкооснование; в связи с этим синий цвет раствора исчезает, как только появляется из-быточная капля стандартного раствора глюкозы, что указывает на конец реакции. Впоследствии раствор окрашивается в желтый цвет благодаря присутствию желтой кровяной соли. При остыва-нии раствора вновь появляется фиолетовое окрашивание, так как лейкооснование легко окисляется кислородом воздуха.
При проведении анализа в коническую колбу вносят 10 см3 сиропа и 25 см3 основного реактива (щелочной раствор гексациа-ноферрата калия). Содержимое колбы нагревают до кипения за
3 мин, кипятят 1 мин, вносят три капли раствора метиленового синего и титруют стандартным раствором глюкозы до исчезнове-ния синей окраски. Содержание глюкозы Х в процентах вычис-ляют по формуле
41
X =
1,6(n − m)⋅V ⋅100
1
V ⋅ q
2
, (1)
где n - количество стандартного раствора глюкозы, пошедшее на титрование 25 см3 щелочного раствора гексацианоферрата калия при холостом опыте, см3; m - количество стандартного раствора глюкозы, пошедшее на дотитрование, см3; 1,6 - количество глю-козы в 1см3, мг; V1 - объем мерной колбы, использованной для приготовления водной вытяжки, см3; V2 - объем водной вытяжки, взятой для анализа, см3; q - масса навески объекта исследования, мг.
Практически этот метод осуществляется путем титрования с применением в качестве индикатора раствора метиленового си-него. Метиленовый синий в щелочной среде переводится избыт-ком редуцирующего сахара в бесцветное лейкооснование; в связи с этим синий цвет раствора исчезает, как только появляется из-быточная капля стандартного раствора глюкозы, что указывает на конец реакции. Впоследствии раствор окрашивается в желтый цвет благодаря присутствию желтой кровяной соли. При остыва-нии раствора вновь появляется фиолетовое окрашивание, так как лейкооснование легко окисляется кислородом воздуха.
При проведении анализа в коническую колбу вносят 10 см3 сиропа и 25 см3 основного реактива (щелочной раствор гексациа-ноферрата калия). Содержимое колбы нагревают до кипения за
3 мин, кипятят 1 мин, вносят три капли раствора метиленового синего и титруют стандартным раствором глюкозы до исчезнове-ния синей окраски. Содержание глюкозы Х в процентах вычис-ляют по формуле
П = 10 + V, (2)
где 10 + V - объем стандартного раствора глюкозы, см3.
Результаты исследований свести в табл. 5.
Таблица 5
Влияние различных факторов на гидролиз сахарозы


Рецептура сиропа
Продолжительность
кипячения,
мин
Кислота,
добавляемая в сироп
Концентрация
кислоты,
%
Количество инвертного
сахара, %
…………..……
…………..……
Сделать выводы о влиянии продолжительности нагревания, концентрации и вида (степени диссоциации) кислоты на степень инверсии сахарозы.
Выполненную работу представить в виде иллюстрации в ра-бочей тетради.
42







Работа 6
Влияние температуры нагревания на органолептические свойства продуктов карамелизации сахарозы
При нагревании сахаров до высоких температур происхо-дит процесс карамелизации, протекающий с отщеплением воды и образованием несахарных компонентов. В зависимости от тем-пературы нагревания, вида и количества сахаров образуются раз-личные продукты карамелизации.
Структура конечных продуктов карамелизации сахаров (карамелана, карамелена и карамелина) не установлена - это ок-рашенные вещества от желтого до черного цвета, горького вкуса, специфически терпкого запаха.
Пропорционально накоплению конечных продуктов кара-мелизации изменяется интенсивность показателей: цвет, запах и вкус.
Процесс карамелизации представлен схемой на рис. 2.
Процесс карамелизации сахаров
Дисахариды
С12Н22О11
Карамелан
С12Н18О9
100°С
+ Н2О
Моносахариды: глюкоза +
+фруктоза
С6Н12О6
108-149ºС
- Н2О
Ангидриды
глюкозан фрук- тозан
t
Продукты
Карамелен конденсации
С36Н50О25 и полимери-
зации
Карамелин
С24Н30О15
Оксиме- Продукты
тилфурфу- реверсии
рол
НС НС О
НОН2С С С С
С Н
Муравьиная кислота Левуленовая кислота
НСООН СН3СОСН2СН2СНСООН
Рис. 2. Схема процесса карамелизации
43













































Цель работы - проследить за изменением органолептиче-ских свойств сахарозы (цвета, вкуса, запаха) при нагревании ее до различных температур; определить максимальную температуру, до которой следует нагревать сахар, чтобы получить жженый са-хар, наиболее интенсивно окрашенный, но без резкой горечи.
Приборы, посуда. Тигель фарфоровый; термометр на 200-250°С; мерный цилиндр емкостью 25-30 см3; четыре мерные колбы емкостью 25-50 см3; воронка; пипетки емкостью 2 см3.
Техника выполнения работы. На технических весах отве-сить в тигли три навески сахара по 5 г, смочить его 1 см3 воды. Тигли поставить на асбестовую сетку и умеренно нагревать. Тем-пературу сахарного расплава замерять термометром, не касаясь дна и стенок тигля. Нагревание вести до указанной температуры (160°, 180°, 200°С). Температуру можно варьировать, например: 170º, 190º, 220°С.
После этого жженый сахар осторожно залить небольшим количеством дистиллированной воды из цилиндра и, помешивая, растворить всю массу. Полученный раствор перелить в мерную колбу. Водой из цилиндра в несколько приемов ополоснуть ти-гель и все промывные воды слить в колбу, охладив ее содержи-мое до комнатной температуры, долить водой до метки и тща-тельно перемешать.
Затем произвести органолептическую оценку полученных растворов жженого сахара и отметить, какой из них имеет интен-сивную окраску, но не имеет резкой горечи и запаха.
Данные свести в табл. 6.
Таблица 6
Органолептическая оценка растворов жженого сахара
Максимальная температура нагревания сахара, ºС
Органолептические показатели цвет вкус запах
160 180 200
В выводах отметить, при каких способах тепловой обра-ботки и изготовлении каких кулинарных изделий образуются продукты карамелизации сахаров и какое влияние оказывает этот процесс на свойства и показатели качества продукции.
44









Работа 7
Клейстеризация крахмала
Клейстеризация, или разрушение нативной структуры крахмальных зерен при нагревании с водой, протекает в несколь-ко стадий и сопровождается набуханием. В начальной стадии зерна крахмала становятся прозрачными, несколько увеличива-ются в объеме, не теряя при этом слоистости. Дальнейшее нагре-вание (при соотношении воды и крахмала не менее чем 1:1) при-водит к необратимому и сильному набуханию зерен, сопровож-даемому увеличением объема зерен и потерей слоистости. Про-должительное нагревание крахмальных клейстеров при высоких температурах (90°С и выше) может вызвать разрушение зерен.
Цель работы - изучить изменение внешнего вида крах-мальных зерен в водной суспензии при разных температурных условиях клейстеризации и определить зависимость между сте-пенью набухания зерен.
Приборы, посуда. Микроскоп с осветителем; стекла пред-метные, покровные и часовые; палочки стеклянные; стаканы хи-мические; бани водяные или песчаные.
Реактивы. 0,004 н. раствор йода в йодистом калии (раствор Люголя); образцы картофельного и кукурузного крахмала. Техника выполнения работы. Для приготовления препарата каждого вида крахмала стеклянной палочкой, смоченной водой, взять немного крахмала и поместить его на предметное стекло. Смочить крахмал капелькой воды и покрыть покровным стеклом. Рассмотреть препарат под микроскопом при увеличении в 280 раз (окуляр 7, объектив 40) и зарисовать зерна сырого крах-мала. Сравнить исследуемые препараты. Обратить внимание на величину зерен и наличие слоистости.
Изучить изменение крахмальных зерен в водной суспензии при нагревании.
Приготовить 2%-ную водную суспензию крахмала: в два химических стакана отвесить на технических весах по 1 г крах-мала, добавить в каждый по 50 см3 воды и размешать. Крахмаль-ные суспензии нагреть при непрерывном помешивании на водя-ной бане до температуры: первую - 58°С, вторую - 80ºС, про-
45
должая помешивать, выдержать их при этой температуре в тече-ние 5 мин, затем охладить.
Приготовить неокрашенные и окрашенные йодом препара-ты крахмала, оклейстеризованного при 58º и 80°С. Для этого на предметное стекло нанести каплю соответствующего клейстера и покрыть его покровным стеклом, рядом (на том же предметном стекле) поместить каплю того же клейстера, окрасив его раство-ром йода. Выступившую из-под покровных стекол жидкость уда-лить фильтровальной бумагой.
Препараты рассмотреть под микроскопом, зарисовать их, отметив обнаруженные изменения крахмальных зерен в резуль-тате клейстеризации при разных температурах (изменение формы и величины зерен, наличие или отсутствие слоистости, появление прозрачности).
Один из приготовленных образцов картофельного или ку-курузного крахмала довести до кипения и прокипятить в течение
1 мин. Каплю клейстера поместить на предметное стекло, окра-сить препарат йодом, рассмотреть под микроскопом и зарисовать крахмальные зерна.
Отметить появление разрушенных крахмальных зерен. Результаты наблюдений свести в табл. 7.
Таблица 7
Зависимость набухания зерна от вязкости клейстера
Объект наблюдения Характеристика крахмальных зерен
Зерна крахмала:
сырого картофельного маисового
клейстеризованного при 58ºС: картофельного
маисового
клейстеризованного при 80°С: картофельного
маисового
В клейстере, подвергшемся кипячению: картофельного
маисового
Сделать выводы по работе. 46




Работа 8
Влияние сахара,
поваренной соли и органических кислот на вязкость крахмального клейстера
При изготовлении крахмалосодержащих кулинарных изде-лий (супов-пюре, соусов, киселей и др.) крахмал клейстеризуется в присутствии составных частей пищевых продуктов (поваренной соли, сахаров, жира, органических кислот и др.), которые оказы-вают влияние на степень набухания крахмальных зерен, раство-римость и ориентацию в растворе крахмальных полисахаридов, что определяет вязкость клейстера.
Цель работы - показать влияние сахаров, поваренной соли, органических кислот на вязкость клейстера крахмала (картофель-ного, кукурузного).
Приборы, посуда. Микроскоп с осветителем; вискозиметр капиллярный; термостат (стакан с водой); секундомер; песочные часы; четыре конические колбы емкостью 100 см3; водяная и пес-чаная бани.
Реактивы. 0,004 н. раствор йода в йодистом калии; 1%-ный раствор поваренной соли; 20%-ный раствор сахарозы; 0,4%-ный раствор лимонной кислоты.
Техника выполнения работы. Для приготовления клейсте-ров в четыре конические колбы емкостью 100 см3 отвесить на технических весах по 1 г крахмала и залить навески 50 см3 соот-ветственно: дистиллированной водой, 20%-ным раствором саха-розы, 1%-ным раствором поваренной соли, 0,4%-ным раствором лимонной кислоты.
Каждую колбу нагреть, помешивая легким встряхиванием, на песчаной бане до кипения. Прокипятить точно 1 мин (следить по песочным часам) и охладить до 20°С (под струей воды).
Приготовить препараты крахмальных клейстеров для мик-рокопирования, окрасить их раствором йода, рассмотреть под микроскопом и зарисовать, обращая внимание на величину и сте-пень распада зерен.
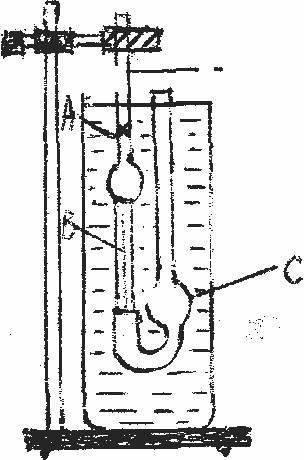
Измерить вязкость приготовленных клейстеров в капил-лярном вискозиметре (рис. 3).
47
Строго постоянный для данного вискозиметра объем жид-кости залить в широкую трубку прибора. Заполненный жидко-стью вискозиметр установить вертикально в стакан с водой (тем-пература 20ºC) так, чтобы метка А была ниже уровня жидкости в стакане.
Рис. 3. Капиллярный вискозиметр
Вискозиметр оставить в термостате на 10 мин, после чего затянуть жидкость в левую трубку выше метки А и с помощью секундомера отметить время истечения объема жидкости между метками А и В. Отчет провести три раза, после чего жидкость вы-лить, вискозиметр промыть водой или спиртом и просушить, а затем наполнить следующим испытуемым раствором, выдер-жать его в термостате 10 мин и замерить время истечении жидко-сти. Замер начать с менее вязкого раствора.
Относительную вязкость η исследуемого раствора опреде-лить по формуле
η=
Т0
Т
ис
,
(3)
где Т0 - время истечения клейстера с дистиллированной водой, с; Тис - время истечения исследуемого раствора, с.
Сделать вывод о влиянии исследуемых добавок на набу-хаемость зерен крахмала и вязкость клейстера.
48

Работа 9
Изменение свойств крахмала в процессе сухого нагрева
Сухой нагрев крахмала сопровождается расщеплением крахмальных полисахаридов с образованием веществ меньшей молекулярной массы (декстринов) и летучих продуктов (СО2, СО, Н2О и др.).
При сухом нагреве крахмала изменяются его органолепти-ческие и физико-химические свойства: цвет (от белого до корич-невого), запах, снижается вязкость клейстера. Степень изменений тем значительнее, чем выше температура и больше длительность сухого нагрева.
Цель работы - сравнить органолептические и физико-химические свойства крахмала исходного и подвергнутого сухо-му нагреву при различных температурах.
Для работы необходимо иметь крахмал исходный и прогре-тый в течение 4 ч при температуре 160° и 180°С (прогревание крахмала проводят лаборанты).
Приборы, посуда. Микроскоп; рефрактометр; аппарат для встряхивания; центрифуга; вискозиметр капиллярный; водяная баня; три конические и три мерные колбы емкостью 100 см3; че-тыре химических стакана емкостью 100 см3 и три емкостью
25 см3; стекла предметные и покровные; палочки стеклянные; стеклянные пластинки размером 100×150 мм.
Реактивы. 0,004 н. раствор йода в йодистом калии; 0,1 н. раствор едкого натрия или калия.
Техника выполнения работы
Органолептические показатели. Цвет образцов, подвергну-тых сухому нагреву, сравнить с цветом исходного крахмала. Для этого на стеклянные пластинки насыпать по 3-5 г исследуемых образцов крахмала. Разровнять образцы с таким расчетом, чтобы получился слой толщиной около 5 мм.
Сравнить цвет непрогретого крахмала и прогретого.
Для определения запаха к 10-15 г каждого вида крахмала добавить небольшое количество теплой воды (не выше 50°С), че-
49
рез 30 с воду слить и установить запах (запах сырого крахмала, отсутствие запаха, легкий запах горелого и пр.).
Для характеристики внешнего вида оклейстеризованных зерен в конические стаканы отвесить по 0,2 г каждого образца крахмала, залить их 40 см3 воды, размешать, нагреть до кипения, кипятить 1 мин, затем приготовить препараты оклейстеризован-ного крахмала для микроскопирования, окрасить их йодом, рас-смотреть в микроскоп, зарисовать и отметить различия вo внеш-нем виде крахмальных зерен.
Растворимость. В конические колбы емкостью 100 см3 от-весить по 1 г каждого образца крахмала, залить 10 см3 дистилли-рованной воды, закрыть колбы пробками, встряхнуть их на аппа-рате для встряхивания в течение 15 мин. После этого содержимое колб перенести в центрифужные пробирки и центрифугировать
3 мин при скорости 1000 об./мин.
В центрифугате определить количество сухих растворимых веществ рефрактометрическим методом.
Результаты исследований свести в табл. 8.
Таблица 8
Изменение свойств крахмала в процессе сухого нагрева
Объект исследования
Органолептические показатели
Внешний вид Цвет Запах
Физико-химические показатели
Растворимость, Относительная
% вязкость
Крахмал:
исходный
прогретый при 160ºС прогретый при 180°С
Сделать выводы по работе.
По теме «Изменения свойств углеводов» обобщить мате-риал и сделать заключение.
2.3. Изменение жиров
при тепловой кулинарной обработке
Жиры представляет собой сложные эфиры трехатомного спирта - глицерина и высокомолекулярных жирных кислот.
50



















Свойства жиров определяются составом жирных кислот, которые могут быть насыщенными (пальметиновая, стеариновая) и нена-сыщенными (непредельными - олеиновая, линолевая, линолено-вая, арахидоновая). Жиры характеризуются пищевой и биологи-ческой ценностью, высокой калорийностью и являются важными вкусовыми и структурными компонентами блюд и кулинарных изделий. При приготовлении продукции жиры используются как: антиадгезионное средство, уменьшающее прилипание продуктов к греющей поверхности при жарке; теплопроводящая среда при жарке (особенно во фритюре); растворители каротинов и арома-тических веществ (пассерование моркови, лука, томата и пр.); со-ставная часть рецептур многих кулинарных изделий и блюд; структурообразователи некоторых соусов (соус голландский, майонез) и видов теста (песочное, слоеное и пр.).
При тепловой кулинарной обработке в жирах происходят как гидролитические, так и окислительные изменения, обуслов-ленные действием на жир высокой температуры, воздуха, воды и других факторов. Преобладание того или иного процесса зави-сит от температуры и продолжительности нагревания, степени воздействия на жир воды и воздуха, а также от присутствия ве-ществ, способных вступать с жиром в химические взаимодействия.
Наиболее глубокие изменения претерпевают жиры в про-цессе фритюрной жарки. Жир подвергается воздействию высоких температур (180°С) в присутствии воздуха и паров, выделяющих-ся из обжариваемых продуктов. Жарка продуктов во фритюре со-провождается гидролизом в жире триглицеридов и окислением свободных жирных кислот. В жире накапливаются перекисные соединения, затем промежуточные (спирты, альдегиды, кетоны, эпокиси) и, наконец, вторичные продукты окисления (дикарбо-нильные соединения, диоксикислоты и др.) и сополимеризации. Частицы продукта попадают в жир, составляющие их вещества под влиянием высокой температуры расщепляются, и продукты расщепления, в свою очередь, могут реагировать с жиром.
Перечисленные факторы вызывают изменения органолеп-тических и физико-химических показателей жира. Общие изменения, происходящие с жиром при тепловой обработке, можно представить в виде схемы (рис. 4).
51
Окисление
Перекиси
R-CH=CH-CH-R
O-OH
и гидроперекиси R-CH-CH-R1
O-O
Жиры
Гидролиз
Свободные Моно-
жирные и диглицериды кислоты
R-COOH
Глицерин
CH2OHCHOHCH2OH
Дегидратация
Окисление
Промежуточные
нестабильные продукты окисления
Окисление
Дальнейшее окисление Полимеризация
и поликонденсация
Акролеин O
CH2=CH-C
H
Вторичные стабильные
Эпоксиды
R=CH-CH-R1 O
Диоксикислоты R=CH-CH-R1
OH OH
Альдегиды
O
R-CH
H
Дикарбоновые соединения
R-C-C-R1
O O
продукты окисления
Производные кислот с сопряженными
связями
R-CH=CH-CH=R
Продукты сополимеризации
Рис. 4. Изменение жира при тепловой кулинарной обработке
Потемнение жира и приобретение специфического запаха и вкуса обусловлено рядом причин, и в первую очередь пироге-нетическим расщеплением органических веществ, входящих в со-став обжариваемых продуктов. Изменение цвета также в опреде-ленной мере обусловлено меланоидинами, меланофосфатидами. Возможно, что в формировании цвета гретого жира участвуют темноокрашенные вторичные продукты окисления (продукты конденсации дикарбонильных соединений и пр.).
В процессе фритюрной жарки физические показатели жира изменяются: возрастает коэффициент преломления, увеличивает-
52






























































ся удельный вес и вязкость. Это свидетельствует о появлении в жире в результате окисления новых функциональных групп (карбонильных, карбоксильных, оксигрупп) и формировании но-вых пространственных и других изомеров, о накоплении продук-тов с повышенным молекулярным весом - полимеров, в образо-вании которых принимают участие ненасыщенные жирные ки-слоты, продукты их окисления (например, оксикислоты) и другие продукты термического разложения глицеридов.
В соответствии с СП 2.3.6.1079-011 определен порядок ис-пользования гретого жира и лимитированы следующие показате-ли: кислотное число не должно быть больше 0,5, а для нагретых -0,5-2,2); вязкость в процессе нагревания жиров не должна увели-чиваться более чем на 35%; число рефракции не должно возрас-тать более чем на 0,0015; количество продуктов термического окисления и сополимеризации не должно превышать 1%. Запре-щается использовать фритюрный жир, если степень термического окисления превышает 1%.
Вопросы для самоподготовки
1. Какие физико-химические показатели характеризуют ка-чество жиров, используемых для приготовления кулинарных из-делий?
2. Как изменяется жир при тепловой обработке? Почему при варке преобладают гидролитические процессы, а при жарке -окислительные?
3. Какие изменения жиров характеризует дымообразование и при каких температурах нагревания наблюдается этот процесс?
4. Что такое «угар» жира и от чего зависит этот показатель?
5. Чем обусловлена неодинаковая степень поглощения жи-ра различными продуктами при жарке?
6. Как изменяются органолептические и физико-химичес-кие показатели качества фритюрного жира при длительном его использовании?
1 СП 2.3.6.1079-01. Санитарно-эпидемиологические требования к орга-низациям общественного питания, изготовлению и оборотоспособности в них пищевых продуктов и продовольственного сырья. М., 2001.
53

Работа 10
Изменение органолептических
и физико-химических показателей растительного масла в процессе фритюрной жарки
Продолжительное нагревание жиров в качестве фритюра сопровождается изменением его органолептических показателей (цвета, вкуса, запаха, консистенции), физико-химических показа-телей (увеличением коэффициента преломления, удельной мас-сы, вязкости, накоплением продуктов термического окисления -сополемиризации).
Цель работы - установить степень изменения органолеп-тических и физико-химических показателей растительного масла в процессе фритюрной жарки.
Приборы, посуда. Пробирки; химические стаканы емко-стью 100 см3; водяная баня; предметные стекла; капиллярный вискозиметр; секундомер; рефрактометр.
Реактивы. 2%-ный спиртовый раствор КОН; 0,01%-ный раствор метиленового голубого.
Техника выполнения работы. В четыре пробирки налить по
15 см3 исследуемых образцов растительного масла свежего, про-гретого в течение 4 и 12 ч при температуре 180°С, использован-ного в течение 4 ч для жарки картофеля, и определить органолеп-тические показатели: цвет, запах, вкус.
Перед определением запаха пробирки с маслом закрыть пробками и нагреть на водяной бане до температуры 50°С. Обра-зец подогретого масла нанести тонким слоем на предметное стекло. Расположить пробы в ряд по возрастанию интенсивности запаха, отмечая его оттенки.
Качественная проба на степень окисленности масла. Реак-ция, основанная на взаимодействии продуктов окисленности с индикатором метиленовым голубым, дает возможность устано-вить ориентировочно степень окисленности масла. В пробирку с внутренним диаметром 10 мм поместить 3 см3 растительного масла, добавить 7 см3 2%-ного спиртового раствора гидрата оки-си калия, закрыть пробирку пробкой и энергично встряхивать в течение 30 с. Верхний слой (спиртово-щелочной) фильтровать
54
через бумажный фильтр в пробирку. Отобрать пипеткой в про-бирку 1 см3 фильтрата и добавить 5 капель 0,01%-ного водного раствора метиленового голубого. При содержании в масле, ис-пользуемом в качестве фритюра, менее 1% продуктов окисления цвет жидкости в пробирке должен быть розовый. Если продуктов окисления более 1%,то цвет - желто-коричневый.
Определение вязкости. Вязкость определяется в капилляр-ном вискозиметре (см. рис. 3).
Необходимый для данного вискозиметра объем масла от-мерить пипеткой и залить в широкую трубку прибора так, чтобы масло заполнило объем шарика С. На тонкую часть прибора на-деть резиновую трубку и затянуть масло в узкую часть прибора выше метки А. После заполнения пространства между метками А и Б мениск масла должен выступать из широкого вогнутого коле-на в шарик С. Заполненный маслом вискозиметр установить строго вертикально в термостат с температурой 20°С на 15-20 мин, после чего затянуть масло в узкую трубку прибора выше метки А и с помощью секундомера отметить время истечения объема мас-ла, заполняющего вискозиметр между метками А и Б.
Отсчет повторить три раза и вычислить среднеарифметиче-скую величину. После исследования каждого образца масло вы-лить из вискозиметра, промыть прибор жирорастворителем (с жи-рорастворителем работать под тягой!) и просушить в сушильном шкафу.
Изменение вязкости η масла в процессе фритюрной жарки выразить отношением времени истечения гретого масла Т0 ко времени истечения холодного Тис.
Определение коэффициента преломления масла произво-дить с помощью рефрактометра путем нанесения капли жира на призму рефрактометра и измерения показания преломления. По окончании измерения масло удалить с призм сухой ватой, смо-ченной эфиром, а затем - мягкой тканью.
Результаты исследований свести в табл. 9.
55
Таблица 9
Изменение показателей растительного масла в процессе фритюрной жарки
Объект
Органолептические показатели
Физические показатели Коэффициент
исследования
Цвет Запах Вкус
Вязкость
преломления
Норма Факт Норма Факт
Масло свежее Увеличивается Увеличивается
прогретое: не более чем на не более чем на
4 ч 35% 0,0015
12 ч
с картофелем
Сделать выводы о влиянии продолжительности нагревания на органолептические и физические свойства масла.
Работа 11
Изменение степени окисленности
растительного масла в процессе нагревания
Продолжительное нагревание масла при жарке продуктов во фритюре сопровождается гидролизом триглицеридов и окис-лением свободных жирных кислот. На первом этапе накаплива-ются перекисные соединения, затем - промежуточные (спирты, альдегиды, кетоны) и, наконец, вторичные продукты окисления (эпокиси, дикарбоновые соединения и др.) и сополимеризации, количество которых не должно превышать 1%. Масло с содержа-нием более 1% продуктов окисления считается непригодным для использования.
Цель работы - сравнить степень окисленности раститель-ного масла при нагревании в течение 4 и 12 ч при 180°С, а также используемого фритюра для жарки картофеля.
Приборы, посуда. Фотоэлектроколориметр; колба емкостью 250 см3; микробюретка; пипетки емкостью 2; 5 и 10 см3; мерный цилиндр емкостью 50 см3; колбы мерные емкостью 25 см3; стек-лянные палочки; пробирки; водяная баня.
56
































Реактивы. 96%-ный этиловый спирт; нейтральная смесь спирта и эфира в соотношении 1:2; 0,1 н. водный раствор КОН;
1 н. спиртовый раствор КОН; 2%-ный спиртовый раствор КОН; 1%-ный спиртовый раствор фенолфталеина или тимолфталеина; хлороформ; 0,01%-ный водный раствор метиленового голубого.
Техника выполнения работы. Накопление свободных жир-ных кислот при термическом окислении масла контролируют, определяя его кислотное число. В коническую колбу емкостью 100 см3 отвесить на технических весах 2 г масла, прилить 20 см3 нейтральной смеси спирта и эфира (1:2), перемешать до полного растворения масла и добавить 3-4 капли 1%-ного спиртового раствора фенолфталеина. Если масло темное, то вместо фенол-фталеина добавить 2 см3 1%-ного раствора тимолфталеина.
Раствор при постоянном помешивании оттитровать из мик-робюретки 0,1 н. раствором едкого калия до появления розовой окраски, если в качестве индикатора использовался фенолфтале-ин, или синей - при использовании тимолфталеина.
Кислотное число Х процентах вычисляют по формуле
X =
5,611⋅K ⋅V
m
, (4)
где V - количество 0,1 н. раствора КОН, израсходованного на тит-рование, см3; К - поправка к титру 0,1 н. раствора КОН; 5,611 -титр точного 0,1 н. раствора КОН; m - навеска масла, г.
Степень термического окисления масла характеризуют ко-личеством дикарбонильных соединений, которые определяют ко-лориметрическим методом. Термически окисленные жиры, обра-ботанные спиртовым раствором КОН, образуют бурое окрашива-ние тем интенсивнее, чем выше степень их окисления. В колбу отвесить 1 г исследуемого масла и добавить 15 см3 1 н спиртово-го раствора КОН. Перемешав смесь энергичным встряхиванием, колбу поместить на 5 мин на водяную баню (90ºС). Время отсчи-тывают от начала закипания жидкости. Затем колбу со смесью быстро охладить под струей холодной воды, довести объем жид-кости до метки этиловым спиртом, не содержащим карбонильных соединений, и фильтровать раствор через бумажный фильтр не-посредственно в кювету фотоэлектроколориметра. Во избежание
57


помутнения раствора быстро измерить оптическую плотность при синем светофильтре против хлороформного раствора иссле-дуемого масла (1 г масла в 25 см3 хлороформа). Результат выра-зить величиной оптической плотности, которая прямо пропор-циональна степени термического окисления масла.
Результаты исследований свести в табл. 10.
Таблица 10
Степень окисленности растительного масла в процессе нагревания
Объект исследования
Показатели степени окисленности масла Кислотное число Оптическая плотность
Масло свежее прогретое: 4 ч
12 ч
с картофелем
Сделать выводы о степени окисленности масла при нагре-вании.
По теме «Изменения жиров при тепловой обработке» обобщить материал и сделать заключение.
2.4. Влияние технологических факторов на изменение консистенции и содержание пищевых веществ при обработке овощей
Технологические свойства растительных продуктов опре-деляются составом и строением образующих их пищевых ве-ществ и взаимодействием этих веществ в отдельных структурных компонентах.
Главная структурная единица растительной ткани - клетка, основными органеллами которой являются оболочка, цитоплаз-ма, вакуоли, в них - пластиды, митохондрии, ядро. Каждая клетка покрыта оболочкой и соединена с другими посредством межкле-точного вещества, определяемого термином срединная пластин-ка. Совокупность срединных пластинок и клеточных оболочек на-зывается клеточными стенками. От их состава и строения зависит прочность растительной ткани. В состав клеточных стенок входят в основном полисахариды (80-95%): целлюлоза, гемицеллюлозы,
58








протопектин - углеводы клеточных стенок. В клеточных стенках содержатся также белки (экстенсин) и минеральные вещества. При тепловой обработке овощей механическая прочность снижается в 10-20 раз, что является, в основном, следствием де-струкции клеточных стенок. Степень размягчения ткани овощей зависит от многих факторов: свойства продукта, способа подго-товки полуфабриката, способа тепловой обработки, температуры и продолжительности нагревания, реакции среды. При обработке овощей, хранении полуфабрикатов и готовой продукции изменяются пищевая ценность и естественная окраска. Влияние технологических факторов на свойства овощей можно проиллюстрировать приведенными ниже работами. Выполняя работы и анализируя полученные результаты, следует обратить внимание на строение клеток различных ово-щей, на изменения органеллы клеток и клеточной структуры тка-ни при варке овощей, на потери растворимых веществ при кули-нарной обработке.
Вопросы для самоподготовки
1. Охарактеризуйте особенности морфологического строе-ния растительной ткани, клетки и клеточной стенки. Каковы осо-бенности химического состава отдельных структурных элементов растительной ткани, клетки и клеточной стенки?
2. Какие изменения происходят при тепловой обработке со структурными компонентами клеточных стенок (клетчатка, геме-целлюлоза, пектиновые вещества)?
3. Какие факторы оказывают влияние на снижение механи-ческой прочности ткани овощей (размягчение) при тепловой об-работке?
4. От каких факторов зависит выбор способа и продолжи-тельность тепловой обработки овощей?
5. Как изменяются масса и пищевая ценность овощей при тепловой обработке? От каких технологических факторов зависит величина этих изменений?
6. Как влияет механическая и тепловая обработка овощей на содержание в них витамина С? Каковы пути повышения С-витаминной активности готовой продукции из овощей?
59
7. Почему изменяется цвет очищенного картофеля, яблок, грибов при хранении? Каковы способы предотвращения очищен-ных полуфабрикатов от потемнения?
8. Как изменяется цвет овощей (свеклы и зеленых) при теп-ловой обработке? Какие факторы оказывают влияние на степень изменения красящих веществ свеклы?
Работа 12
Строение ткани овощей
и влияние технологических факторов на сохранность клеточных стенок
Цель работы - ознакомиться со строением ткани овощей и изменениями некоторых структурных элементов клеток (кле-точных стенок, протоплазмы и др.) при тепловой обработке. Со-поставить количество клеток с разорванными клеточными стен-ками в пюре овощном, полученном при протирании овощей в го-рячем и холодном состоянии.
Приборы, посуда. Микроскоп с осветителем; лезвие; скаль-пель; препаровальные иглы; стекла предметные и покровные; фильтры бумажные; стаканы химические емкостью 200 см3; тер-мометр; ступка с пестиком.
Реактивы. 1%-ный раствор йода в 3%-ном йодистом калии; 10%-ный раствор поваренной соли; раствор сафранина.
Техника выполнения работы
Вариант 1. Изучение строения клеток и изменений от-дельных элементов исследуют на препаратах сырых и вареных продуктов. Для получения препаратов из овощей каждый экземп-ляр разрезают пополам и одну половину оставляют сырой, а дру-гую варят. Для сравнения результатов срезы для микроскопиро-вания снимают с тех мест мякоти, которые соприкасались друг с другом до разрезания.
Для микроскопирования на каждое предметное стекло по-мещают по два препарата: из сырых и из вареных продуктов, до-бавив к ним по капле воды. Каждый препарат рассматривают в неокрашенном и окрашенном виде. В качестве красителей для препаратов из овощей используют сафранин, который окрашива-
60
ет пектиновые вещества в оранжево-желтый цвет, а клетчатку и хлопья денатурированных белков - в вишнево-красный, для крахмалосодержащих овощей используют йод.
Можно исследовать лук, картофель, морковь, свеклу, пет-рушку, бобовые и другие растительные продукты. При изучении строения ткани лука репчатого - разрезать луковицу вдоль оси роста, из одной половины вынуть мясистую чешую (один слой) и разрезать ее пополам. Одну половину чешуи хранить в стакане с водой, другую варить в течение 15 мин.
С внутренней стороны сырой и вареной чешуи препаро-вальной иглой снять легко отделяющуюся пленку, которая состо-ит из одного слоя вытянутых клеток, и из каждой пленки скаль-пелем вырезать по два квадратика 2×2 мм.
Для удобства наблюдения под микроскопом сырой и варе-ный препараты рекомендуется поместить на одно предметное стекло на расстоянии 3 см. Ко всем препаратам прибавить по ка-пле воды и расправить их препаровальными иглами.
Препараты на одном предметном стекле покрыть покров-ными стеклами и рассмотреть под микроскопом при увеличении 7×40. Препараты на одном предметном стекле оставить не окра-шенными, а на другом окрасить сафранином. Подготовленные препараты покрыть покровными стеклами и рассмотреть под микроскопом, обратив внимание на толщину и состояние клеточ-ных стенок, плотность прилегания друг к другу, степень прозрач-ности содержимого клеток, наличие ядер и других органелл. От-метить различия в строении тканей сырого и вареного лука, а также в структуре и интенсивности окраски отдельных элемен-тов клеток. Зарисовать окрашенные препараты, обозначив на ри-сунках структурные элементы клеток.
Чтобы проследить изменение свойств пристенного слоя протоплазмы в результате варки, используют явление плазмолиза
- отставание протоплазмы от оболочки, вызванное оттоком воды из клеточного сока под действием осмотического давления. С препаратов пленки лука снять покровные стекла, фильт-ровальной бумагой удалить воду и заменить ее двумя-тремя кап-лями 10%-ного раствора поваренной соли. Спустя 5-10 мин пре-параты накрыть покровными стеклами, рассмотреть под микро-скопом и зарисовать плазмолизованные клетки. Обратить внима-
61
ние на уменьшение объема вакуолей в клетках сырого препарата вследствие плазмолиза и на отсутствие плазмолиза в вареном препарате.
Далее изучить строение тканей сырого и вареного картофе-ля и других овощей с помощью микроскопа.
Из середины очищенного клубня картофеля вырезать лом-тик толщиной 5 см и разрезать пополам. Одну половину клубня картофеля - хранить в холодной воде, а другую - варить 15 мин. Затем из сырой и вареной половинок вырезать с помощью брит-венного лезвия по одному брусочку размером 20×5×5 мм для приготовления срезов. С торцевой стороны брусочков сделать по три тонких прозрачных среза площадью 2×4 мм2 (делая срезы, объект и лезвие обильно смачивать водой). Препараты перенести препаровальной иглой на три предметных стекла и добавить по капле воды. Препараты на одном предметном стекле оставить не-окрашенными, на другом окрасить сафранинов, на третьем - саф-ранином и йодом. Избыток краски снять фильтровальной бума-гой, накрыть покровными стеклами и рассмотреть под микроско-пом (при увеличении 7×40). При изучении строения тканей кор-неплодов препараты подготовить так же и варить ломтики свеклы
40 мин, моркови - 20 мин. Препараты свеклы и моркови окраши-вают только сафранином.
Обратить внимание на форму клеток, плотность прилегания их друг к другу, состояние клеточных стенок, крахмальных зерен в тканях сырого и вареного картофеля. Сделать выводы о влиянии тепловой обработки овощей на строение их тканей.
Вариант 2. Очищенный клубень картофеля средних раз-меров разрезать пополам, опустить в пол-литровый стакан, залить горячей водой и варить при слабом кипении 20-25 мин. Одну по-ловинку клубня растереть в горячем виде в ступке, другую охла-дить и также растереть.
Из того и другого пюре приготовить препараты для микро-скопирования: для этого на предметное стекло перенести препа-ровальной иглой немного пюре, прибавить каплю раствора йода и накрыть покровным стеклом.
Изучая препараты под микроскопом при увеличении 7×40, обратить внимание на различие в количестве разорванных клеток картофеля в том и другом пюре. Препараты зарисовать.
62
Сделать вывод о влиянии температуры вареного картофеля при его протирании на степень сохранности клеточных стенок.
Работа 13
Влияние некоторых факторов на механическую прочность
и продолжительность тепловой обработки овощей
Критерием оценки кулинарной готовности овощей при те-пловой обработке служит степень размягчения ткани. Размягче-ние ткани овощей при тепловой обработке связывают с ослабле-нием связей между клетками, обусловленным частичной дест-рукцией клеточных стенок. Степень размягчения овощей в про-цессе тепловой обработки оценивают по механической прочности (определяют сопротивление ткани овощей резанию, разрыву, сжатию, проколу и пр.). При прочих равных условиях размягче-ние ткани овощей зависит от температуры и продолжительности нагревания: чем выше температура и продолжительнее нагрева-ние, тем больше размягчается продукт. Продолжительность теп-ловой обработки овощей зависит от свойств продукта, pH среды и вида органических кислот.
Цель работы - выяснить влияние температуры и продолжи-тельности варки овощей на снижение механической прочности ткани и определить продолжительность тепловой обработки ово-щей при варке их в растворах различных органических кислот.
Приборы, посуда. Нож столовый; четыре химических ста-кана емкостью 500 см3; термометры на 100°С; игла поварская; пипетки на 10 см3 и 1 см3; три колбы мерные емкостью 250 см3.
Реактивы. 3%-ный раствор уксусной кислоты; 1%-ный рас-твор щавельной кислоты; универсальная индикаторная бумага.
Техника выполнения работы
Вариант 1. Для определения влияния температуры на ме-ханическую прочность ткани из очищенного клубня картофеля или корнеплодов (свеклы или моркови) диаметром не менее 10 см вырезать вдоль оси роста две пластинки толщиной по 3 см и раз-резать каждую вдоль пополам. Один сырой образец хранить в во-де, а три другие сварить при различных температурах (80°; 90°
63
и 100°С). Для этого в химические стаканы налить по 200 см3 воды и опустить по одному образцу. Воду нагреть на асбестовой сетке до соответствующей температуры (измеряя термометром) и варить образцы картофеля и моркови 20 мин, свеклы - 40 мин, регулируя нагрев так, чтобы колебания температуры не превышали ± 2ºС.
После варки образцы охладить и произвести испытания ме-ханической прочности - консистенции (поварской иглой). Вариант 2. Для определения влияния продолжительности варки на механическую прочность подготовить образцы, как ука-зано в варианте 1. Один образец, оставив сырым, хранить в воде, а три порознь варить в химических стаканах, добавив 200 см3 во-ды или в пароварочных кастрюлях: один - 10; другой - 20 и тре-тий - 30 мин. После охлаждения образцов водопроводной водой произвести испытания механической прочности с помощью по-варской иглы.
Вариант 3. Для определения влияния pH среды и вида ор-ганических кислот на продолжительность варки очищенный кар-тофель или корнеплоды (свекла, морковь) разрезать на четыре симметричные части, полученные образцы положить в стакан с хо-лодной водой. Приготовить растворы органических кислот для варки. Для этого взять 10 см3 3%-ного раствора уксусной кислоты,
10 и 1 см3 1%-ного раствора щавелевой кислоты, перенести их в три соответствующие мерные колбы на 200 см3, довести до метки дистиллированной водой, перенести в химические стаканы и с по-мощью универсальной индикаторной бумаги определить pH рас-творов.
Стаканы с растворами кислот и дистиллированной водой нагреть до кипения, положить в каждый по одному образцу. От-метить время начала варки образцов и варить их до готовности, проверяя степень размягчения в процессе варки с помощью по-варской иглы. Отметить время окончания варки.
Результаты наблюдений свести в табл. 11.
64
Таблица 11
Влияние продолжительности тепловой обработки
на прочность ткани овощей
Продолжительность (мин) и температура
варки, °С
Варочная среда Органолептическая
Раствор кислоты оценка
Дистиллированная Вид, механической
вода концентрация, pH прочности
% (консистенции)
Сделать выводы по работе.
Работа 14
Влияние тепловой обработки на белки протоплазмы и структурный белок клеточных стенок
В состав клеточных стенок входит структурный белок (экс-тенсин). Пристенный слой протоплазмы клеток состоит в основ-ном из липопротеидов и представляет собой полупроницаемую мембрану. Наглядное представление об этом дает нагревание об-разцов свеклы в воде. Красящие вещества свеклы (как и прочие водорастворимые вещества) находятся в клеточном соке. По мере нагревания свеклы в воде увеличивается диффузия красящих ве-ществ из неповрежденных клеток.
Цель работы - продемонстрировать диффузию раствори-мых веществ клеточного сока вследствие изменения белков про-топлазмы и структурного белка клеточных стенок овощей - свек-лы. Сравнить количество веществ, переходящих в раствор из сы-рых и прогретых образцов свеклы.
Приборы, посуда. Рефрактометр; нож; водяная баня; два химических стакана емкостью 100 см3; две воронки; мерный ци-линдр емкостью 50 см3; термометр на 100°С; две мерные колбы емкостью 50 см3.
Техника выполнения работы. Очищенную свеклу разрезать вдоль оси роста на половинки, из которых вырезать две одинако-вые квадратные пластинки размером 3,0×3,0×2,0 см. Обе пла-
65





























исследования
Объект
стинки промыть несколько раз водой до тех пор, пока вода не пе-рестанет окрашиваться в розовый цвет. Затем свеклу слегка об-сушить фильтровальной бумагой и взвесить каждую пластинку на технических весах. Поместить пластинки порознь в стаканы и залить каждую 45 см3 дистиллированной воды.
Один из стаканов поставить на водяную баню и нагреть во-ду до 70°С. В процессе нагревания следить за появлением из свеклы струек красящих веществ и окрашиванием воды в стака-не. Выдержать при этой температуре 15 мин и охладить до ком-натной температуры.
Профильтровать вытяжки из первого и второго стаканов в мерные колбы емкостью 50 см3, довести их содержимое до мет-ки дистиллированной водой и определить в фильтратах количе-ство сухих веществ, извлеченных из сырой и прогретой свеклы, рефрактометрическим методом.
Зная содержание сухих веществ в исследуемых жидкостях, можно рассчитать далее количество веществ, извлеченных из сы-рой и прогретой свеклы, Х в процентах от массы исходного про-дукта по формуле
Х =
а⋅V
В
, (5)
где а - содержание сухих веществ с учетом поправки на темпера-туру по рефрактометру, %; V - объем вытяжки, 50 см3; В - масса образцов, г.
Сравнить количество веществ, извлеченных из сырой и про-гретой свеклы, и сделать выводы о влиянии тепловой обработки на белки протоплазмы. В выводах отметить температуру, при ко-торой начинается выделение красящих веществ (денатурация белков).
66


Работа 15
Влияние степени измельчения картофеля
на потери растворимых веществ при хранении в воде
При хранении сырых овощей в воде растворимые вещества, извлекаются только из механически поврежденных клеток. По-верхностный слой протоплазмы целых клеток представляет собой мембрану, которая препятствует переходу растворимых веществ в воду.
Цель работы - показать влияние степени измельчения кар-тофеля на потери растворимых веществ при хранении его в воде. Приборы, посуда. Рефрактометр; два стакана емкостью 250 см3; две конические колбы емкость 100 см3; две воронки; ча-совые отекла.
Техника выполнения работы. Очистить три клубня карто-феля и разрезать каждый на две симметричные половинки. Три половинки картофеля взвесить и положить в стакан емкостью 250 см3. Налить в мерный цилиндр 200 см3 дистиллированной во-ды и залить ею картофель так, чтобы только покрыть его. Запи-сать объем израсходованной воды. Три другие половинки клуб-ней нарезать на брусочки сечением 10×10 мм, взвесить их, сло-жить в стакан и залить таким же количеством дистиллированной воды. Закрыть стаканы часовыми стеклами и оставить обе пробы картофеля на 30 мин. В конце настаивания жидкость тщательно перемешать, дать отстояться в течение 5 мин и профильтровать через бумажный фильтр в сухие конические колбы емкостью 100 см3.
Определить количество сухих веществ в каждой вытяжке рефрактометрическим методом. Количество водорастворимых веществ, извлеченных из картофеля, рассчитать по формуле, при-веденной в работе 14.
Сделать выводы по работе. Отметить влияние степени из-мельчения картофеля на извлечение растворимых веществ.
67
Работа 16
Влияние различных способов влажного нагрева на извлечение растворимых веществ из овощей
При тепловой обработке овощей увеличивается проницае-мость клеточных оболочек, облегчается диффузия растворимых веществ в окружающую среду. Потери растворимых веществ за-висят от вида овощей, способа подготовки полуфабриката и спо-соба тепловой обработки.
Цель работы - показать влияние способа тепловой обра-ботки на извлечение растворимых веществ из овощей. Приборы, посуда. Рефрактометр; два стакана емкостью 250 см3; два стакана емкостью 100 см3; две мерные колбы емко-стью 100 см3; часовые стекла.
Техника выполнения работы. Овощи (морковь, свеклу или картофель) очистить, нарезать вдоль на пластинки толщиной 10 мм, а затем на кубики с ребром 10 мм. Кубики тщательно перемешать и разделить на две равные части. Каждую пробу взвесить. Одну положить в стеклянный стакан емкостью 250 см3 и залить горячей дистиллированной водой. Вторую пробу перенести в стакан, на дне которого установлен сетчатый вкладыш, и налить такое же количество горячей дистиллированной воды, как и в первый ста-кан. Закрыть оба стакана часовыми стеклами и довести воду до кипения. Одну пробу отварить основным способом до размягче-ния, а другую проварить на пару в течение 30 мин.
По окончании тепловой обработки отвары слить в стакан-чики емкостью 100 см3, придерживая кусочки овощей часовыми стеклами. Охлажденные отвары профильтровать в мерные колбы емкостью 100 см3, фильтры промыть небольшим количеством дистиллированной воды. Растворы довести до метки дистиллиро-ванной водой, перемешать и определить в них количество сухих веществ рефрактометрическим методом.
Содержание сухих веществ, извлеченных из овощей, в про-центах от массы рассчитать по формуле, приведенной выше (см. ра-боту 14).
Сделать выводы. Отметить влияние способа тепловой об-работки на извлечение (диффузию) растворимых веществ.
68
Работа 17
Влияние тепловой обработки овощей и хранения блюд в горячем состоянии на содержание витамина С
Витамин С (аскорбиновая кислота) является наиболее ла-бильным при хранении и технологической обработке раститель-ных продуктов. Витамин С легко окисляется под действием ки-слорода воздуха при участии окислительных ферментов; он хо-рошо растворим в воде. Металлы и щелочная среда ускоряют разрушение аскорбиновой кислоты, а крахмал, поваренная соль, кислоты способствуют ее сохранению, задерживая процесс окис-ления. При тепловой обработке и хранении продукции часть ас-корбиновой кислоты превращается в дегидроаскарбиновую ки-слоту, а затем происходит деградация обеих форм витамина С.
Степень снижения витамина С зависит от ряда факторов: содержания витамина С и его форм в сыром продукте, режима тепловой обработки (длительности, соотношения воды и продук-та, скорости прогрева продукта, контакта с кислородом воздуха), состава и pH среды, присутствия других веществ, ускоривших или замедляющих его разрушение.
Для определения массовой доли витамина С используют химические (титрометрические), физико-химические (колори-метрические) методы. Метод количественного определения ас-корбиновой кислоты основан на способности восстанавливать натриевую соль 2,6-дихлорфенолиндофенола, которая в щелоч-ной среде имеет синюю окраску, в кислой - красную, а при вос-становлении обесцвечивается.
Цель работы - определить содержание витамина C в сырых и вареных овощах и установить степень снижения C-витаминной активности в процессе тепловой обработки овощей и хранения блюд в горячем состоянии.
Приборы, посуда. Ступка с пестиком; две мерные колбы емкостью 100 см3; мерный цилиндр емкостью 50 см3; два мерных цилиндра с притертыми пробками емкостью 25 см3; четыре кони-ческие колбы емкостью 100 см3; две микробюретки; пипетки ем-костью 1, 2, 5, 10 см3; водяная баня; кастрюля емкостью 0,5 дм3; химические стаканы 0,5 дм3; пароварочная кастрюля.
69
Реактивы. 0,001 н. раствор натриевой соли 2,6-дихлорфено-линдофенола (краска Тильманса); 1%-ный раствор щавелевой ки-слоты; 2%-ный раствор соляной кислоты; кристаллическая аскор-биновая кислота; кристаллический йодистый калий; 2%-ный рас-твор серной кислоты; 0,001 н. раствор йодата калия KJO3; 1%-ный раствор крахмала; витаминизированная поваренная соль.
Техника выполнения работы
Вариант 1. Очищенные картофель, свеклу, морковь или зачищенный лист капусты белокочанной разрезать вдоль оси роста на две половинки. Одну половинку оставить сырой, другую половину взвесить на технических весах и варить до готовности способом, указанным преподавателем.
После варки овощи охладить и взвесить. Изменение массы овощей при варке V в процентах вычислить по формуле
V
−
=
а
в ⋅100,
(6)
а
где а - масса сырого продукта, г; в - масса вареного продукта, г.
Определить содержание витамина C в сырых и вареных овощах индофенольным методом.
Подготовить растворы для титрования. Взять четыре кони-ческие колбы емкостью 100 см3 и внести в них по 1 см 2%-ного раствора HCl и 9 см3 дистиллированной воды (при исследовании овощей) или по 5 см3 кислоты и 5 см3 воды (при исследовании отвара).
Для определения содержания витамина С в овощах из сы-рых и вареных половинок взять навеску массой примерно 10 г. Отмерить мерным цилиндром определенный объем 2%-ного рас-твора HCl из расчета 3 см3 на 1 г овощей.
Навеску сырых или вареных овощей (g) поместить в ступ-ку, добавить из мерного цилиндра небольшое количество кисло-ты и растереть содержимое, постепенно добавляя кислоту. Рас-тертую смесь оставить в ступке для настаивания на 10 мин, затем перенести в мерный цилиндр, профильтровать (V4).
Из полученного экстракта или отвара с помощью пипетки отобрать две пробы по 5 см3 (V3) и перенести их в две ранее под-готовленные конические колбы с раствором кислоты.
70

Оттитровать полученные растворы 0,001 н. раствором 2,6-дихлорфенолиндофенола. Для титрования необходимо пользо-ваться микробюреткой. Титрование следует проводить по каплям, общая продолжительность титрования - не более 2 мин. Конец титрования определяют по появлению розового окрашивания, не исчезающего в течение 30 с.
По окончании титрования записать объем затраченного раствора натриевой соли 2,6-дихлорфенолиндофенола (V1) и при-бавить еще две капли краски. Если при этом образуется устойчи-вое розовое окрашивание, конец титрования определить правиль-но. Результаты параллельных определений не должны расходить-ся более чем на 5%. Для расчетов взять среднее значение этих двух определений.
Параллельно поставить контрольный опыт: вместо экстрак-та, полученного из овощей, или отвара внести в две подготовлен-ные конические колбы с раствором кислоты по 5 см3 дистиллиро-ванной воды и оттитровать, как указано выше. Записать объем краски (V2), затраченной на титрование контрольного раствора. Из двух параллельных определений взять среднее значение.
Содержание витамина С в сырых Х1 и вареных овощах Х2 в граммах на 100 г рассчитать по формуле
(V
−V
)⋅T
⋅V
⋅100
X , X =
1 2
1 2 4
g ⋅V
3
, (7)
где V1 - объем раствора натриевой соли 2,6-дихлорфенолиндо-фенола, затраченного на титрование рабочего раствора, см3; V2 -объем раствора натриевой соли 2,6-дихлорфенолиндофенола, за-траченного на титрование контрольного раствора, см3; V3 - объем экстракта, взятого для титрования, см3; V4 - общий объем смеси в мерном цилиндре, см3; g - навеска, мг; Т - титр раствора натрие-вой соли 2,6-дихлорфенолиндофенола (титр раствора определяют лаборанты); 100 - коэффициент пересчета в мг на 100 г.
Для расчета концентрации витамина С в отварах использу-ют формулу
Х =
(V −V )⋅Т ⋅100
1 2
V 3
(8)
,
71




где V1 - объем раствора натриевой соли 2,6-дихлорфенолиндо-фенола, затраченного на титрование отвара, см3; V2 - объем рас-твора натриевой соли 2,6-дихлорфенолиндофенола, затраченного на титрование контрольного раствора, см3; V3 - объем отвара, взя-того на титрование, см3; Т - титр раствора натриевой соли 2,6-дихлорфенолиндофенола; 100 - коэффициент пересчета в мг на 100 см3.
В связи с тем, что при варке овощей масса изменяется, для определения сохранности витамина С в процентах пользуются формулой
X
С =
(100−V )
2
X
1
, (9)
где X2 - содержание витамина С в вареных овощах, мг на 100 г; V - изменение массы при варке, %; X1 - содержание витамина С в сырых овощах, мг на 100 г.
Изменение содержания витамина С - потери П в процентах при тепловой обработке овощей определяют по формуле
П = 100 - С. (10)
Результаты работы оформить в табл. 12.
Таблица 12
Изменение содержания витамина С при тепловой обработке
Объект Изменение массы
исследования при варке, %
Содержание витамина С, мг на 100 г Изменение
овощей содержания
сырых вареных витамина С, %
Вариант 2. Для того, чтобы изучить влияние продолжи-тельности хранения кулинарных изделий в горячем состоянии на содержание в них витамина С, следует приготовить суп из одного вида овощей, из смеси овощей или концентрата супа (рекоменду-ется преподавателем).
В кастрюлю или химический стакан емкостью 0,5 см3 влить 400 см3 водопроводной воды и нагреть ее до кипения. В кипящую
72






















воду положить нарезанные соломкой (кубиками) овощи (100 г) или концентрат супа (20 г). После вторичного закипания жидко-сти уменьшить нагрев до слабого кипения и варить овощи до го-товности, концентрат супа 15 мин.
Определить содержание витамина С в супе (можно только в отваре).
В 12 конических колб емкостью 100 см3 внести по 2 см3 2%-ной соляной кислоты и по 13 см3 дистиллированной воды. Из готового супа отобрать пипеткой две порции по 5 см3 отвара и слить их в две колбы для титрования с раствором соля-ной кислоты. Затем в суп прибавить 2 г витаминизированной со-ли, хорошо размешать и спустя 2 мин снова отобрать две порции по 5 см3 отвара и перенести их в следующие две колбы для тит-рования. Заметить время.
Кастрюлю или стакан с супом закрыть крышкой, перенести в горячую баню и хранить при температуре 70ºС два часа. Через каждые 30 мин отбирать две пробы супа по 5 см3 в колбы для титрования.
Отобранные пробы оттитровать из микробюретки раство-ром 2,6-дихлорфенолиндофенола до появления слабо розового-окрашивания, не исчезающего в течение 1 мин.
Рассчитать содержание витамина С в пробах супа по фор-муле 7.
Степень изменения содержания витамина С в супе X в про-центах определяют по формуле
X
−
=
а
в ⋅100,
(11)
а
где а - содержание витамина С в свежеприготовленном витами-низированном супе, мг на 100 см3; в - содержание витамина С в супе, хранившемся определенное время, мг на 100 см3.
Результаты работы свести в табл. 13.
73

Таблица 13
Изменение содержания витамина С
при хранении супа в горячем состоянии
Продолжительность хранения, мин Содержание витамина С в супе
мг на 100 см3 от первоначального, %
Контроль (с солью) 30
60 90
Вычертить график зависимости содержания витамина С в супе от продолжительности его хранения.
Сделать выводы по работе.
По теме «Изменения функционально-технологических свойств (изменение консистенции) и пищевой ценности овощей (сухих веществ и витамина С)» обобщить материал и сделать заключение.
Работа 18
Влияние некоторых факторов на изменение окраски свеклы
Антоцианы представляют собой полифенольные соедине-ния из группы флавонидов (моно- и цигликозиды), они распада-ются при гидролизе на сахар и агликоны антоцианидины. Различ-ные антоцианы в соединении с другими пигментами, присутст-вующими в овощах, плодах и ягодах, обусловливают те или иные оттенки их краски. Окраска антоцианов зависит от pH среды. В кислой среде они красные, в нейтральной - фиолетовые, в ще-лочной - синие. При изготовлении сладких блюд из ягод и плодов интенсивность окраски их ослабевает, так как антоцианы могут подвергаться окислительной гидратации и вступать в реакции с металлами под действием света и окисления кислородом возду-ха с участием полифенолоксидаз.
Окраска столовой свеклы обусловлена пигментами бета-лаинами, не относящимися по химической природе к группе ан-тоцианов.
74








Беталаины подразделяются на две группы пигментов -красные (бетацианины) и желтые (бетаксантины). Красных пиг-ментов в свекле больше, чем желтых, содержание их может дос-тигать 95% общего содержания. Бетацианины представлены в ос-новном бетанином (75-95%) общего содержания красных пиг-ментов, а также бетанидином, пробитанином и их изомерами. Содержание и соотношение красных и желтых пигментов в свек-ле обусловливают различия в оттенках ее окраске.
Изменение окраски свеклы в процессе тепловой обработки обусловлено в основном изменением бетанина. Бетанин пред-ставляет собой моногликозид, агликоном которого является бета-нидин и изобетанидин.
При тепловой обработке свеклы бетанины в той или иной степени разрушаются, вследствие чего красно-фиолетовая окра-ска свеклы становится менее интенсивной, а также может приоб-ретать буроватый оттенок.
Степень разрушения бетанина зависит от ряда факторов: способа тепловой обработки и температуры нагревания, концен-трация пигмента, рН среды, контакта с кислородом воздуха, при-сутствия в варочной среде ионов металла и др. Чем выше концен-трация бетанина, тем лучше он сохраняется, чем выше темпера-тура нагревания, тем быстрее разрушается пигмент. Окраска аг-ликона бетанидина зависит от рН среды. В очень кислых средах (рН меньше 2) он имеет фиолетовую окраску, в растворах с более высокими значениями рН - красную. Для сохранения окраски свеклы при припускании, тушении добавляют уксусную или ли-монную кислоту, а в некоторых случаях томат-пюре, содержащий лимонную кислоту. Побурение окраски свеклы в процессе тепло-вой обработки связывают с образованием из бетанина веществ, окрашенных в желто-коричневый цвет.
При охлаждении и последующем хранении готовой свеклы окраска ее частично восстанавливается вследствие регенерации бетанина. Такое явление наблюдается при хранении отварных целых или нарезанных корнеплодов свеклы.
Цель работы - продемонстрировать влияние продолжи-тельности нагревания, концентрации пигментов свеклы и реак-ции среды на устойчивость окраски свеклы при тепловой обра-ботке.
75
Приборы, посуда. Фотоколориметр; чашка фарфоровая диаметром 15 см; мерный стакан емкостью 250-500 см3; десять пробирок емкостью 20 см3; три градуированные пипетки емко-стью 5 см3; восемь мерных колб емкостью 50 см3; три химиче-ских стакана емкостью 250 см3; водяная баня с вкладышем для пробирок.
Реактивы. 4%-ный раствор уксусной кислоты; поваренная соль; кристаллическая лимонная кислота; универсальная индика-торная бумага.
Техника выполнения работы
Вариант 1. Очищенную свеклу натереть на терке и отжать сок в стакан емкостью 250 см3.
В штатив поставить восемь пробирок и пронумеровать их. В две первых пробирки налить по 5 см3 свекольного сока, вторую нагреть; в третью и четвертую - по 4 см3 свекольного сока и до-бавить по 1 см3 дистиллированной воды, четвертую нагреть; в пя-тую и шестую налить по 4 см3 свекольного сока и 1 см3 4%-ного раствора уксусной кислоты, шестую нагреть; в седьмую пробир-ку - 5 см3 свекольного сока и 0,3 г сахарозы; в восьмую - 5 см3 свекольного сока и 0,3 г поваренной соли. Пробирки закрыть пробками и содержимое их тщательно перемешать.
Оставить в качестве эталонов пробирки № 1, 3, 5, а № 2, 4, 6, 7, 8 вместе со штативом поставить на кипящую баню и нагре-вать при кипении в течение 20 мин. Вынуть пробирки из бани и охладить до комнатной температуры. Содержимое всех восьми пробирок перенести в мерные колбы емкостью 50 см3. Пробирки обмыть несколько раз небольшими порциями дистиллированной воды, слить промывные воды в соответствующие мерные колбы.
Содержимое колб довести до метки дистиллированной во-дой, тщательно перемешать и проколориметрировать на фото-электроколориметре с синим светофильтром, в кювете с расстоя-нием между гранями 5 мм. В качестве контрольного раствора ис-пользовать дистиллированную воду (если при измерении величи-на оптической плотности равна более 0,5-0,6, необходимо разба-вить сок водой в 2-3 раза или выбрать другую кювету).
Замер оптической плотности следует начинать с первого раствора.
76
Результаты работы оформить в виде диаграммы, отложив в масштабе величину оптической плотности исходного раствора, а рядом - соответствующего прогретого раствора. Отметить влия-ние концентрации пигментов свеклы, реакции среды и тепловой обработки на степень их разрушения, учитывая, что между кон-центрацией вещества и оптической плотностью его растворов су-ществует прямая зависимость.
Вариант 2. Очищенную свеклу нарезать ломтиками 20×20 мм и толщиной 1 мм общей массой 120 г и разделить на три части по 40 г. На технических весах отвесить две навески кри-сталлической лимонной кислоты по 0,4 г. В три химические ста-кана емкостью 250 см3 налить по 160 см3 дистиллированной воды. В один стакан добавить 0,4 г лимонной кислоты. Определить рН раствора и воды с помощью универсальной индикаторной бумаги, жидкость в стаканах довести до кипения и поместить в нее подго-товленные ломтики. Сделать отметку уровня жидкости и варить свеклу при слабом кипении в течение 40 мин.
По мере выкипания жидкости в стаканы следует добавлять горячую дистиллированную воду до отмеченного уровня. В ста-кан, где ломтики варились в воде, в конце варки добавить 0,4 г лимонной кислоты.
Сравнить интенсивность окраски отваров и свеклы при различных условиях варки. Обратить внимание на консистенцию свеклы, сваренной в воде и в растворе лимонной кислоты.
Сделать выводы по работе.
Работа 19
Влияние бисульфита натрия на сохранение от потемнения очищенного картофеля
Картофель, капуста белокочанная, лук репчатый и другие овощи, а также плоды (яблоки, груши, и др.) имеют белую окра-ску благодаря содержанию в них полифенольных соединений -флавоновых гликозидов, которые бесцветны. В процессе кули-нарной обработки овощи, плоды приобретают желтоватый отте-нок или темнеют. Это происходит вследствие гидролиза гликози-дов с отщеплением несахарного компонента - агликона или обра-
77
зования темноокрашенных продуктов в результате превращений полифенольных соединений и образования меланинов. Предше-ственниками темноокрашенных веществ могут быть такие фе-нольные соединения, как тирозин и хлорогеновая кислота.
При хранении на воздухе поверхность очищенных клубней картофеля темнеет, появляется розовая или коричнево-красная окраска, которая с течением времени становился более интенсив-ной, превращаясь в темно- коричневую или черную.
Причиной потемнения картофеля является окисление со-держащихся в нем полифенолов под действием кислорода возду-ха при участии фермента полифенолоксидазы.
Тирозин (α-оксифенилаланин) и хлорогеновая кислота окисляются с образованием промежуточных продуктов - хинонов и конечных - меланинов. Кроме того, хиноны могут соединяться с аминокислотами, белками и образовывать окрашенные более темные соединения.
Чтобы сохранить от потемнения очищенный картофель, его хранят кратковременно в воде, уменьшая соприкосновение клуб-ней с кислородом воздуха. Для предотвращения очищенных клубней от потемнения в предприятиях общественного питания его сульфитируют, т.е. обрабатывают водным раствором кислых натриевых солей сернистой кислоты:
Na2S2O5+H2O→2NaHSO3.
Эти соли легко разлагаются с образованием сернистого ан-гидрида (SO2), который способен снижать активность полифено-локсидазы и задерживать образование меланинов:
NaHSO3→SO2↑+Na2SO3+H2O.
Кроме того, SO2 вступает во взаимодействие с различными окрашенными органическими веществами и переводит их в бес-цветные или слабоокрашенные соединения.
Цель работы - продемонстрировать влияние обработки очищенного картофеля бисульфитом натрия на его потемнение. Посуда. Две фарфоровые чашки; химический стакан 250 см3; нож поварской.
78
Реактивы. 1%-ный раствор бисульфита натрия (в пересчете на SO2).
Техника выполнения работы. Пять клубней картофеля очи-стить, промыть и разрезать каждый пополам. Пять половинок по-грузить на 6 мин в 1%-ный раствор бисульфита натрия, вынуть и ополоснуть водопроводной водой.
В одну фарфоровую чашку положить пять половинок клуб-ней, обработанных раствором бисульфита, на другую - необрабо-танные половинки (контроль).
Следить за изменением окраски картофеля, отмечая резуль-таты через каждые полчаса. Степень изменения окраски отмечать знаками + (например, слабо выраженное потемнение +, более значительное ++, почернение +++).
Оформить результаты в табл. 14.
Таблица 14
Потемнение очищенного картофеля при хранении
Объект исследования
Время хранения, ч 0,5 1,0 1,5 2,0 …
Картофель:
сульфитированный
несульфитированный
Сделать выводы по работе.
Работа 20
Влияние кислой среды
на изменение окраски зеленых овощей
Зеленый цвет овощей (щавель, шпинат и др.) и некоторых плодов (крыжовник, виноград и др.) обусловлен присутствием в них пигмента хлорофилла, в основном хлорофилла А.
По химической природе хлорофилл А представляет собой сложный эфир двухосновной кислоты и двух спиртов: метилово-го и фитола, общая их формула (C32H30ON4Mg)×(COOCH3)× ×(COOC20H39).
79














В сырых овощах, плодах хлорофилл находится в хлоропла-стах, отделен от органических кислот, содержащихся в вакуолях, тонопластом. Кроме того, хлорофилл соединен с белками, липи-дами, защищен этими веществами от внешних воздействий.
При тепловой обработке зеленые овощи буреют. Происхо-дит это вследствие того, что белки протоплазмы и пластид дена-турируют, мембраны пластид и тонопласт разрушаются, хлоро-филл вступает во взаимодействие с кислотами и кислыми солями этих кислот, содержащимися в соке овощей. Образующееся но-вое вещество - феофитин сообщает овощам бурый цвет:
(C32H30ON4Mg)×(COOCH3)×(COOC20H39)+2HK= =(C32H32ON4) × (COOCH3) × (COOC20H39)+Mg2.
Феофитин. Эта реакция в сырых овощах наблюдается лишь при нарушении целости клеток паренхимной ткани: обычно в местах повреждения овощей появляются бурые пятна.
Степень изменения зеленой окраски овощей и плодов зави-сит от продолжительности тепловой обработки и концентрации органических кислот в продукте и водной среде.
Цель работы - продемонстрировать влияние кислоты на изменение цвета зеленых овощей (на примере вытяжки хлоро-филла).
Приборы, посуда. Штатив с пробирками; водяная баня.
Реактивы. Вытяжка хлорофилла; 0,1 н. раствор щавелевой кислоты.
Техника выполнения работы. Налить в две пробирки вы-тяжку хлорофилла по 5 мл в каждую. В одну из пробирок осто-рожно по каплям прибавлять 0,1 н. раствор щавелевой кислоты до изменения окраски. Содержимое пробирок прогреть на водя-ной бане 1-2 мин.
Сравнить цвет исходной вытяжки хлорофилла и с добавле-нием кислоты после нагревания.
Сделать выводы по работе.
По теме «Изменение цвета овощей при механической и те-пловой обработке» обобщить материал и сделать заключение.
80
2.5. Изменение технологических свойств растительных набухающих продуктов
Качество мучных кондитерских и булочных изделий зави-сит от технологических свойств муки и структуры теста. Струк-тура теста определяется составом и свойствами гидрофильных полимеров (белков, крахмала, гемицеллюлоз, клетчатки), скоро-сти физико-химических процессов (растворения, набухания), а также от ферментативных, биохимических процессов.
Процесс производства мучных хлебобулочных изделий можно подразделить на три этапа, каждый из которых характери-зуется определенными особенностями:
1) замес теста - непродолжительный по времени, но харак-теризующийся протекающими коллоидными процессами - гид-ратация клейковинных белков, переход в раствор альбуминов и глобулинов, растворимых углеводов;
2) брожение теста, занимающее 90% времени, отведенного на приготовление изделий, - в тесте протекает целый ряд биохи-мических и коллоидных процессов, интенсивность и направление которых зависят от исходных свойств муки, наличия тех или иных ингредиентов и температуры окружающей среды;
3) выпечка мучных кондитерских и булочных изделий за-вершает весь цикл изменений, происходящих при замесе и бро-жении теста. Денатурация белковых веществ закрепляет порис-тую структуру теста, а частичная клейстеризация крахмала при-водит к формированию упругого мякиша изделий.
Крупы и бобовые относятся к сухим продуктам, поэтому скорость процессов, приводящих к изменению их структурно-механических свойств, консистенции и массы при замачивании и варке, во многом зависит от интенсивности проникновения во-ды в межклеточное пространство. Размягчение круп и бобовых при замачивании и варке объясняется в основном набуханием белковых и крахмальных студней, клеточных стенок и размягче-нием ткани в целом.
Размягчение и продолжительность варки круп зависят от деструкции гемицеллюлоз, набухания клетчатки и скорости рас-пределения влаги в ядрах, которая обусловлена толщиной кле-точных стенок. Размягчение и продолжительность варки бобовых
81
зависят, кроме того, от деструкции протопектина и экстенсина. При механической и тепловой обработке круп и бобовых вслед-ствие изменения белков и углеводов изменяются их технологиче-ские свойства.
Вопросы для самоподготовки
1. Какие наиболее важные технологические свойства муки учитываются при приготовлении теста?
2. Что происходит с коллоидами муки при замесе теста?
3. Какие технологические факторы могут оказывать влия-ние на качество и количество клейковины?
4. Какие биохимические процессы протекают при приго-товлении дрожжевого теста?
5. Какие факторы оказывают влияние на активность дрож-жей в процессе приготовления дрожжевого теста?
6. Сущность спиртового и молочнокислого брожения при приготовлении дрожжевого теста?
7. Каковы особенности химического состава отдельных структурных элементов ядра и клеточной стенки круп и бобовых?
8. Каковы основные технологические свойства круп и бо-бовых и как они изменяются при замачивании и варке?
9. Почему при тепловой обработке происходит размягчение круп и бобовых?
10. От каких факторов зависит продолжительность тепло-вой обработки круп и бобовых?
Работа 21
Влияние технологических факторов на свойства клейковины муки
Полимеры муки и растворитель (вода, молоко) образуют основу коллоидной структуры теста, которую дополняют и пла-стифицируют различные добавки (сахар, жир, кислоты, химиче-ские разрыхлители и др.).
Цель работы - определить содержание и качество клейко-вины и продемонстрировать влияние тепловой обработки и до-
82
бавления лимонной кислоты на технологические свойства белков муки (клейковины).
Приборы, посуда. Прибор для определения упругости и ра-стяжимости клейковины ИДК-1; три фарфоровые чашки; три ча-совых стекла; три шпателя; два мерных цилиндра емкостью
25 см3; термометр на 100ºС.
Реактивы. 0,2%-ный раствор лимонной кислоты.
Техника выполнения работы. На технических весах отве-сить три навески муки по 25 г и поместить их в фарфоровые чаш-ки, одну из них прогреть в сушильном шкафу при 160°С в тече-ние 40 мин. К навеске прогретой муки и одной навеске непрогре-той муки добавить по 13 см3 водопроводной воды, ко второй на-веске непрогретой муки - 13 см3 0,2%-ной лимонной кислоты и замесить тесто. Замешивание теста вести до тех пор, пока оно не станет совершенно однородным. По окончании замеса полу-ченное тесто хорошо промять руками, скатать в виде шарика, по-местить в чашку, прикрыть стеклом (для предотвращения завет-ривания) и оставить на 20 мин для набухания белков. После этого отметить консистенцию комочков теста.
Из проб теста 2 и 3 (из непрогретой муки) отмыть клейко-вину под слабой струей воды температурой 18-20°С (над ситом). Отмывание вести осторожно, разминая тесто пальцами и наблю-дая за тем, чтобы вместе с крахмалом не отрывались кусочки тес-та или клейковины. Когда бóльшая часть крахмала будет отмыта и клейковина, сначала мягкая и рвущаяся, станет более связанной и упругой, отмывание следует вести энергичнее до тех пор, пока вода, стекающая при отмывании клейковины, не станет прозрач-ной. Для установления полноты отмывания можно к капле воды, выжатой из клейковины, добавить каплю раствора Люголя. От-сутствие синего окрашивания свидетельствует о полноте отмы-вания крахмала. Отмытую клейковину хорошо отжать руками (прессованием между ладонями), обсушить фильтровальной бу-магой и взвесить. После первого взвешивания клейковину еще раз промыть в течение 3-5 мин, отжать, обсушить и взвесить. Ес-ли разница между двумя взвешиваниями не превышает 0,1 г, от-мывание считается законченным.
Содержание сырой клейковины Х в процентах определить по формуле
83
Х =
В
a
⋅100, (12)
где В - масса сырой клейковины, г; а - навеска муки, г.
Так как навеска муки - 25 г, то для определения содержа-ния клейковины в 100 г продукта (в процентах) можно умножить значение массы сырой клейковины на 4.
Качество сырой клейковины определить по цвету, упруго-сти и растяжимости, цвет клейковины - после окончательного отмывания: светлая, серая, темная.
Если клейковина крошащаяся, представляет собой после отмывания губчатообразную, легкорвущуюся массу и не форму-ется в шарик, ее относят к неудовлетворительной без определе-ния качественных показателей упругости, растяжимости и эла-стичности.
Для определения упругости и растяжимости клейковины следует использовать простой прибор ИДК-1 (измерение дефор-мации клейковины в единицах прибора), который позволяет объ-ективно характеризовать качество клейковины по ее сжатию. При определении этих показателей из окончательно отжатой и взве-шенной клейковины отобрать навеску массой 4 г и сформовать шарик с гладкой, без разрывов поверхностью. Сформованный ша-рик необходимо поместить основанием в центр столика ИДК-1. За-тем нажать кнопку «Пуск» и, удерживая в нажатом состоянии 2-3 с, отпустить ее. По истечении 30 с перемещение пуансона ав-томатически прекращается, загорается лампочка «Отсчет». Запи-сав показания прибора, нажать кнопку «Тормоз», поднять пуансон в верхнее исходное положение и снять клейковину со столика прибора.
Результаты измерений упругих свойств клейковины выра-жают в условных единицах прибора, и в зависимости от значения клейковину относят к соответствующей группе качества: сильная
- 61-70; средняя - 71-80; удовлетворительная - 81-100; слабая -101 и более.
Для определения растяжимости клейковины в сантиметрах показания прибора умножают на 0,2.
Эластичность клейковины характеризует набухаемость бел-ков. Эластичная прочная клейковина отличается меньшей растя-
84


жимостью, т.е. длиной, на которую растягивается кусочек клей-ковины.
Данные свести в табл. 15.
Таблица 15
Влияние технологических факторов на свойства клейковины муки
Проба теста
Содержание сырой клейковины, %
Показатели качества Цвет Упругость Растяжимость
С водой
С лимонной кислотой Из прогретой муки
Сделать выводы по работе.
Работа 22
Влияние технологических факторов
на скорость приготовления опары дрожжевого теста
Цель работы - показать влияние технологических факто-ров на скорость приготовления опары. Технологическими факто-рами, оказывающими влияние на подъем опары и активность ферментов дрожжей, являются компоненты, входящие в состав опары теста, и температура брожения.
Приборы, посуда. Четыре мерных стакана емкостью 250-500 см3; водяная баня; термометр.
Техника выполнения работы. На технических весах отве-сить четыре навески муки по 30 г и поместить в химические ста-каны. Взвесить также четыре навески по 2 г прессованных или 0,5 г сухих дрожжей, развести каждую навеску теплой водой в коли-честве 25 см3 и добавить в каждый из четырех стаканов с мукой. Содержимое стаканов перемешать. Один стакан с опарой оставить в качестве контрольного, а в три других добавить: в первый - 0,5 г соли + 1 г сахара; во второй - 4 г сахара; в третий - 2 г соли. Ста-каны закрыть стеклами и поставить на водяную баню с темпера-турой 35°С. Опару в стаканах выдержать до готовности (пока она
85














не станет опадать). Отметить начальный объем опары, скорость подъема, готовность и объем опары в каждом из образцов. Определить увеличение объема образцов V в процентах по формуле
V −V
k
V =
0 ⋅100,
V
0
(13)
где Vk - объем готовой опары, см3; V0 - объем опары после заме-са, см3.
Данные исследований свести в табл. 16.
Таблица 16
Влияние технологических факторов на скорость приготовления опары
Характеристика опары
Образцы V0 Vк V по пористости
и однородности
Сделать выводы о влиянии технологических факторов на скорость приготовления опары.
Работа 23
Изменение технологических свойств круп и бобовых при замачивании и варке
Основными технологическими показателями круп и бобо-вых при замачивании и варке являются увеличение объема и мас-сы. Технологические показатели определяются технологически-ми свойствами сырья и характеризуются коэффициентом набуха-ния, коэффициентом водопоглотительной способности и коэф-фициентом разваривания.
Цель работы - показать изменение технологических свойств круп и бобовых при замачивании и варке и определить технологические показатели (объем, массу и коэффициент разва-ривания).
86












Приборы, посуда. Четыре градуированных цилиндра емко-стью 100 см3; четыре мерных цилиндра с притертыми пробками емкостью 50 см3; водяная баня.
Техника выполнения работы. На технических весах отве-сить по две навески массой 5 г гороха и перловой крупы и помес-тить в градуированные, предварительно взвешенные цилиндры, залить 50 см3 дистиллированной воды, отметить объем зерен (V0); цилиндры закрыть притертыми пробками и оставить для замачи-вания на 1,5-2 ч. Через каждые 30 мин измерять увеличение объ-ема (V) гороха и крупы при замачивании в течение 2 ч. Затем за-крытые цилиндры с навесками поставить на водяную баню и ва-рить при температуре 100ºС. Через каждые 10 мин измерять уве-личение объема (V) до окончания времени варки: гороха - 40 мин, перловой крупы 90 мин (время, идентичное продолжительности тепловой обработки).
Определить коэффициент набухания К (во сколько раз):
K=
V
V
, (14)
o
где V - объем замоченного или сваренного зерна, см3; Vo - объем навески зерна, см3.
Для характеристики увеличения объема сваренного зерна определить степень набухания КV в процентах по формуле
V
К =
−V
o
V
o
⋅100 (15)
Для определения коэффициента водопоглотительной спо-собности Кр предварительно отвар слить в мерные цилиндры ем-костью 50 см3, сваренную крупу взвесить.
Для расчета использовать формулу
Кр =
Р
Р
, (16)
о
где Р - масса сваренного зерна, г; Ро - масса навески, г.
87






В целях выявления показателя распада зерна в процессе варки определить коэффициент развариваемости Х в процентах к сухому остатку отвара, полученного после варки, по формуле:
Х =
А⋅100
Р
о
, (17)
где А - масса сухого остатка, определяемая методом высушивания или рефрактометрически, г.
Данные свести в табл. 17.
Таблица 17
Технологические свойства круп и бобовых при замачивании и варке
Коэффициент Степень набухания набухания
(К) (Кv)
Виды круп, бобовых
Коэффициент
водопоглотительной способности
(Кр)
Коэффициент развариваемости
(Х)
Перловая (30, 60, 90, 120 мин)
Горох (30, 60, 90, 120 мин)
По данным таблицы построить график изменения объема и массы исследуемых продуктов при замачивании и варке в зави-симости от продолжительности варки.
По теме «Изменение функционально-технологических свойств растительных набухающих продуктов» обобщить ма-териал, сделать заключение.
88























при варке
при замачивании
при варке
при замачивании
при варке
при замачивании
2.6. Влияние технологических факторов на изменение консистенции
и содержание пищевых веществ
при обработке продуктов животного происхождения
Из мясопродуктов и рыбы готовят широкий ассортимент полуфабрикатов и блюд. Для доведения их до кулинарной готов-ности, которая характеризуется определенными структурно-меха-ническими и органолептическими показателями (консистенция, цвет, вкус, запах, сочность) и безвредностью, применяют различ-ные способы тепловой обработки.
Ассортимент полуфабрикатов и выбор способа тепловой обработки обусловлены особенностями морфологического строе-ния и химического состава мясопродуктов и рыбы. Мясо различ-ных животных и рыбы содержит: 45-80% воды, 11-21% белков и 1-49% жира, 0,6-1,6% минеральных веществ. В белках мяса и рыбы содержатся все незаменимые аминокислоты, причем в со-отношении близком к оптимальному.
Технологическое использование и пищевая ценность раз-личных видов мяса, птицы и рыбы зависят от химического соста-ва и морфологического строения мышечной, соединительной, жировой и других тканей, входящих в состав продуктов.
Мышечная ткань в мясе и рыбе является преобладающей, служит основой мускулатуры животных и наиболее ценна в пи-щевом отношении. Строение мышечной ткани - это в основном своеобразное сочетание различных белков, определяющих физи-ко-химические свойства ткани: плотность, упругость, эластич-ность. Содержание воды в мышечной ткани - 70-75%. Различают две формы воды, находящейся в мышечной ткани, - связанная и свободная. Связанная вода довольно прочно удерживается бел-ком. Содержание свободной воды в ткани от 50 до 70%; она удер-живается в ткани за счет осмотического давления и адсорбции структурами клеток, а также в результате заполнения внутрикле-точных и межклеточных пространств ткани; в ней растворены экстрактивные, минеральные вещества, витамины и некоторое количество белков.
Различают несколько видов соединительной ткани: рыхлая (прослаивает все органы и ткани), плотная (сухожилия, хрящи)
89
и твердая (составляет основу костей). Структурно-механические свойства и консистенция мяса и рыбы (жесткость, нежность) обу-словлены в основном строением рыхлой соединительной ткани.
В процессе тепловой обработки происходит размягчение ткани мяса и рыбы, связанное с деструкцией коллагена внутри-мышечной соединительной ткани и переходом его в глютин. Ос-новными технологическими факторами, ускоряющими переход коллагена в глютин, являются: температура греющей среды, про-должительность обработки, рН среды.
Пищевая ценность мясопродуктов и рыбы при технологи-ческой обработке изменяется вследствие выделения в окружаю-щую среду воды с растворенными в ней питательными вещест-вами и прямых потерь части этих веществ за счет диффузии, раз-рушения и реакции взаимодействия.
Сочность готового продукта определяется содержанием в нем воды и тесно связана с показателем влагоудерживающей способности (ВУС) мышечной ткани. Миофибриллярные белки в связи с особенностями пространственной структуры их молекул обладают сильно выраженной способностью к набуханию. Сар-коплазматические белки заметного влияния на ВУС мышечной ткани не оказывает.
Способность мяса связывать воду зависит от многих фак-торов: вида мяса и рыбы, температуры замораживания, хранения и оттаивания, степени измельчения, количества растворимых белков, их способности к гидратации, рН среды и др. На ВУС мышечной ткани оказывает влияние добавление поваренной со-ли, фосфатов, протеолетических ферментов.
При кулинарной тепловой обработке полуфабрикатов из мясопродуктов и рыбы происходят физико-химические изменения тканевых белков. Основной вклад в этот процесс вносят струк-турные изменения и гидролитическое расщепление соединитель-но-тканных белков, денатурационные изменения мышечных бел-ков, а также комплекс реакций, влияющих на их кислотно-основ-ные свойства. В результате изменяется химический состав гото-вой продукции, происходит формирование органолептических свойств. Динамика выделения веществ, качественный и количест-венный состав бульонов из мясопродуктов, рыбы неодинаковы.
90
В процессе тепловой обработки мяса изменяется его цвет, что является одним из объективных показателей его кулинарной готовности. Изменение цвета мяса от красного до серо-коричне-вого обусловлено окислительными превращениями гемпротеинов миоглобина.
Вопросы для самоподготовки
1. Пищевая ценность и значение мяса и рыбы в питании.
2. Особенности морфологического строения мышечной и соединительной ткани мяса, птицы, рыбы.
3. Каков состав, свойства и содержание белков мышечной и соединительной ткани мяса и рыбы?
4. В чем отличие мышечной ткани свежего и замороженно-го мяса по характеру распределения воды и способности восста-навливать первоначальное состояние при оттаивании?
5. Сколько воды содержится в мышечной ткани теплокров-ных животных и рыбы? Какая ее часть является гидратной?
6. Как изменяются мышечные белки мяса и рыбы при замо-раживании, оттаивании и тепловой обработке?
7. В каком коллоидном состоянии находятся белки мышеч-ных волокон мяса и рыбы? Как оно изменяется в результате дена-турации?
8. От каких факторов зависит степень дезагрегации колла-гена и ослабления прочности мышечной ткани при тепловой об-работке мяса?
9. Как изменяется содержанке воды и растворимых веществ при тепловой обработке мяса, птицы, рыбы? Какова динамика их выделения? Какие факторы влияют на величину потерь массы и растворимых веществ?
10. Каков состав экстрактивных веществ мяса и рыбы?
11. Каков качественный и количественный состав мясного, костного и рыбного бульонов?
12. Изменение цвета мяса при тепловой обработке, причи-ны сохранения красного цвета в кулинарных изделиях.
13. Чем обусловлено образование вкусовых и ароматиче-ских веществ при тепловой обработке мяса, птицы, рыбы?
91
Работа 24
Микроскопия
сырого и подвергнутого тепловой обработке мяса
Кулинарное использование различных видов и частей туши мяса (варка, припускание, жарка, тушение в натуральном виде или после измельчения на мясорубке) обусловлено количеством соединительной ткани в мускулах и сложностью ее строения.
Содержание соединительной ткани в мышцах и гидротер-мическая устойчивость коллагеновых волокон зависят от ряда факторов: вида мяса, породы, пола животных, их возраста, усло-вий жизни и питания, интенсивности работы, которую произво-дят мышцы при жизни животного.
В результате перехода коллагена в глютин при тепловой обработке гистологическая структура мышц, и особенно просло-ек перимизия, заметно изменяется.
Цель работы - ознакомиться с гистологическим строением различных мышц туши и с изменениями соединительно-тканных прослоек при тепловой обработке на постоянных готовых гисто-логических препаратах.
Приборы. Микроскоп с осветителем; препараты мышечной ткани.
Техника выполнения работы. Для микрокопирования сле-дует взять готовые гистологические препараты из разных частей туши - нежной (например, вырезка, толстый или тонкий край) и жесткой (наружная часть задней ноги или мясо голяшки).
Рассмотреть продольные и поперечные срезы при увеличе-нии 7×40, сопоставить количественное соотношение мышечных волокон и соединительно-тканных прослоек в разных мышцах, сложность плетения коллагеновых пучков в перемизии.
При увеличении 7×40 поместить в поле зрения характер-ный для данного среза участок (должны быть видны мышечные волокна и прослойка пиримизия) и зарисовать его. На рисунках обозначить элементы строения мышечных волокон и перимизия.
В выводах по работе описать различие в строении мускула-туры нежных и жестких частей мяса.
92
Работа 25
Деформация соединительной ткани
вследствие тепловой денатурации белков
Скелетная мускулатура теплокровных животных и рыб представляет собой совокупность мышечных волокон, связанных в единую структуру прослойками соединительной ткани; колла-геновые волокна последней при повышении температуры денату-рируют, при этом резко укорачиваясь и утолщаясь.
Денатурация коллагена, в свою очередь, вызывает сокра-щение и деформацию мышц и выделение из них жидкости, кото-рая освобождается при тепловой денатурации мышечных белков. При этом масса мышц уменьшается на 30-40%.
Степень сжатия и характер деформации мускулатуры вслед-ствие денатурации коллагена зависят от содержания коллагена, сложности строения и плетения его волокон в соединительно-тканных прослойках.
Коллагеновые волокна теплокровных животных и рыб де-натурируют при различных температурах, что обусловлено раз-личием их химического состава и морфологического строения.
Цель работы - проследить за степенью укорочения и харак-тером деформации соединительной ткани мяса говядины и рыбы при нагревании, выяснить влияние денатурации коллагена на из-менение массы и определить температуру денатурации коллагена. В качестве объекта исследования использовать кожу рыбы и за-чищенную пленку эпимизия говядины.
Оборудование, посуда. Два лабораторных зажима Мора; термометр на 100°С; химический стакан емкостью 500 см3; нитки. Техника выполнения работы. Из мускула говяжьей туши, эпимизия говяжьих мышц и рыбьей кожи вырезать вдоль мышеч-ных волокон по одной полоске размером примерно 10×1×1 см, измерить их длину и взвесить с точностью до 0,1 г. К одному кон-цу каждой полоски прикрепить зажим, к другому - нитку. На плитку поставить стакан, опустить в него оба образца и закрепить нитки на кольце штатива так, чтобы зажимы едва касались дна стакана (рис. 5).
93
Рис. 5. Схема установки для проведения опыта
В стакан налить водопроводную воду примерно на 1 см выше верхних концов образцов и погрузить в нее термометр. Медленно нагревая воду в стакане, отметить температуру денатурации белков по моменту отрыва зажимов от дна стакана. Отметить также температуру, при которой уменьшение длины образцов окажется максимальным. После закипания воды опыт-ные образцы вынуть из стакана, снять зажимы, обсушить фильт-ровальной бумагой, взвесить и измерить длину. Обратить внима-ние на различие в степени укорочения образцов, изменения мас-сы и внешнего вида.
Данные наблюдений свести в табл. 18.
Таблица 18.
Характер деформации ткани мяса при нагревании
Объект исследования
Показатель Мясо Эпимизий говяжьих Кожа
говядины мышц рыбы
Длина образцов до нагревания, см
Температура начала укорочения, ºС
Температура максимального укорочения, °С Длина прогретых образцов, см
Укорочение, %
Масса образцов до нагревания, г Масса прогретых образцов, г Изменение массы, %
94




















































































Сделать выводы по работе. В выводах отметить различия в характере деформации образцов мяса вследствие сваривания коллагена и температуры сваривания коллагена рыбы и говядины.
Работа 26
Влияние продолжительности нагревания на степень дезагрегации коллагена
При кулинарной обработке продуктов, содержащих колла-ген (или оссеин костей), под действием тепла и воды часть его превращается в глютин. Степень перехода коллагена в глютин зависит от продолжительности нагревания.
Цель работы - продемонстрировать влияние продолжи-тельности нагрева на количество глютина, образующегося из коллагена соединительной ткани или костей в процессе варки.
Оборудование, посуда. Плитка электрическая; сушильный шкаф; две фарфоровые чашки; две кастрюли емкостью 500 см3; два металлических бюкса; две мерные колбы емкостью 250 см3; две воронки; две пипетки емкостью 25 см3; тигельные щипцы.
Техника выполнения работы. Соединительно-тканные пленки мяса или говяжьи кости хорошо измельчить и переме-шать. На технических весах взять две навески по 50 г, поместить их в кастрюли емкостью 500 см3 и залить четырехкратным коли-чеством дистиллированной воды. Простым карандашом отметить уровень воды на наружной стенке кастрюли, закрыть крышкой, быстро довести до кипения и варить одну навеску 1 ч, другую -
2 ч, подливая по мере выкипания горячую дистиллированную воду. Сваренные бульоны охладить, после чего снять с поверхно-сти жир и профильтровать через вату в мерные колбы емкостью 250 см3. Содержимое колб довести до метки дистиллированной водой, закрыть пробками и хорошо перемешать.
Определить в 25 см3 бульонов содержание сухих веществ путем высушивания проб в сушильном шкафу. Перед определением сухого остатка металлические бюксы довести до постоянного веса (для этого их прогреть 40 мин в су-шильном шкафу при 130°С и охладить в эксикаторе), затем взве-сить на аналитических весах и внести в них с помощью пипетки по 25 см3 каждого бульона.
95
Бульон выпарить на плитке досуха, а затем остаток в бюк-се сушить в сушильном шкафу при 130°С в течение 1 ч 20 мин. В процессе выпаривания бульонов необходимо следить за пробами и периодически смывать со стенок бюксов сухие веще-ства осторожными колебательными движениями. Особенно вни-мательно надо наблюдать за состоянием проб в конце высушива-ния, чтобы избежать их подгорания. Бюксы с сухими остатками вынуть из сушильного шкафа с помощью щипцов, охладить в эк-сикаторе в течение 20 мин и взвесить на аналитических весах. После этого снова поставить боксы в сушильный шкаф, досушить сухие остатки, охладить в эксикаторе 20 мин и взвесить. Основной составной частью сухого остатка костного бульо-на (70%) является глютин. По количеству сухих веществ в буль-оне можно рассчитать содержание в нем глютина Х в % от массы пленок или костей по формуле
Х =
m⋅0,7⋅V ⋅100
, (18) V ⋅ C
1
где m - масса сухого остатка, г; 0,7 - коэффициент пересчета су-хого остатка на глютин; V - объем колбы, см3; V1 - объем бульона, взятого для высушивания, см3; С - навеска пленок или костей, г.
Результаты оформить в табл. 19.
Таблица 19
Влияние продолжительности нагрева на количество глютина
Продолжительность варки соединительно-тканных пленок (костей), ч
Количество сухих
веществ, г
Содержание глютина от массы
соединительно-тканных пленок (костей), %
1
2
Для ускорения исследования массу сухих веществ в бульо-не можно определить рефрактометрическим методом и при рас-чете содержания глютина в формулу (17) внести коррективы.
Сделать выводы по работе.
96








Работа 27
Влияние реакции среды
на степень дезагрегации коллагена
Степень перехода коллагена в глютин зависит не только от продолжительности нагревания, но и от реакции среды: чем боль-ше кислотность ее, тем скорее коллаген переходит в глютин при прочих равных условиях.
Применение органических кислот используется при туше-нии мяса с приправами (томат-пюре, сухое вино), которые содер-жат органические кислоты, а также при мариновании мяса уксус-ной или лимонной кислотой.
Цель работы - продемонстрировать влияние реакции среды на степень перехода коллагена в глютин при тепловой обработке. Оборудование, посуда. Термостойкие стаканы емкостью 250 см3 или 500 см3; две мерные колбы емкостью 100 см3; две во-ронки.
Реактивы. 4%-ный раствор уксусной кислоты; универсаль-ная индикаторная бумага.
Техника выполнения работы. Соединительно-тканные плен-ки из говяжьего мяса нарезать на кусочки размером 5×5 см и хо-рошо перемешать. На технических весах взять две навески пленок по 25 г, поместить их в стаканы и залить трехкратным количест-вом дистиллированной воды. Измерить рН дистиллированной во-ды с помощью универсальной индикаторной бумаги.
В одном из стаканов подкислить воду до рН = 4,5, осторож-но подливая 4%-ный раствор уксусной кислоты (около 15 см3). Величину рН контролировать с помощью универсальной индика-торной бумаги. Затем отметить уровень воды в стаканах каранда-шом, быстро довести воду до кипения и варить 1 ч, подливая по мере выкипания горячую дистиллированную воду.
По окончании варки соединительно-тканные пленки вынуть из стаканов, а бульоны охладить и профильтровать в мерные кол-бы емкостью 100 см3. Пленки промыть дистиллированной водой и слить промывные воды в соответствующие колбы. Содержимое колб довести до метки дистиллированной водой, тщательно пере-мешать и определить в бульонах количество сухих веществ реф-рактометрическим методом. Количество глютина в процентах от
97
массы соединительно-тканных пленок вычислить по формуле, приведенной в работе 26.
Результаты оформить в табл. 20.
Таблица 20
Влияние реакции среды на переход коллагена в глютин
рН
Количество Содержание глютина, % от массы
сухих веществ, г соединительно-тканных пленок
рН дистиллированной воды
рН……………………4,5
Сделать выводы по работе.
Работа 28
Сравнение органолептических показателей
и состава мясного, костного и рыбного бульонов
Цвет, прозрачность, вкус и запах бульонов зависит от их химического состава.
При варке мяса выделяется вода, в которой pacтворены бел-ки, экстрактивные и минеральные вещества. Плавящийся при варке жир частично эмульгирует и равномерно распределяется в бульоне.
При варке костей и рыбных отходов в бульон переходят глютин, жир, небольшое количество минеральных, экстрактив-ных веществ и белков альбуминного характера.
В процессе варки мяса, рыбы и костей белки денатурируют, жир частично расщепляется и окисляется, азотистые и безазоти-стые экстрактивные вещества, вступая друг с другом во взаимо-действие, образуют соединения, которые участвуют в образова-нии вкуса, цвета и аромата бульонов.
Количество веществ, выделяемых из продуктов в варочную среду, зависит от ряда факторов: химического состава и морфо-логического строения продуктов, количества воды, температуры и продолжительности варки.
Критерием оценки качества бульонов являются содержание сухих веществ, в том числе экстрактивных, и органолептические показателя: цвет, прозрачность, вкус и запах.
98






Цель работы - установить различие в органолептических показателях бульонов: мясного, костного, рыбного и из рыбных отходов; определить содержание сухих веществ, количество креатина и креатинина, характеризующих содержание экстрак-тивных веществ.
Приборы, оборудование, посуда. Фотоколориметр; четыре кастрюли емкостью 500 см3; четыре мерные колбы емкостью 250 см3; шесть мерных колб емкостью 50 см3; две воронки; две пипетки емкостью 25 см3; градуированные пипетки емкостью
2 см3; четыре металлических бюкса.
Реактивы. 20%-ная сульфосалициловая кислота; 1 н. соля-ная кислота; насыщенный раствор пикриновой кислоты; 10%-ный раствор едкого натра; 1 н. раствор едкого натра; лакмусовая бумага.
Техника выполнения работы. На технических весах отве-сить по 50 г мяса, рыбы, хорошо измельченных костей и рыбных отходов, поместить в кастрюли емкостью 500 см3, залить каждую навеску четырехкратным количеством дистиллированной воды, быстро довести до кипения, после чего нагрев уменьшить. Каст-рюли закрыть крышками и варить при слабом кипении: кости -
2 ч, рыбные отходы - 1 ч, мясо - 40 мин, рыбу - 20 мин (до го-товности). В процессе варки по мере выкипания жидкости перио-дически подливать горячую дистиллированную воду, следя за тем, чтобы продукт все время был покрыт ею.
По окончании варки бульоны перелить в стаканы, мясо, рыбу, кости и рыбные отходы промыть небольшим количеством дистиллированной воды и соединить промывные воды с соответ-ствующим бульоном. Бульоны охладить, с поверхности снять за-стывший жир и отметить, в каком из них больше жира.
Охлажденные бульоны профильтровать в мерные колбы через вату. Для этого в воронку положить небольшое количество ваты и залить ее дистиллированной водой, которая, стекая, спо-собствует достаточно плотному прилеганию ваты к стенкам во-ронки.
После фильтрования бульонов вату следует промыть не-большим количеством дистиллированной воды. Содержимое колб довести до метки дистиллированной водой и тщательно переме-шать.
99
Налить в стаканы по 50 см3 бульонов, довести до кипения и определить их цвет, запах, прозрачность и вкус. Пипеткой емкостью 25 см3 взять пробы мясного, рыбного, костного и из рыбных отходов бульонов и перенести их в метал-лические бюксы. Содержимое бюксов выпарить, а затем высу-шить. Сравнить цвет и запах сухих остатков.
В бюксы добавить по 25 см3 дистиллированной воды и, по-мешивая стеклянной палочкой, растворить сухие остатки бульо-нов. Отметить наличие осадка, сравнить количество его в мясном, рыбном, костном и из рыбных отходов бульонах, объяснить при-чину образования осадка.
Жидкость с осадками перенести в химические стаканы ем-костью 50 см3, довести до кипения и определить вкус, запах, обра-тив внимание на цвет, прозрачность.
Количество экстрактивных веществ в бульонах можно оха-рактеризовать по содержанию креатинина и креатина. Для определения количества креатина и креатинина в мер-ные колбы емкостью 50 см3 внести по 25 см3 исследуемых бульо-нов, добавить по 20 мл 20%-ной сульфосалициловой кислоты для осаждения белков. Содержимое колб довести до метки дистилли-рованной водой и тщательно перемешать. Колбы оставить на
15 мин для осаждения белков, затем жидкости над осадком про-фильтровать через сухие фильтры в сухие конические колбы. Из фильтратов отобрать до 25 см3, перенести в мерные колбы емко-стью 50 см3, добавить по 12,5 см3 1 н. соляной кислоты. Колбы поставить на плитку и кипятить в течение 60 мин. При нагревании в присутствии соляной кислоты креатин превращается в креатинин.
После нагревания содержимое колб охладить под струей водопроводной воды до комнатной температуры, нейтрализовать соляную кислоту 1 н раствором едкого натра по индикаторной бумаге. Долить содержимое колб до метки водой и тщательно пе-ремешать.
Полученные растворы использовать для определения креа-тинина.
В результате взаимодействия креатинина с пикриновой ки-слотой в щелочной среде образуется пикрат креатинина, имею-щий красно-оранжевую окраску.
Для образования пикрата креатинина по 3 см3 каждого об-разца внести пипеткой в мерные колбы емкостью 50 см3, добавить
100
1,5 см3 насыщенного раствора пикриновой кислоты и 0,5 см3 10%-ного едкого натра. Колбы встряхнуть для перемешивания жидко-сти и оставить на 5 мин.
Окрашенные растворы долить до метки водой, тщательно перемешать и колориметрироватъ на фотоэлектроколориметре с синим светофильтром в кювете с расстоянием между рабочими гранями равным 5 мм. Колориметрирование нужно проводить бы-стро, так как через 20 мин после добавления пикриновой кислоты начинают реагировать сахара. В качестве контрольного раствора использовать щелочной раствор пикриновой кислоты, который приготовить в мерной колбе емкостью 50 см3, для чего внести в нее 1,5 см3 пикриновой кислоты и 0,5 см3 10%-ного едкого на-тра. Содержимое колбы довести водой до метки, тщательно пере-мешать и определить оптическую плотность. Считать, что количе-ство креатинина прямо пропорционально оптической плотности.
Результаты работы оформить в табл. 21, 22.
Таблица 21
Органолептические показатели бульонов
Объекты исследования
Органолептические показатели прозрачность цвет запах вкус
Мясной бульон Костный бульон Рыбный бульон
Бульон из рыбных отходов Сухой остаток бульона: мясного
костного рыбного
из рыбных отходов
Бульоны, полученные при разведении сухих остатков:
мясного
костного рыбного
из рыбных отходов
101
















Таблица 22
Определение креатинина в бульонах
Объекты исследования Оптическая плотность бульонов
Мясной бульон Костный бульон Рыбный бульон
Бульон из рыбных отходов
В выводах по данной работе объяснить разницу показате-лей бульонов.
Работа 29
Влияние фосфатов и органических кислот на водоудерживающую способность белков мышечной ткани мяса и рыбы
Измельченное мясо теплокровных животных и рыбы спо-собно удерживать содержащуюся в нем влагу и связывать воду, добавляемую в фарш. Важные структурно-механические показа-тели качества сырого фарша - вязкость и липкость, а также масса и сочность термически обработанных изделий зависят от водо-удерживающей способности (ВУС) белков мяса, т.е. от отноше-ния воды, выделенной под действием внешней силы, к общему содержанию ее в ткани. Водоудерживающая способность мы-шечной системы удерживать тканевую воду в натуральных по-луфабрикатах и дополнительную - в рубленых зависит от доба-вок, вводимых при приготовлении - солей фосфорной кислоты, поваренной соли, органических кислот и др.
Цель работы - выяснить влияние степени измельчения мя-са и добавления кислот, солей на ВУС фарша, а также органолеп-тические показатели сырых полуфабрикатов и готовых кулинар-ных изделий.
Приборы, оборудование, посуда. Мясорубка; песочные часы на 10 мин; шесть чашек фарфоровых; двенадцать стекол 10×10×1 см; фильтры бумажные; кружочки из полиэтиленовой пленки (диаметр - 2,5 см); пипетка градуированная емкостью
10 см3; три стакана емкостью 250 см3.
102




Реактивы. 10%-ный раствор поваренной соли; 5%-ный триполифосфат натрия в 10%-ном хлористом натрии; 1%-ный раствор лимонно-кислого маринада (рецептура).
Техника выполнения работы. Примерно 350 г зачищенной бескостной говядины или филе рыбы без кожи и костей измель-чить на мясорубке с крупной решеткой, половину фарша дважды измельчить через мелкую решетку. Тот и другой фарш тщательно перемешать и развесить на три порции по 50 г, которые помес-тить в фарфоровые чашки.
К двум порциям из крупной и мелкой рубки прибавить по
10 см3 10%-ного раствора поваренной соли; к двум следующим -столько же раствора триполифосфата и к двум последним - по
10 см3 маринада. Мясо тщательно перемешать с жидкостями и сформовать по два шарика (фрикадельки): один оставить для ис-следования сырых полуфабрикатов, другой подвергнуть тепловой обработке (варке или припусканию).
В процессе перемешивания и формования дать органолеп-тическую оценку консистенции фаршей (однородности, вязкости и липкости) по пятибалльной системе.
Определить влагоудерживающую способность (ВУС) в сы-рых полуфабрикатах и после их тепловой обработки. Для опреде-ления ВУС в сырых полуфабрикатах необходимо на шесть стекол размером 10×10×1 см положить по одному среднепористому фильтру, в центры которых поместить навески образцов массой точно по 10 г, сформованных в шарики. Навески накрыть таким же стеклом, точно по центру поставить грузы весом 1 кг (гиря или сосуд с водой). Ровно через 10 мин грузы и верхние стекла снять. Отделить навески от бумаги и взвесить на весах с точно-стью до 0,1 г.
Подготовленные образцы (шарики) для тепловой обработки взвесить и отварить до готовности. Для этого в три химических стакана положить образцы, налить 50-100 см3 дистиллированной воды, быстро довести до кипения и, уменьшив нагрев, варить ша-рики в течение 15 мин. Образцы вынуть из воды, охладить, взве-сить. Дать оценку полуфабрикатов после варки по внешнему ви-ду, консистенции, сочности по пятибалльной системе. Затем раз-резать образцы пополам, из середины их взять на полиэтилено-вые кружочки навески точно по 10 г. Далее определить ВУС, как
103
описано выше. Влагоудерживающую способность Х в процентах определить по формуле
Х
1
= а ⋅100 ,
а
2
(19)
где X- содержание связанной воды к мясу, %; a1 - масса навески после прессования, г; а2 - масса навески до прессования, г. Результаты работы свести в табл. 23.
Таблица 23
Оценка ВУС белков мышечной ткани мяса, рыбы
Растворы, добавленные в фарш
контроль Показатели (с водой)
поваренной триполи-
соли фосфата
маринада
Виды фарша
крупный мелкий крупный мелкий крупный мелкий крупный мелкий
Для образцов из сырого
фарша, г:
вес навеки до прессо-вания
вес навеки после
прессования ВУС, % Оценка консистенции, баллов
Для образцов после вар-ки, г:
вес навески до прес-сования
вес навески после
прессования ВУС, % Оценка консистенции, баллов
В выводах по работе отметить влияние фосфатов, поварен-ной соли и органических кисло на ВУС белков мышечной ткани говядины и рыбы.
104




























Работа 30
Изменение содержания растворимых веществ в мясе и рыбе при тепловой обработке
Тепловая обработка мяса или рыбы сопровождается уменьшением массы, в основном за счет потери воды денатури-рующимися белками и в меньшей степени - за счет выделения вместе с водой растворимых в ней веществ. Количество раство-римых веществ, выделяемых из мяса, зависит от способа тепло-вой обработки, температурного режима, а также от степени из-мельчения продукта и количества воды при варке.
Цель работы - продемонстрировать влияние степени из-мельчения мяса или рыбы на потерю растворимых веществ при варке.
Приборы, оборудование, посуда. Рефрактометр; мясорубка; нож; три химических стакана емкостью 250 см3; три мерные кол-бы емкостью 100 см3; три воронки; три мерные колбы емкостью
50 см3; палочки стеклянные.
Техника выполнения работы. На технических весах отве-сить один кусочек мяса или рыбы массой 10-30 г, четыре кусоч-ка мяса общей массой 10-30 г, 10-30 г мясного фарша (из фарша сформовать шарики).
Навески мяса или рыбы и фарш положить в химические стаканы, налить в каждый по 50-100 см3 дистиллированной во-ды, быстро довести до кипения и, уменьшив нагрев, варить мясо и рыбу до готовности, а шарики из фарша - в течение 15 мин. По мере выкипания периодически доливать горячую дистиллиро-ванную воду, следить за тем, чтобы мясо было все время покрыто водой.
По окончании варки кусочки мяса или рыбы и сформован-ный фарш вынуть, обмыть небольшим количеством (не более
50 см3) дистиллированной воды, которую присоединить к соот-ветствующему бульону, слегка обсушить фильтровальной бума-гой поверхность кусочков и взвесить их.
Бульоны охладить, снять с поверхности бульонов застыв-ший жир и профильтровать через вату в мерные колбы емкостью 50-100 см3. Колбы долить до метки дистиллированной водой, пе-
105
ремешать содержимое и определить количество сухих веществ рефрактометрическим методом.
Выразить содержание сухих веществ в бульонах Х в про-центах к массе по формуле
Х =
a⋅V ⋅100
в
, (20)
где а - содержание сухих веществ в бульоне, %; V - объем мерной колбы, см3; в - навеска мяса, г.
Результаты исследований свести в табл. 24.
Таблица 24
Влияние измельчения на потерю растворимых веществ в мясе или рыбе при варке
Объект исследования
Потери массы при варке, % Всего Водорастворимые сухие вещества
Один кусок
Четыре кусочка Шарик из фарша
Сделать выводы по работе и отметить, как влияет измель-чение на потерю водорастворимых веществ и изменение массы при варке.
Работа 31
Влияние реакции среды
на изменение цвета мяса при варке
Цвет сырого мяса обусловлен наличием хромопротеида миоглобина. По своему строению миоглобин состоит из белка глобина и простетической группы гема. В сыром мясе в состав гема входит в основном двухвалентное железо. Характерной осо-бенностью миоглобина является его способность легко присое-динять за счет дополнительных валентностей кислород и некото-рые другие соединения без изменения валентности железа.
При тепловой обработке мяса белок глобин денатурирует, а двухвалентное железо в мясе окисляется до трехвалентного.
106










Продуктом окисления является метмиоглобин. Гемовый пигмент, в состав которого входит трехвалентное железо, ведет себя как индикатор; он имеет коричневую окраску в кислой среде и крас-ную - в щелочной.
Обычно вареное мясо окрашено в различные оттенки серо-коричневого цвета в зависимости от содержания миоглобина (в основном) в мышечной ткани. При сдвиге реакции среды в ще-лочную сторону, вызванном начинающимся гнилостным распадом белков, возможно появление розовых оттенков у вареного мяса.
Цель работы - продемонстрировать влияние реакции сре-ды на изменение цвета вареного мяса.
Приборы, посуда. Шесть часовых стекол; шесть химиче-ских стаканов емкостью 200 см3.
Реактивы. Бикарбонат натрия в порошке; 10%-ный раствор уксусной кислоты; универсальная индикаторная бумага. Техника выполнения работы. На технических весах отве-сить шесть кусочков мяса массой 20 г. Навески положить в хими-ческие стаканы, залить каждую 50 см3 дистиллированной воды, отметить уровень. Заготовить навески питьевой соды, равные 0,1; 0,3; 0,5; 0,8; 1,0 г.
В стаканы № 2, 3, 4, 5 и 6 добавить навески соды. Стакан № 1 (без соды) будет контролем. Подготовленные образцы мяса варить до готовности при слабом кипении в стаканах, подливая периоди-чески воду (готовность определить проколом поварской иглы).
Отметить цвет кусочков вареного мяса и бульонов. Опре-делить рН среды бульонов с помощью индикаторной бумаги. Один из кусочков вареного мяса с аномальной окраской еще горячим переложить в стакан с горячей дистиллированной водой и прилить 10%-ный раствор уксусной кислоты до слабоки-слой реакции (проверить по индикаторной бумаге). Результаты оформить в табл. 25.
107
Таблица 25
Влияние реакции среды на изменение цвета мяса при варке
Номер
стакана
Количество NaHCO3, г
рН бульона Цвет вареного мяса
снаружи и на разрезе
Цвет и прозрачность бульона
1 Контроль
2 0,1
3 0,5
4 1,0
Сделать выводы по работе, обратив особое внимание на изменение цвета вареного мяса и бульона в зависимости от рН среды. Отметить влияние реакции среды на прозрачность бульона.
По результатам проведенных исследований в подразделе
2.6 сделать заключение об изменении мышечных и соединитель-но-тканных белков мяса и рыбы при тепловой обработке, о влия-нии технологических факторов на влагоудерживающую способ-ность белков, об изменении функционально-технологических свойств мяса и рыбы при тепловой обработке (консистенции, объема, массы, цвета).
2.7. Влияние технологических факторов на функционально-технологические
свойства продукции
Функционально-технологические свойства продукции обу-словлены свойствами входящих в рецептуру компонентов, изме-нениями их структуры и пищевых веществ при различных спосо-бах обработки и рядом других факторов, влияющих на эти про-цессы.
Большое значение при производстве продукции широкого ассортимента имеют массообменные процессы: эмульгирование, пенообразование. Одним из важнейших свойств белковых и крах-мальных систем является их водосвязывающая и водоудержи-вающая способность. Она определяет изменение массы и органо-лептические показатели продукции.
Соусы являются составной частью широкого ассортимента закусок, горячих блюд и десертов. Они разнообразят и дополня-
108










ют вкус блюда, улучшают консистенцию, повышают пищевую ценность. Большая часть ассортимента соусов готовится с загус-тителями. В качестве загустителей горячих соусов используется мука пшеничная, которую пассеруют для придания соусам харак-терной консистенции и других органолептических показателей. При изготовлении холодных сладких соусов загустителем явля-ется крахмал.
Консистенция масляных соусов (горячих - голландского, хо-лодных - майонеза) обусловлена процессом образования эмульсии. При изготовлении ассортимента сладких блюд, кондитер-ских изделий широко используются процессы пенообразования.
Работа 32
Изменение функционально-технологических свойств муки при приготовлении соусов
Основным компонентом соусов с загустителями является пассерованная мука. При пассеровании муки происходят физико-химические изменения пищевых веществ. Основными измене-ниями являются денатурация белков и частичная деструкция крахмала с последующей клейстеризацией при варке соусов. Пассерование муки увеличивает количество водорастворимых веществ, снижает вязкость мучной суспензии, придает соусу вкус и аромат. Например, вязкость растворов муки пшеничной пассе-рованной меньше, чем исходной сырой в горячем состоянии (65ºС) на 1,5-4%, в холодном (20°С) - на 20-30%.
Цель работы - показать изменение технологических свойств муки при нагревании до 120°С (белая пассеровка) и 150°С (красная пассеровка) и приготовлении соусов.
Приборы, посуда. Водяная баня; вискозиметр; три фарфо-ровые чашки; три градуированных цилиндра емкостью 150-200 см3; три мерных химических стакана емкостью 150-200 см3; термометры.
Техника выполнения работы. На технических весах отве-сить в три фарфоровых чашки по 5 г муки. Одну навеску (проба 1) оставить в качестве контрольной, две навески прогреть в сушиль-ном шкафу в течение 30 мин соответственно при 120ºС (проба 2)
109
и 150°С (проба 3) (условия, идентичные процессу приготовления сухой белой и красной пассеровки).
Навески непрогретой и прогретой муки перенести в гра-дуированные цилиндры и отметить объем, залить 95 см3 воды (t = 60°С), тщательно перемешать суспензию путем встряхивания и оставить для осаждения на 1 ч. По истечении часа отметить объ-ем набухшей муки и отслоившейся воды.
Степень набухания муки К определить по формуле
V V −V
K
=
или КV =
V V
0 ⋅100, (21)
0 0
где V - объем набухшей муки, см3; Vо - объем сухой муки, см3.
Суспензии в цилиндрах перемешать стеклянной палочкой, перелить в химические стаканы и проварить при температуре 95ºС в течение минуты (условия, идеентичные варке соусов). Суспензии снова перелить в мерные цилиндры. Отметить объем. Определить степень набухания муки при варке по вышеприве-денной формуле, а также рассчитать степень деструкции муки Кд при приготовлении белой и красной пассеровки по формуле
Кд =
KV1 − KV 2
KV
KV1 − KV
или Kд =
KV
3
, (22)
2 3
где KV1 - степень набухания муки (непрогретой); KV2 - степень набухания муки (прогретой при 120°С); KV3 - степень набухания муки (прогретой при 150ºС).
Определить относительную вязкость приготовленной сус-пензии из муки с помощью капиллярного вискозиметра. Относи-тельную вязкость определить как отношение времени истечения суспензии из прогретой муки (Т1 - при 120°С, Т2 - при 150°С) ко времени истечения суспензии из непрогретой муки (То). Дать ор-ганолептическую оценку по цвету и запаху проваренных суспен-зий, приготовленных из непрогретой и прогретой муки.
Данные исследований свести в табл. 26 .
110





Таблица 26
Изменение функционально-технологических свойств муки при приготовлении соусов
Органолептические
показатели
суспензий из муки
Объекты Относительная Коэффициент
исследования вязкость деструкции
Цвет Запах
Мука:
непрогретая
прогретая при 120ºС прогретая при 150°С
Сделать выводы по работе и отметить, вследствие каких физико-химических изменений пищевых веществ муки изменя-ются ее технологические свойства.
Работа 33
Функционально-технологические свойства майонезов
Майонез представляет собой мелкодисперсную эмульсию типа «масло в воде», приготовленную из рафинированных дезо-дорированных растительных масел с добавлением эмульгаторов, стабилизаторов, вкусовых добавок и пряностей. Эмульсии пред-ставляют собой дисперсную систему, состоящую из несмеши-вающихся жидкостей, одна из которых распределена в другой в виде мельчайших капель.
Условием существования такой системы является плохая взаимная растворимость жидкостей. Механизм получения эмуль-сии заключается в образовании капель дисперсной фазы в дис-персной среде и стабилизации при помощи адсорбции на их по-верхности эмульгатора.
Для получения устойчивых концентрированных эмульсий (это имеет место при промышленном производстве майонезов) используются эмульгаторы, обладающие одновременно поверх-
111






















Степень набухания
муки до варки, %
Степень набухания
муки после варки, %
ностной активностью и способностью образовывать структури-рованные коллоидно-адсорбционные слои.
Технология приготовления майонезов в условиях общест-венного питания отличается от промышленного способа произ-водства, так как качество майонезов характеризуется небольшой стойкостью эмульсии.
Цель работы - ознакомиться с технологией приготовления майонезов и определить стойкость их эмульсии. Приборы, оборудование, посуда. Центрифуга с числом обо-ротов не менее 1500 мин-1; водяная баня; фарфоровая тарелка ем-костью 250 см3; четыре пробирки (П-1-10-02-ХС по ГОСТ 1770). Техника выполнения работы. В качестве объекта исследо-вания следует принять майонез промышленного изготовления1 (провансаль) и приготовленный по СТН2 (рецептура № 564 вари-ант 1: масло растительное - 125 г; яйца - 1 шт. (желток - 15 г); горчица столовая - 4 г; сахар - 3 г; соль - 1 г; уксус 3%-ный -
25 г). Для приготовления майонеза сырое куриное яйцо, промы-тое в соответствии с санитарными требованиями, разбить и от-делить белок от желтка. В кастрюле из нержавеющей стали рас-тереть желтки с солью, сахаром и горчицей до однородной мас-сы и постепенно тонкой стрункой при непрерывном равномерном помешивании вливать растительное масло. Когда масло соеди-нится с желтками и смесь превратится в густую однородную мас-су, необходимо влить уксус и размешать.
В штатив поставить четыре центрифужные пробирки и про-нумеровать их (опыт предусмотреть в параллельном исполнении). В две первых пробирки налить по 10 г (пробирки заполняют до верхнего деления) майонеза промышленного изготовления («Про-вансаль»), а третью и четвертую - по 10 г майонеза, приготовлен-ного по рецептуре СТН.
Заполненные майонезом пробирки помещают в центрифугу и центрифугируют 5 мин со скоростью 1500 мин-1. Затем эти про-
1 ГОСТ 30004.2-93. Межгосударственный стандарт. Майонезы. Правила приемки и методы испытаний. Минск, 1993.
2 СТН - Сборник технических нормативов. Сборник рецептур блюд и кулинарных изделий для предприятий общественного питания. М., 1996. Ч.1.
112

бирки помещают в кипящую воду на 3 мин и снова центрифуги-руют 5 мин.
Стойкость эмульсии Хс в процентах неразрушенной эмуль-сии по объему вычисляют по формуле
X =
V
,
10
(23)
где V - объем неразрушенной эмульсии, см3; 10 - объем пробы майонеза, см3.
За окончательный результат определения принимают сред-нее арифметическое результатов двух параллельных определе-ний, допускаемые расхождения не должны превышать 2,0%.
Результаты исследований свести в табл. 27.
Таблица 27
Стойкость эмульсии майонеза
Объект исследования
Стойкость эмульсии, % неразрушенной эмульсии Данные исследований Норма для вида майонеза
Майонез провансаль 98
Майонез по рецептуре СТН
Сделать выводы по работе.
Работа 34
Функционально-технологические показатели пенообразных взбивных масс
Процесс пенообразования имеет место при взбивании яиц, сливок, сметаны, некоторых растительных продуктов. При меха-ническом воздействии на белки яиц они превращаются в пену, состоящую из пузырьков воздуха, окруженными тонкими белко-выми пленками (денатурированными белками). Образование бел-ковой пленки сопровождается первоначально развертыванием полипептидной цепи в молекуле белка, и на поверхности раздела двух фаз: «воздух» - «белок» возникают силы поверхностного натяжения и полипептидная цепь сворачивается, образуя форму
113














окружности, наполненную воздухом. При большом увеличении пузырьков воздуха образуется слой белковой пленки в одну мо-лекулу, и при дальнейшем механическом воздействии молекулы белка могут растянуться до предела. Такое изменение конформа-ции белковой молекулы называется механической денатурацией белка. При «перебивании» белков пленка лопается и взбитые белки оседают.
Образовавшаяся пена представляет собой аэрозоль, образо-ванный пузырьками воздуха (дисперсная фаза), денатурирован-ными белками, располагающимися вокруг воздушных пузырьков, и водой с растворенными в ней пищевыми веществами (дисперс-ная среда).
Цель работы - ознакомиться с процессом образования пе-ны при взбивании белков яиц и молочных сливок, определить ус-тойчивость пены в зависимости от добавления пищевых ингреди-ентов и охарактеризовать ее структуру.
Оборудование, посуда. Аппарат для взбивания пены (миксер, взбивальная машина); четыре мерных химических стакана емко-стью 400 см3; четыре стеклянных палочки; три часовых стекла.
Реактивы. Сахарный песок; сахарная пудра; лимонная ки-слота.
Техника выполнения работы
Вариант 1. Определение показателей качества пенообра-зующих взбивных масс. К наиболее важным параметрам, характе-ризующим пену, относятся пенообразование (кратность), плот-ность (дисперсность) и устойчивость.
Для определения показателей пены следует принять при-мерно одинаковый объем исследуемого объекта: 150 мл молоч-ных сливок жирностью 25-30% и 6 яиц куриных (белок составля-ет 61 % от массы яйца без скорлупы, или 146 г). Яйца, промытые в соответствии с санитарными требованиями, разбить и отделить белок от желтка.
1. Определение пенообразования. Белки и молочные сливки поместить в мерные химические стаканы и определить первона-чальный объем Vо в см3. Затем белки яиц перелить во взбиваль-ную емкость и взбить миксером в пенообразную формоустойчи-вую массу. Молочные сливки следует взбивать с помощью мик-
114
сера в течение 3 мин (при более длительном взбивании сливок может произойти отслонение твердой фазы от жидкой).
Взбитые пены осторожно переложить в мерные химические стаканы, определить объем V и рассчитать кратность Кр в про-центах как отношение конечного объема пены к начальному объ-ему жидкости, пошедшей на образование пены по формуле
K
р
V
=V
⋅100,
0
(24)
где V - конечный объем столба пены, см3; Vо - первоначальный объем столба жидкости, см3.
2. Определение плотности (дисперсности). Для определе-ния плотности необходимо взбитые пены в мерных стаканах по-местить во взвешенный с водой стакан (объем 200 см3), взвесить стакан с водой и объектом исследования, и определить объем во-ды вытесненной (выделенной из стакана).
Рассчитать плотность пены В по формуле
M−M
B =
V
ст
, (25)
где М - масса стакана с объектом, г; Мст - масса стакана с во-дой, г; V - объем воды, см3.
3. Определение устойчивости пены при хранении. Устой-чивость пены (УП) при хранении в процентах определить как от-ношение высоты столба пены после разрушения к высоте столба пены перед разрушением
УП =
КВ
НВ
⋅100%, (26)
где КВ - конечная высота столба пены (после разрушения), см3; НВ - начальная высота столба пены (перед разрушением), см3. Данные исследований свести в табл. 28.
115






Таблица 28
Показатели качества пенообразующих взбивных масс
Объект Пенообразующая способность Плотность пены, Устойчивость
исследования (кратность), % г/см3 пены, %
Белки яиц
Сливки молочные
Вариант 2. Влияние технологических факторов на ста-бильность пены при хранении взбитых белков яиц. Четыре яйца, промытые в соответствии с санитарными требованиями, разбить и отделить белок от желтка. Белки взбить миксером в пенообраз-ную формоустойчивую массу. Разложить пенообразную массу в мерные химические стаканы, разделив равномерно на четыре части.
В один из стаканов добавить сахарный песок в соотношении «белок: сахар» как 1: 2, т.е. 48 г, в другой - сахарную пудру в та-ком же количестве, в третий добавить лимонную кислоту в коли-честве 15 мг, а четвертый оставить в качестве контрольного об-разца. Добавление сахарного песка, сахарной пудры и лимонной кислоты необходимо сопровождать перемешиванием белковой пены. Образцы белковой пены оставить на 2-2,5 ч (до окончания лабораторной работы).
В процессе выстаивания пенообразных масс будет наблю-даться отсечение жидкой фазы, количество которой следует за-мерить. Охарактеризовать структуру пен.
Данные исследований свести в табл. 29.
Таблица 29
Влияние технологических факторов на стабильность пены при хранении взбивной массы
Объект Первоначальный
исследования объем, V, дм3
Конечный Структура
объем, V, дм3 пены
Количество отделившейся жидкой фазы
Белковая пена - контроль Белковая пена:
с сахарным песком с сахарной пудрой с лимонной кислотой
116


















Сделать выводы по работе.
По результатам проведенных исследований, в подразде-ле 2.7, сделать заключение об изменении функционально-техно-логических свойств продуктов при различных способах производ-ства (приготовление соусов, пены) и дать характеристику ис-следуемых показателей качества соусов и пенообразующих масс.
Библиографический список
1. ГОСТ Р 50763-95. Общественное питание. Кулинарная продукция, реализуемая населению. Общие технические условия. М.: Госстандарт России, 1995.
2. Технология продукции общественного питания. Физико-химические процессы, протекающие в пищевых продуктах при их кулинарной обработке: учебник /А.С. Ратушный, В.И. Хлеб-ников, Б.А. Баранов и др. М., 2004. Т. 1.
3. Технология производства продукции общественного пи-тания: учебник / B.C. Баранов, А.Л. Мглинец, Л.М. Алешина и др. М., 1986.
4. Лабораторные работы по технологии производства про-дукции общественного питания: учеб. пособие / Л.М. Алешина, Г.Н. Ловачева, Н.Н. Лучкина и др. М., 1987.
5. Массообменные характеристики пищевых продуктов: справочник / А.С. Гинзбург. М., 1990.
6. Теплофизические характеристики пищевых продуктов: справочник / А.С. Гинзбург. М., 1990.
7. Инженерная реология пищевых материалов / Ю.А. Ма-чихин, С. А. Мачихин. М., 1981.
8. Химический состав российских продуктов питания: справ. табл. /под ред. И.М. Скурихина, В.А. Тутельяна. М., 2002, 2006.
9. Химический состав пищевых продуктов: справ. табл.: в 2 кн. /под ред. И.М. Скурихина, М.Н. Волгарева. М., 1987.
10. Химический состав пищевых продуктов: справ. табл.: в 2 т. / под ред. И.М. Скурихина, М.Н. Волгарева. 2-е изд. М., 1994.
11. Руководство по методам анализа качества и безопасно-сти пищевых продуктов / под ред. И.М. Скурихина, В.А. Тутель-яна. М., 1998.
117
12. Справочник технолога общественного питания /А.И. Мглинец, Г.Н. Ловачева, Л.М. Алешина и др. М., 2000.
13. Строение и состав углеводов клеточных стенок, их влияние на технологические свойства растительных продуктов: учеб. пособие / Л.И. Николаева, Г.Ф. Фролова. Екатеринбург, 2002.
Особенности химического состава, строение ткани и техно-логические свойства продуктов животного происхождения: учеб. пособие / Г.С. Лешкова, Л.И. Николаева, Л.В. Рыжова. Екатерин-бург, 2004.
Особенности химического состава, строение ткани и техно-логические свойства продуктов растительного происхождения: учеб. пособие / Г.С. Лешкова, Л.И. Николаева, Л.В. Рыжова. Ека-теринбург, 2005.
118

Приложение
Пример схемы эксперимента в рабочей тетради
Работа 1. Типы коагуляции глобулярных белков
Цель: показать коагуляцию глобулярных белков в резуль-тате тепловой денатурации в зависимости от коллоидного со-стояния и концентрации.
Объекты исследования: сырое яйцо; простокваша; мясной сок. Техника выполнения:
елок
Яйцо
5 см3 мясного 5 см3
сока
5 см3 90 см3 Дист.
вода
Перемешать
5 см3 5 см3 простокваши
Отметить
1. Температуру начала коагуляции
белков
!
2. Образование хлопьев
3. Полное загустение и уплотнение сгустка с выделением жидкости
Вода (постепенное нагревание)
Результаты наблюдений сведены в табл. 1.
Таблица 1 - Исследование коагуляции глобулярных белков
Показатель
Мясной
сок
Простокваша
Яйцо Яйцо натуральное разведенное
Примерная концентрация белков, % Исходное коллоидное состояние бел-ков
Температура начала коагуляции, ºС Температура полной коагуляции, °С Вид белковых гелей после кипячения
Выводы:
119
РазбитьБ
Оглавление
Предисловие 0
