
- •Лекция № 34-37. Химия биогенных элементов
- •Классификации элементов
- •1. Биосфера,круговорот биогенных элементов.Кларки элементов.
- •2. Классификацииэлементов
- •3. Топография важнейших биогенных элементов в организме человека
- •4. Биологическая роль основных классов элементов в организме
- •5. Биологическая рольs-элементов iа-группы.Их применение в медицине
- •6. Биологическая роль s-элементов iIa-группы. Бериллий
- •Кальций
- •Стронций
- •Рубидий и цезий
- •7. Биологическая рольp-элементов
- •8. Биологическая роль d-элементов iб-группы. Биологическая роль ионов меди.
- •Соединения золотаи серебра,их токсичность иприменение в медицине
- •9. Биологическая роль d-элементов viб-группы. Их применение в медицине
- •Молибден
- •10. Биологическая роль d-элементов семейства железа. Применение их соединений в медицине
6. Биологическая роль s-элементов iIa-группы. Бериллий
Бериллий постоянно находится в растениях, а также в организмах животных, т.е. он является примесным ультрамикроэлементом. Биологическая роль бериллия изучена недостаточно. Известно, что соединения бериллия токсичны и вызывают ряд заболеваний (бериллиевый рахит, бериллиоз и т.д.). Особенно токсичны летучие соединения бериллия. Как уже было рассмотрено выше, отрицательное влияние иона Ве2+ на физиологические процессы можно объяснить его химическими свойствами (способностью образовывать прочные связи с биолигандами и хорошей растворимостью фосфатов бериллия).
Магний
Магний формально относится к макроэлементам. Общее содержание его в организме 0,027 % (около 20 г). Топография магния в организме человека такова: в наибольшей степени магний концентрируется в дентине и эмали зубов, костной ткани. Накапливается он также в поджелудочной железе, скелетных мышцах, почках, мозге, печени и сердце. У взрослого человека суточная потребность в магнии составляет около 0,7 г. Ион магния, так же как и ион калия, является внутриклеточным катионом.
В биологических жидкостях и тканях организма магний находится как в виде акваиона, так и в связанном с белками состоянии в количестве <: 10~2 %, т. е. по сущности это микроэлемент.
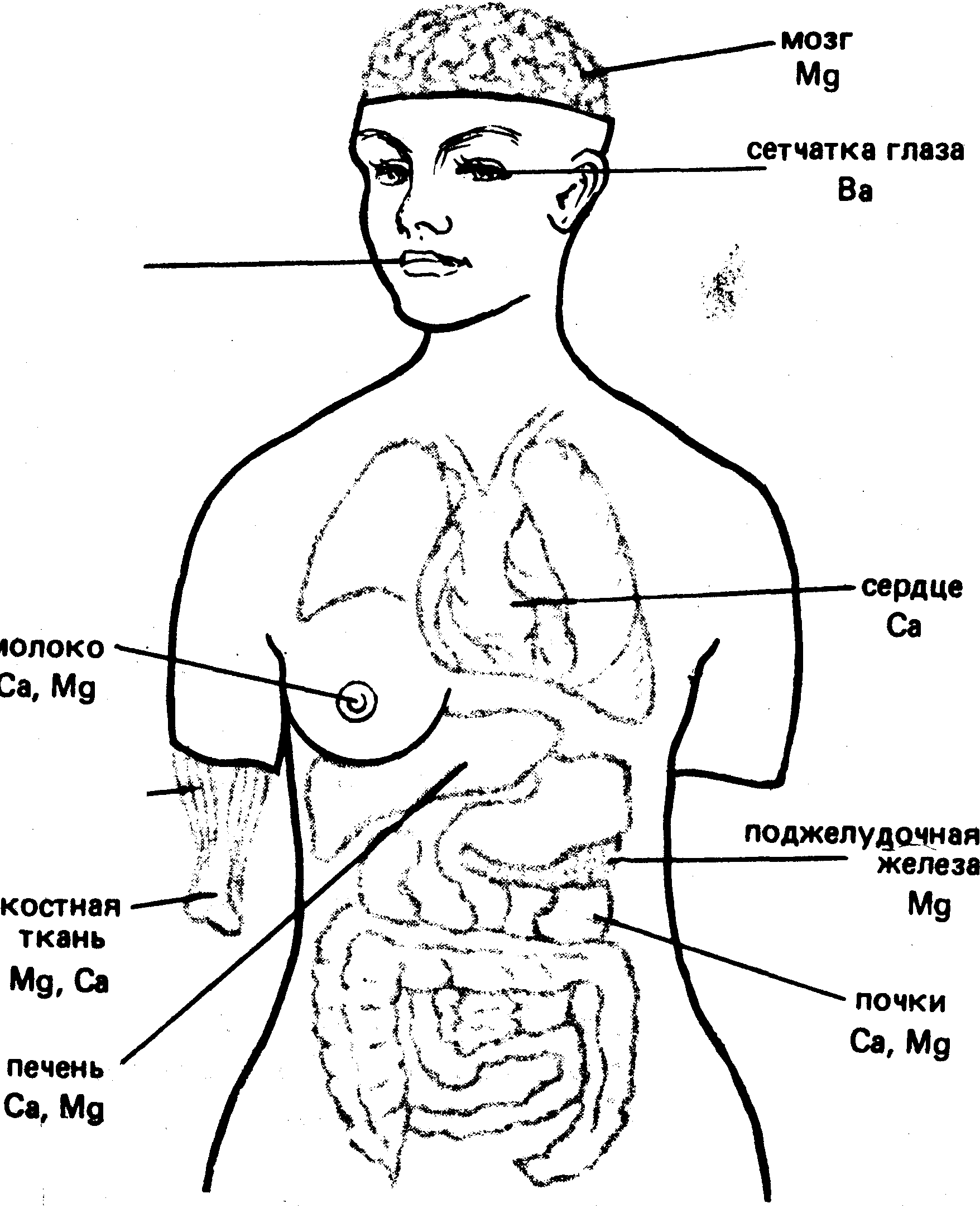
Рис. Топография s-элемёнтов IIА-группы в организме человека
Концентрация ионов магния внутри клеток примерно в 2,5—3 раза выше, чем во внеклеточных жидкостях. Ионы магния играют важную биологическую роль в организме человека. Вследствие меньшего радиуса иона и большей энергии ионизации ион Мg2+ образует более прочные связи, чем ион кальция, и поэтому является более активным катализатором ферментативных процессов. Входя в состав различных ферментативных систем, ион магния является их незаменимым компонентом и активатором (такие ферменты, как карбоксипептидаза, холинэстераза и некоторые другие, являются специфическими для иона магния).
Гидролиз АТФ, сопряженный с рядом ферментативных реакций, в результате которых образуется гидрофосфат-ион НРО42- и выделяется большое количество энергии, проходит при обязательном избытке ионов Мg2+.
Кальций
Кальций относится к макроэлементам. Общее содержание его в организме 1,4 %/ Кальций содержится в каждой клетке человеческого организма. Основная масса кальция находится в костной и зубной тканях. В среднем взрослый человек в сутки должен потреблять 1 г кальция, хотя потребность в кальции составляет только 0,5 г. Это связано с тем, что кальций, вводимый с пищей, только на 50 % всасывается в кишечнике. Сравнительно плохое всасывание является следствием образования в желудочно-кишечном тракте труднорастворимых кальция фосфата Са3(РO4)2 и кальциевых солей жирных кислот.
В организме концентрация ионов кальция регулируется гормонами.
В костях и зубах взрослого человека около 1 кг кальция находится в виде нерастворимого кристаллического минерала — гидроксилапатита Са10(РO4)б(ОН)2, образование которого происходит при взаимодействии ионов кальция с фосфат-ионами.
В крови и лимфе кальций находится как в ионизированном, так и в неионизированном состоянии—в соединениях с белками, углеводами и др. Механизм свертывания крови состоит из ряда этапов, многие из которых зависят от наличия ионизированного Са2+. Ионы кальция принимают активное участие в передаче нервных импульсов, сокращении мышц, регулировании работы сердечной мышцы.
Концентрации ионов кальция внутри и вне клетки соответственно составляют 10-6 и (2,25—2,8) 10-3 моль/л. Поскольку кальций практически не используется внутри клетки, он выступает в качестве строительного материала в организме, в костях, зубах. Скелет — основное хранилище кальция в организме.
Используют кальций хлорид при отравлении солями магния, а также оксалат- и фторид-ионами. Применение препарата в первом случае основано на взаимозамещаемости ионов кальция и магния в организме, а во втором случае—на,образовании нетоксичных малорастворимых соединений кальция оксалата и фторида.
Антацидным и адсорбирующим действием обладает кальций карбонат СаСОз. Его назначают внутрь при повышенной кислотности желудка, так как он нейтрализует соляную кислоту:
СаСОз (т) +2НС1 (жел.сок) = СаСl2 (р) + Н2O (ж) + СO2 (г)
Кальций сульфат (жженый гипс) применяют для приготовления гипсовых повязок при переломах, а также в качестве слепочного материала при протезировании зубов.
Находит применение в медицине и радиоактивный изотоп Са. С помощью этого изотопа были изучены процессы всасывания и распределения кальция в организме, отложения его в костях и выведение при нормальной жизнедеятельности организма и различных патологиях.
