
1 Дано:


![]()
![]()
![]()
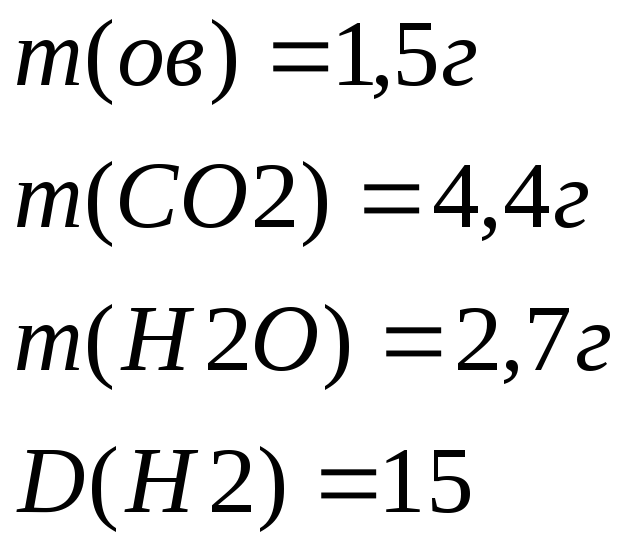
![]() Формула-?
Формула-?
![]()
![]()
![]()

С учетом закона сохранения массы вещества после реакции атомов углерода и водорода столько же, сколько и до реакции С2Н6-простейшая M(C2H6)=30г/моль
Сравнивая массы n2 и n6 одинаковые => истенная формула С2Н6
Ответ: С2Н6
Условие задачи.
Определите молекулярную формулу вещества, при сжигании 3,75г которого получили 2,25г водяного пара и 5,5г оксида углерода(IV). Относительная плотность вещества по водороду равна 15.
1 Дано:


![]()
![]()
![]()
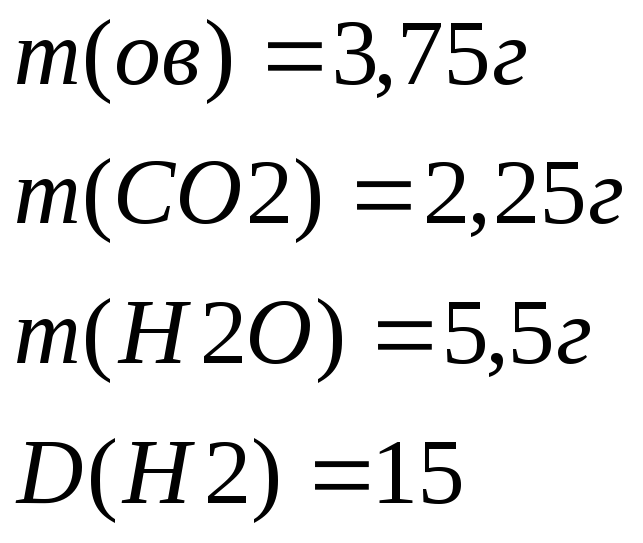
![]() Формула-?
Формула-?
![]()
![]()
![]()

Простейшая СН2 М(СН2)=14г/моль
Сравнивая массы
30г/моль-14г/моль=16/моль=>есть третий элемент О.
Истинная формула СН2О
Ответ: СН2О
Условие задачи.
Сожгли 1,4г органического вещества плотностью 1,25г/л. В результате 1,8г воды и 2,24г оксида углерода(IV).Определите молекулярную формулу вещества.
1 Дано:


![]()
![]()
![]()
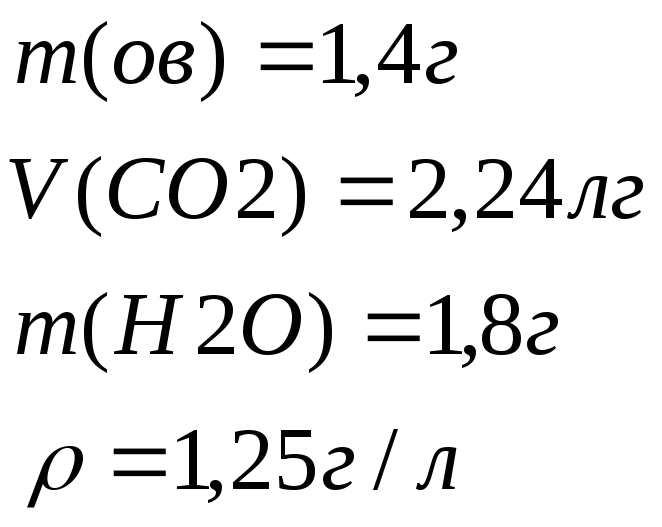
Формула-?
![]()
![]()
![]()

С учетом закона сохранения массы вещества после реакции атомов углерода и водорода столько же, сколько и до реакции С2Н4-простейшая M(C2H4)=28г/моль
Сравнивая массы n2 и n6 одинаковые => истенная формула С2Н4
Ответ: С2Н4
Задачи.
-
При сжигании органического соединения массой 4,2г получен оксида углерода(IV) массой 13,2г и воду массой 5,4г. Относительная плотность этого соединения по воздуху 2,9. Выведите молекулярную формулу органического соединения. Ответ: С6Н2
-
При сгорании 3,6г органического соединения образовалось 11г оксида углерода(IV) и 5,4г воды. Относительная плотность паров этого вещества по водороду равна 36. Определите молекулярную формулу. Ответ: С5Н12
-
Определите молекулярную формулу органического вещества, если при сжигании 25,2г его образовалось 40,32л оксида углерода(IV) (н.у.) и 32,4г воды. Плотность этого вещества равна 1,815г/л. Ответ: С3Н6
-
При сгорании 1,8г органического вещества образовалось 3,96г оксида углерода(IV) и 1,96г воды. Относительная плотность паров этого вещества по водороду равна 30. Выведите молекулярную формулу этого вещества.
-
Выведите молекулярную формулу органического соединения, если относительная плотность его по водороду равна 15. При сгорании 8,96л(н.у) этого вещества, выделилось 8,96л оксида углерода(IV) (н.у) и 7,2г воды
Список литературы:
1. Шамова М.О.
Учимся решать расчетные задачи по химии: технология и алгоритмы решения.
М.: Школа – Пресс, 2001.
2. Радицкий А. М., Курьянова Т. Н.
Дидактический материал по общей химии для 11 класса: Пособие для учителя. – М.: Просвещение, 1997.
3. Гара Н. Н., Габрусева Н. И.
Сборник задач для проведения устного экзамена по химии за курс средней школы. 11класс – М.: Дрофа 1999
4. Штремплер Г. И.
Методика решения расчетных задач по химии: 8-11кл. М.:Просвещение, 2001
