
- •Статистическая физика и термодинамика
- •Элементы статистической физики Основные формулы
- •Тепловые свойства Основные формулы
- •Примеры решения задач
- •I. Основы молекулярно-кинетической теории
- •Физические основы термодинамики
- •Элементы статистической физики
- •Энтропия
- •1. Плотность веществ
- •2. Коэффициенты теплового расширения
- •7. Характеристики некоторых газов
- •8. Критические температура и давление
Термодинамика и статистическая физика
Методические указания и контрольные задания для студентов заочного обучения
Шелкунова З.В., Санеев Э.Л.
Методическое указания и контрольные задания для студентов заочного обучения инженерно-технических и технологических специальностей. Содержат разделы программ ”Статистическая физика”, ”Термодинамика”, примеры решения типовых задач и варианты контрольных заданий.
Ключевые слова: Внутренняя энергия, теплота, работа; изопроцессы, энтропия: функции распределения: Максвелла, Больцмана, Бозе – Эйнштейна; Ферми – Дирака; Энергия Ферми, теплоемкость, характеристическая температура Эйнштейна и Дебая.
Редактор Т.Ю.Артюнина
Подготовлено в печать г. Формат 6080 1/16
Усл.п.л. ; уч.-изд.л. 3,0; Тираж ____ экз. Заказ № .
___________________________________________________
РИО ВСГТУ, Улан-Удэ, Ключевская, 40а
Отпечатано на ротапринте ВСГТУ, Улан-Удэ,
Ключевская, 42.
Федеральное агентство по образованию
Восточно-Сибирский государственный
технологический университет
ФИЗИКА №4
(Термодинамика и статистическая физика)
Методические указания и контрольные задания
для студентов заочного обучения
Составитель: Шелкунова З.В.
Санеев Э.Л.
Издательство ВСГТУ
Улан-Удэ, 2009
Статистическая физика и термодинамика
Тема 1
Динамические и статистические закономерности в физике. Термодинамический и статистический методы. Элементы молекулярно-кинетической теории. Макроскопическое состояние. Физические величины и состояния физических систем. Макроскопические параметры как средние значения. Тепловое равновесие. Модель идеального газа. Уравнение состояния идеального газа. Понятие о температуре.
Тема 2
Явления переноса. Диффузия. Теплопроводность. Коэффициент диффузии. Коэффициент теплопроводности. Температуропроводность. Диффузия в газах, жидкостях и твердых телах. Вязкость. Коэффициент вязкости газов и жидкостей.
Тема 3
Элементы термодинамики. Первое начало термодинамики. Внутренняя энергия. Интенсивные и экстенсивные параметры.
Тема 4
Обратимые и необратимые процессы. Энтропия. Второе начало термодинамики. Термодинамические потенциалы и условия равновесия. Химический потенциал. Условия химического равновесия. Цикл Карно.
Тема 5
Функции распределения. Микроскопические параметры. Вероятность и флуктуации. Распределение Максвелла. Средняя кинетическая энергия частицы. Распределение Больцмана. Теплоемкость многоатомных газов. Ограниченность классической теории теплоемкости.
Тема 6
Распределение Гиббса. Модель системы в термостате. Каноническое распределение Гиббса. Статистический смысл термодинамических потенциалов и температуры. Роль свободной энергии.
Тема 7
Распределение Гиббса для системы с переменным числом частиц. Энтропия и вероятность. Определение энтропии равновесной системы через статистический вес микросостояния.
Тема 8
Функции распределения Бозе и Ферми. Формула Планка для разновесного теплового излучения. Порядок и беспорядок в природе. Энтропия как количественная мера хаотичности. Принцип возрастания энтропии. Переход от порядка к беспорядку о состоянии теплового равновесия.
Тема 9
Экспериментальные методы исследования колебательного спектра кристаллов. Понятие о фононах. Законы дисперсии для акустических и оптических фононов. Теплоемкость кристаллов при низких и высоких температурах. Электронные теплоемкость и теплопроводность.
Тема 10
Электроны в кристаллах. Приближение сильной и слабой связи. Модель свободных электронов. Уровень Ферми. Элементы зонной теории кристаллов. Функция Блоха. Зонная структура энергетического спектра электронов.
Тема 11
Поверхность Ферми. Число и плотность числа электронных состояний в зоне. Заполнения зон: металлы, диэлектрики и полупроводники. Электропроводность полупроводников. Понятие о дырочной проводимости. Собственные и примесные полупроводники. Понятие о p-n переходе. Транзистор.
Тема 12
Электропроводность металлов. Носители тока в металлах. Недостаточность классической электронной теории. Электронный ферми-газ в металле. Носители тока как квазичастицы. Явление сверхпроводимости. Куперовское спаривание электронов. Туннельный контакт. Эффект Джозефсона и его применение. Захват и квантование магнитного потока. Понятие о высокотемпературной проводимости.
СТАТИСТИЧЕСКАЯ ФИЗИКА. ТЕРМОДИНАМИКА
Основные формулы
1. Количество вещества однородного газа (в молях):
![]() ,
или
,
или
![]() ,
,
где N-число молекул газа; NA- число Авогадро; m-масса газа; -молярная масса газа.
Если система представляет смесь нескольких газов, то количество вещества системы
![]() ,
,
или
![]() ,
,
где i, Ni, mi, i -соответственно количество вещества, число молекул, масса, молярная масса i-й компоненты смеси.
2. Уравнение Клапейрона-Менделеева (уравнение состояния идеального газа):
![]()
где m - масса газа; - молярная масса; R - универсальная газовая постоянная; = m/ - количество вещества; T-термодинамическая температура Кельвина.
3. Опытные газовые законы, являющиеся частными случаями уравнения Клапейрона-Менделеева для изопроцессов:
закон Бойля-Мариотта
(изотермический процесс - Т=const; m=const):
![]() ,
,
или для двух состояний газа:
![]() ,
,
где p1 и V1 - давление и объем газа в начальном состоянии; p2 и V2 - те же величины в конечном состоянии;
закон Гей-Люссака (изобарический процесс - p=const, m=const):
![]()
или для двух состояний:
![]()
где V1 и Т1 - объем и температура газа в начальном состоянии; V2 и Т2 - те же величины в конечном состоянии;
закон Шарля (изохорический процесс - V=const, m=const):
![]()
или для двух состояний:
![]()
где р1 и Т1 - давление и температура газа в начальном состоянии; р2 и Т2 - те же величины в конечном состоянии;
объединенный газовый закон (m=const):
![]()
![]()
где р1, V1, Т1 - давление, объем и температура газа в начальном состоянии; р2, V2, Т2 - те же величины в конечном состоянии.
4. Закон Дальтона, определяющий давление смеси газов:
р = р1 + р2 + ... +рn
где pi - парциальные давления компонент смеси; n - число компонентов смеси.
5. Молярная масса смеси газов:
![]()
где mi - масса i-го компонента смеси; i = mi/i - количество вещества i-го компонента смеси; n - число компонентов смеси.
6. Массовая доля i i-го компонента смеси газа (в долях единицы или процентах):
![]()
где m - масса смеси.
7. Концентрация молекул (число молекул в единице объема):
![]()
где N-число молекул, содержащихся в данной системе; - плотность вещества. Формула справедлива не только для газов, но и для любого агрегатного состояния вещества.
8. Основное уравнение кинетической теории газов:
![]() ,
,
где <> - средняя кинетическая энергия поступательного движения молекулы.
9. Средняя кинетическая энергия поступательного движения молекулы:
![]() ,
,
где k - постоянная Больцмана.
10. Средняя полная кинетическая энергия молекулы:
![]() ,
,
где i - число степеней свободы молекулы.
11. Зависимость давления газа от концентрации молекул и температуры:
p = nkT.
12. Скорости молекул:
средняя
квадратичная
![]() ;
;
средняя
арифметическая
![]() ;
;
наиболее
вероятная
![]() ,
,
где mi - масса одной молекулы.
13. Относительная скорость молекулы:
u = v/ vв,
где v - скорость данной молекулы.
14. Удельные теплоемкости газа при постоянном объеме (сv) и при постоянном давлении (ср):
![]() ;
;
![]() .
.
15. Связь между удельной (с) и молярной (С) теплоемкостями:
![]() ;
C = c.
;
C = c.
16. Уравнение Роберта Майера:
Cp -Cv = R.
17. Внутренняя энергия идеального газа:
![]()
18. Первое начало термодинамики:
![]() ,
,
где Q - теплота, сообщенная системе (газу); dU - изменение внутренней энергии системы; А - работа, совершенная системой против внешних сил.
19. Работа расширения газа:
в
общем случае
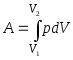 ;
;
при
изобарическом процессе
![]() ;
;
изотермическом
процессе
![]() ;
;
при
адиабатическом процессе
![]() ,
,
или
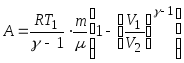 ,
,
где
![]() - показатель адиабаты.
- показатель адиабаты.
20. Уравнения Пуассона, связывающие параметры идеального газа при адиабатическом процессе:
![]() ;
;
 ;
;
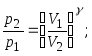
 ;
;
21. Термический к.п.д. цикла:
![]() ;
;
![]()
