
- •Расчёт δh˚298, δs˚298, δСр химической реакции по таблицам стандартных химических величин.
- •Результаты расчёта термодинамических функций δh˚t, δs˚t, δg˚t и ln(kp)
- •Точный расчёт термодинамических функций в интервале t1 – t2
- •V. Расчёт равновесных составов
- •Исследование вопроса о направлении реакции при температуре реакции t3 и давлении p.
- •Термодинамический анализ выхода реакции от давления и температуры.
- •Расчёт теплового эффекта достижения состояния равновесия реакционными смесями.
Вариант 16
Дано:
Уравнение реакции: COS+H2S=CS2+H2O
T1=1500 К
T2=2500 К
T3=2200 К
Р=2 атм.
Термодинамические данные:
|
вещество |
Агрегатное состояние |
ΔH˚298 Дж/моль |
ΔS˚298 Дж/(моль*К) |
Cp=a+bT+cT-2 |
||
|
a (Дж/К) |
b*103 (Дж/K2) |
c*10-5 (Дж/К) |
||||
|
COS |
g |
-141700 |
231.54 |
48.12 |
8.45 |
-8.20 |
|
CS2 |
g |
116700 |
237.77 |
52.09 |
6.69 |
-7.53 |
|
H2S |
g |
-29600 |
205.69 |
29.37 |
15.40 |
0.00 |
|
H2O |
g |
-241810 |
188.72 |
30.00 |
10.71 |
0.33 |
-
Расчёт δh˚298, δs˚298, δСр химической реакции по таблицам стандартных химических величин.
-- По закону Гесса, тепловой эффект химической реакции определяется только начальным и конечным состоянием вещества. ΔH реакции равен разности сумм энтальпий продуктов и реагентов реакции
ΔH˚298=( ΔH˚298(CS2)+ ΔH˚298(H2O)) - (ΔH˚298(H2S) +ΔH˚298(COS))
ΔH˚298=(116700 - 241810) - (-29600 – 141700)= 37190 Дж/моль
-- Изменение энтропии реакции равно, как и в первом случае, разности сумм энтропий продуктов и реагентов:
ΔS˚298=( ΔS˚298(CS2)+ ΔS˚298(H2O)) - (ΔS˚298(H2S) +ΔS˚298(COS))
ΔS˚298=(237.77 - 188.72) - (205.69 + 231.54)= -10,74 Дж/(моль*К)
-- Теплоёмкость вещества выражается в уравнении Cp=a+bT+cT-2, следовательно, ΔСр тоже функция температуры, выражающаяся как:
ΔCp=Δa+ΔbT+ΔcT-2 => ΔCp= 4.60 -6.45* 10-3 T+105 *T-2
-
Результаты расчёта термодинамических функций δh˚t, δs˚t, δg˚t и ln(kp)
-
ΔCp=0
ΔH˚T = ΔH˚298= 37190 Дж/моль
ΔS˚T = ΔS˚298= -10,74 Дж/(моль*К)
ΔG˚T = ΔH˚T – T*ΔS˚T
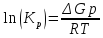
|
T,К |
∆H,Дж |
∆S,Дж/К |
∆G,Дж |
lnKp |
∆Cp,Дж/(моль*К) |
Kp |
|
1500 |
37190 |
-10,74 |
53300 |
-4,276 |
0 |
0,014 |
|
1600 |
37190 |
-10,74 |
54374 |
-4,090 |
0 |
0,017 |
|
1700 |
37190 |
-10,74 |
55448 |
-3,925 |
0 |
0,020 |
|
1800 |
37190 |
-10,74 |
56522 |
-3,779 |
0 |
0,023 |
|
1900 |
37190 |
-10,74 |
57596 |
-3,648 |
0 |
0,026 |
|
2000 |
37190 |
-10,74 |
58670 |
-3,530 |
0 |
0,029 |
|
2100 |
37190 |
-10,74 |
59744 |
-3,424 |
0 |
0,033 |
|
2200 |
37190 |
-10,74 |
60818 |
-3,327 |
0 |
0,036 |
|
2300 |
37190 |
-10,74 |
61892 |
-3,238 |
0 |
0,039 |
|
2400 |
37190 |
-10,74 |
62966 |
-3,157 |
0 |
0,043 |
|
2500 |
37190 |
-10,74 |
64040 |
-3,083 |
0 |
0,046 |
-
ΔCp= ΔC298 = 4.60 -6.45* 10-3 T+T-2 (T= 298 K)
ΔC298 = 3,804
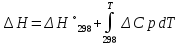
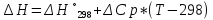
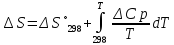
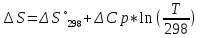
|
T,К |
∆H,Дж |
∆S,Дж/К |
∆G,Дж |
lnKp |
∆Cp,Дж/(моль*К) |
Kp |
|
1500 |
41762,378 |
-4,592 |
48650,818 |
-3,903 |
3,804 |
0,020 |
|
1600 |
42142,776 |
-4,347 |
49097,640 |
-3,693 |
3,804 |
0,025 |
|
1700 |
42523,174 |
-4,116 |
49520,672 |
-3,505 |
3,804 |
0,030 |
|
1800 |
42903,571 |
-3,899 |
49921,314 |
-3,337 |
3,804 |
0,036 |
|
1900 |
43283,969 |
-3,693 |
50300,813 |
-3,186 |
3,804 |
0,041 |
|
2000 |
43664,366 |
-3,498 |
50660,281 |
-3,048 |
3,804 |
0,047 |
|
2100 |
44044,764 |
-3,312 |
51000,722 |
-2,923 |
3,804 |
0,054 |
|
2200 |
44425,161 |
-3,135 |
51323,041 |
-2,807 |
3,804 |
0,060 |
|
2300 |
44805,559 |
-2,966 |
51628,064 |
-2,701 |
3,804 |
0,067 |
|
2400 |
45185,956 |
-2,804 |
51916,542 |
-2,603 |
3,804 |
0,074 |
|
2500 |
45566,354 |
-2,649 |
52189,166 |
-2,512 |
3,804 |
0,081 |
-
ΔCp= ΔCp((T1+T2)/2)= ΔCp(2000)
Cp= -8,275
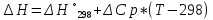
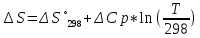
|
T,К |
∆H,Дж |
∆S,Дж/К |
∆G,Дж |
lnKp |
∆Cp,Дж/(моль*К) |
Kp |
|
1500 |
28915,00 |
-24,113 |
65085,175 |
-5,221 |
-8,275 |
0,005 |
|
1600 |
26415,95 |
-24,648 |
65851,960 |
-4,953 |
-8,275 |
0,007 |
|
1700 |
25588,45 |
-25,149 |
68342,048 |
-4,838 |
-8,275 |
0,008 |
|
1800 |
24760,95 |
-25,622 |
70880,840 |
-4,739 |
-8,275 |
0,009 |
|
1900 |
23933,45 |
-26,070 |
73465,628 |
-4,653 |
-8,275 |
0,010 |
|
2000 |
23105,95 |
-26,494 |
76093,989 |
-4,578 |
-8,275 |
0,010 |
|
2100 |
22278,45 |
-26,898 |
78763,742 |
-4,513 |
-8,275 |
0,011 |
|
2200 |
21450,95 |
-27,283 |
81472,914 |
-4,456 |
-8,275 |
0,012 |
|
2300 |
20623,45 |
-27,651 |
84219,713 |
-4,406 |
-8,275 |
0,012 |
|
2400 |
19795,95 |
-28,003 |
87002,502 |
-4,362 |
-8,275 |
0,013 |
|
2500 |
18968,45 |
-28,341 |
89819,780 |
-4,323 |
-8,275 |
0,013 |
