
- •Расчёт δh˚298, δs˚298, δСр химической реакции по таблицам стандартных химических величин.
- •Результаты расчёта термодинамических функций δh˚t, δs˚t, δg˚t и ln(kp)
- •Точный расчёт термодинамических функций в интервале t1 – t2
- •V. Расчёт равновесных составов
- •Исследование вопроса о направлении реакции при температуре реакции t3 и давлении p.
- •Термодинамический анализ выхода реакции от давления и температуры.
- •Расчёт теплового эффекта достижения состояния равновесия реакционными смесями.
-
Исследование вопроса о направлении реакции при температуре реакции t3 и давлении p.
Пусть в реакции
COS+H2S=CS2+H2O
|
вещество |
количество вещества (моль) |
мольные доли |
|
COS |
1 |
1/6 |
|
H2S |
1 |
1/6 |
|
CS2 |
2 |
1/3 |
|
H2O |
2 |
1/3 |
Как было выявлено выше, давления в уравнении константы равновесия сокращаются, следовательно, мольные доли реагентов не зависят от давления.
Выражаем константу равновесия:
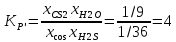
Чтобы определить равновесие реакции, запишем формулу изменения энергии Гиббса:
ΔGT3 = ΔG˚T3 + RT3ln(Kp’)
Подставляем численные значения:
ΔGT3 = 59931,939 + 2200*8.31*ln(4) = 85276,173 Дж
Энергия Гиббса больше нуля, следовательно, равновесие реакции будет смещено влево, в сторону образования исходных веществ.
-
Термодинамический анализ выхода реакции от давления и температуры.
От температуры:
Как видно, в графике изменения константы равновесия от температуры, KP увеличивается. Так как уравнение KP имеет вид:
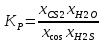
Значит, что мольные доли продуктов реакции увеличиваются, а реагентов – уменьшаются. Следовательно, чтобы повысить выход реакции, нужно повысить температуру.
Это объяснимо, с точки зрения закона Ле-Шателье – приведённая реакция эндотермическая, так как ΔH˚298>0. При повышении температуры, равновесие сместится в сторону образования продуктов, чтобы ослабить внешнее воздействие против увеличения температуры.
От давления:
Перепишем реакцию: COS+H2S=CS2+H2O
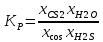
Константа равновесия от давления не зависит, но при изменении P, мольные доли веществ постоянны, следовательно, давление на выход реакции не влияет.
-
Расчёт теплового эффекта достижения состояния равновесия реакционными смесями.
-
Реагирует стехиометрическая смесь исходных веществ
COS+H2S=CS2+H2O
|
вещество |
количество вещества (моль) |
мольные доли |
|
COS |
1-z |
(1-z)/2 |
|
H2S |
1-z |
(1-z)/2 |
|
CS2 |
z |
z/2 |
|
H2O |
z |
z/2 |
Нам известно, что
z = 0,1622 моль
ΔH˚2200=30761,651 Дж/моль.
Следовательно, ΔH2200= 0,1622 * 30761,651 = 4989,54 Дж.
Реакция эндотермическая
-
Реагирует стехиометрическая смесь всех веществ
COS+H2S=CS2+H2O
|
вещество |
количество вещества (моль) |
мольные доли |
|
COS |
1-z |
(1-z)/4 |
|
H2S |
1-z |
(1-z)/4 |
|
CS2 |
1+z |
(z+1)/4 |
|
H2O |
1+z |
(z+1)/4 |
Нам известно, что
z = – 0,6755 моль
ΔH˚2200=30761,651 Дж/моль.
Следовательно, ΔH2200= – 0,6755 * 30761,651 = -20779,5 Дж.
Реакция экзотермическая
-
Расчёт условий P и T ( температур в интервале 1500-2500 К с шагом 100 К) , при которых сумма мольных долей газообразных продуктов составит не менее 0,8 при реакции стехиометрической смеси исходных веществ.
COS+H2S=CS2+H2O
|
вещество |
количество вещества (моль) |
мольные доли |
|
COS |
1-z |
(1-z)/2 |
|
H2S |
1-z |
(1-z)/2 |
|
CS2 |
z |
z/2 |
|
H2O |
z |
z/2 |
Составляем неравенство, где нужно найти z:
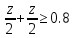
В
результате, выходит, что z
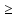 0.8 моль, так как двойки в выражении
сократятся. Подставляем выражение в
уравнение константы равновесия:
0.8 моль, так как двойки в выражении
сократятся. Подставляем выражение в
уравнение константы равновесия:
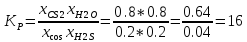
Стоит в очередной раз заметить, что мольные доли не зависят от давления, только от температуры среды, где реагирует газовая смесь COS и H2S
