
методички для лаб.раб. по молек. физике / Лабораторная работа №1
.docx
ИЗУЧЕНИЕ ТЕМПЕРАТУРНСЙ ЗАВИСИМОСТИ ДАВЛЕНИЯ НАСЫЩЕННЫХ ПАРОВ И ОПРЕДЕЛЕНИЕ СКРЫТОЙ ТЕПЛОТЫ ИСПАРЕНИЯ.
Составитель: Виталий Иванович Семихин
Ответственный за выпуск: А.Л.Болотов
Работа утверждена на заседании кафедры молекулярной физики от 6.06.83.
Печатается по решению учебно-методического совета университета.
Лабораторная работа составлена старшим преподавателем кафедры молекулярной физики В.И. Семихиным
Краткое содержание - экспериментально исследуется зависимость давления насыщенных паров жидкости от температуры в области значений давления и температуры, далеких от критических. Рассчитывается среднее значение скрытой теплоты парообразования.
ИЗУЧЕНИЕ ТЕМПЕРАТУРНОЙ ЗАВИСИМОСТИ ДАВЛЕНИЯ НАСЫЩЕННЫХ ПАРОВ И ОПРЕДЕЛЕНИЕ СКРЫТОЙ ТЕПЛОТЫ ИСПАРЕНИЯ.
КРАТКАЯ ТЕОРИЯ. Анализируя уравнение Ван-дер-Ваальса, можно видеть» что в определенном интервале температур и давлений жидкость и насыщенный пар над ней, помещенные в закрытый сосуд, могут находиться в равновесии. Это равновесие является динамическим, устанавливается само собой. С повышением температуры давление насыщенных паров увеличивается.
Характер
температурной зависимости давления
насыщенных паров определяется
уравнением Клапейрона - Клаузиуса.
(1)
где
L
-
молярная скрытая теплота испарения,
V2
- молярный объём тара, V1
-
молярный объём жидкости.
Уравнение (1) можно привести к виду: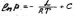
(2)
если рассматривать поведение насыщенных паров при давлениях и температурах, далёких от критических значений этих параметров. Зависимость натурального логарифма давления . насыщенных паров от 1/Т представляет собой прямую линию.

Рис 1.
Экспериментально получена зависимость давления насыщенных паров от температуры, можно, воспользовавшись уравнением (2), определить молярную скрытую теплоту испарения. Запишем уравнение (2) для двух давлений и температур (P2P1):
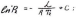
(3)
![]()
(4)
Исключая константу С из уравнений (3) и (4) находим молярную скрытую теплоту испарения:
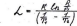
(5)
ОПИСАНИЕ УСТАНОВКИ.
Изучение зависимости давления насыщенных паров от температуры производится на установке, схема которой приведена на рис.2. Исследуемое вещество помещается в герметично закрывающийся сосуд 1. Давление пара, находящегося в равновесии с жидкостью, и соответствующая температура измеряются манометром 2 и термометром 3, закрепленным в крышке сосуда. Оставшийся в сосуде воздух откачивается с помощью вакуумного насоса 4 в течение 3-4 минут, затем вентиль 5 закрывается, отключая рабочий объём сосуда от окружающей атмосферы. После удаления воздуха из сосуда можно приступить к исследованию зависимости давления насыщенных паров от температуры. В нижней части сосуда помещён Нагреватель 6, напряжение на него подается от лабораторного трансформатора 7.
ИЗМЕРЕНИЯ И ОБРАБОТКА РЕЗУЛЬТАТОВ
После
удаления воздуха из сосуда можно
включить нагреватель, установив
напряжение на нём 100 В. В течение 40-50
минут снимают зависимость РН.П.
f
(Т),
затем напряжение надо повысить до 120
В и продолжить измерения. После
достижения температуры 110-115
0С,
нагрев прекращают и снимают РН.П.
от температуры при охлаждении сосуда
жидкостью.
В качестве
отчета необходимо представить график
зависимости РН.П.
от
температуры, график зависимости LnРН.П.
от l/Т,
величины,
обратной абсолютной температура, и
рассчитать по формуле (5) молярную
скрытую
теплоту испарения.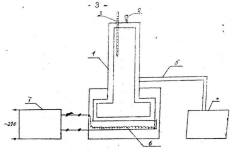
Рис. 2.
КОНТРОЛЬНЫЕ ВОПРОСЫ.
-
Что такое фаза, фазовое равновесие, фазовый переход?
-
Написать уравнение Ван-дер-Вальса и изобразить изотермы, соответствующие этому уравнению.
-
Что такое скрытая теплота испарения, скрытая теплота фазового перехода?
-
Вывести уравнение Клапейрона-Клаузиуса.
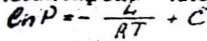
-
Вывести уравнение
