
Мотиторинг 2012
.pdf
Дворец детского (юношеского) творчества
“У Вознесенского моста” Адмиралтейский район
Исследовательская работа на тему:
МОНИТОРИНГ СОСТОЯНИЯ АТМОСФЕРНОГО ВОЗДУХА В АДМИРАЛТЕЙСКОМ РАЙОНЕ ГОРОДА САНКТ-ПЕТЕРБУРГА В 2006-2011 ГОДАХ
Авторы: ученик 77 школы 10 класса Гуляев Кирилл
Телефон 783-24-41, 89218918314
Руководитель:
к. х. н. Иванов Антон Рубенович
Санкт-Петербург
2012
Содержание
1. Введение |
3 |
2. Литературный обзор |
3 |
3. Материалы и методика выполнения работы |
5 |
3.1. Материалы и методика химического анализа |
5 |
3.1.1. Диоксид азота |
5 |
3.1.2. Углеводороды и монооксид углерода |
7 |
3.2. Количественный расчет транспортных источников |
|
NO2, СО и углеводородов |
8 |
3.3. Лихеноиндикация |
9 |
3.4. Методика расчета риска |
10 |
3.5. Метод расчета ожидаемого уменьшения продолжительности
жизни (УПЖ) населения за счет интоксикации |
10 |
|
4. |
Результаты и их обсуждение |
11 |
5. |
Итоги опросов жителей Адмиралтейского района. |
13 |
6. |
Выводы |
15 |
7. |
Литература |
16 |
8. |
Приложение |
17 |
1.Введение.
Втечение нескольких лет на базе ДДТ «У Вознесенского моста» в секции экологии ведутся наблюдения за состоянием атмосферного воздуха и здоровьем населения Адмиралтейского района. Цель данного исследования заключалась в продолжении мониторинга и анализа его результатов, сравнении с результатами прошлых лет. Для решения поставленной задачи нами использованы социологические опросы, а так же три способа оценки содержания опасных примесей в воздухе:
-полуколичественный химический анализ примесей в атмосферном воздухе;
-прямой подсчет транспортных источников диоксида азота, монооксида углерода и летучих органических соединений (ЛОС);
-лихеноиндикация токсичных примесей в воздухе.
2.Литературный обзор.
Адмиралтейский район, (площадь 1400 га, население 191,2 тыс. чел.) – исторический центр Санкт-Петербурга с высокой плотностью населения, в котором сосредоточены многочисленные памятники культуры и более 20 зон зеленых насаждений общей площадью 80 га
По оценкам специалистов, за период с 1990 по 2000 годы количество автомобилей в нашем городе возросло почти в десять раз и достигло к тому времени 1 миллиона единиц, а в 2006 году превысило 1,3 миллиона. Средняя суммарная интенсивность движения автотранспорта на улицах нашего города к 2007 году достигла 4500 единиц в час. Дорожная сеть СанктПетербурга представляет собой сочетание радиальной и прямоугольной систем, в которой, вплоть до последнего времени, не было обходных направлений. Из-за этого значительные транспортные потоки следуют через центр города по узким улицам, с частыми остановками перед светофорами, что оказывает негативное влияние на состояние атмосферного воздуха в этом районе города. Несмотря на принимаемые городской администрацией меры, в результате сочетания постоянно возрастающего количества автомобилей и неприспособленности инфраструктуры центра города к новым условиям, экологическая обстановка в Адмиралтейском районе за этот период ухудшалась. С 1997 по 2003 годы темп роста заболеваемости населения, связанной с расстройством органов дыхания, в районе составил 104-129%. Здоровье горожан - это фактор, который необходимо учитывать при любом обсуждении путей развития транспортной отрасли Санкт-Петербурга. [1-15] Высокая концентрация отравляющих веществ в воздухе напрямую связана с количественным увеличением автомобильного транспорта. Критерием количественной оценки опасности является предельно допустимая концентрация (ПДК) вещества. Так, за 2003 г. общее число автомобилей в Санкт-Петербурге выросло на 5,1%. Среднегодовая концентрация NO2 в воздухе Санкт-Петербурга в 2006 составила 1,4ПДКсс (среднесуточной), а
среднегодовая скорость прироста концентрации с 2000 г. к настоящему времени равна 0,11ПДКсс. Число проб воздуха, не отвечающих санитарным
нормам, выросло на 20% за этот период. Основные опасные примеси в воздухе района это: взвешенные вещества (пыль неизвестного состава) 1,4- 5,8 ПДК, оксид углерода (II) 0,5-4,0 ПДК, диоксид и монооксид азота 1,8-13,2
ПДК [8-10].
Однако наиболее опасным последствием загрязнения атмосферы продуктами сгорания бензина является возникновение смоговой ситуации в населенном пункте (городе). При условии, что температура воздуха превышает 20 0С, под действием солнечного излучения продукты неполного сгорания топлива и оксиды азота вступают в дальнейшее химическое взаимодействие. Продуктами этих превращений являются токсичные для человека, животных и растений органические пероксиды и озон. Впервые такой тип загрязнения атмосферы был описан в городе Лос-Анджелесе (США). Признаком его появления является голубоватая дымка, вызванная интенсивным аэрозолеобразованием. Причиной возникновения фотохимического смога в присутствии диоксида азота (NO2) является, как правило, образование вторичных загрязнителей из компонентов выхлопов автотранспорта, под действием солнечного излучения. Главным действующим фактором фотохимического смога является озон в концентрации свыше 3 мг/м3 и пероксиды. Их определение является задачей мониторинга атмосферы.
Среди последствий отравления продуктами сгорания топлива можно назвать: заболевания дыхательной системы, проявления аллергии, первично токсические реакции, ослабление иммунитета. Существует несколько способов определения этих веществ. Первый способ – использование высокоточных приборов принцип действия, которых, основан на таких свойствах газов, как теплопроводность, горючесть и других. Второй способ – использование химических реактивов, которые дают яркую окраску в присутствии анализируемых примесей. Этот метод называют колориметрией. Третий способ – метод прямого подсчета источников опасных примесей с последующими пересчетами на основании проведенных ранее испытаний на полигоне. Четвертый способ – это биоиндикация, в частности, по наличию лишайников, применяемый для определения присутствия оксидов азота и некоторых других примесей. [15-20].
Таблица 1. Предельно допустимые концентрации токсичных примесей в воздухе [2,3].
Компонент |
|
Углеводороды |
|
|
NO2 |
бензиновой |
СО |
|
|
фракции (пентан) |
|
ПДКсс, мг/м3 |
0,04 |
25,0 |
3,0 |
(среднесуточная) |
|
|
|
|
|
|
|
ПДКмр, мг/м3 |
0,085 |
100,0 |
5,0 |
(максимальная разовая) |
|
|
|
|
|
|
|
3.Материалы и методика выполнения работы
3.1.Материалы и методика химического анализа.
Пассивный пробоотбор проводился с помощью пробирок на 1 мл и изготовленных нами стеклянных трубок, заполненных инертным носителем с нанесенным индикатором (Приложение, иллюстрации 1,2).
Расчет содержания примесей в воздухе проводили по формуле:
__
C= a×m/(t×S×√T) |
(1), |
где С – концентрация компонента в воздухе, г /м3;
а – коэффициент, который составляет 0,21 для NO2; 1,72 для бензиновой фракции углеводородов (пентана); для СО: 0,07 – при определении по CrO3 2·10-3 – при определении по KMnO4 (см. ниже);
m – масса реагента – индикатора, г; t – время экспозиции, с;
S– площадь абсорбции, м2;
T– температура воздуха, К [16,17].
3.1.1. Диоксид азота
Нами были проведены серии экспериментов по подбору органических веществ для приготовления йод содержащего реактива, позволяющего селективно определять диоксид азота. Для этого необходимо было выполнить ряд требований:
-реактив должен хорошо смешиваться и с органическими веществами и с водой;
-реактив должен быть сильным восстановителем и взаимодействовать с йодом;
-компоненты реактива должны быть дешевы и доступны.
Врезультате выбора мы остановились на растворе камфары в этиловом спирте («Камфорный спирт 10%» продажный фармацевтический препарат)
Нами не обнаружены в литературе сведения, касающиеся взаимодействия камфары и йода. Однако понятно, что именно камфара и продукт ее взаимодействия с йодом являются активными компонентами
полученного нами реактива на NO2. Нагревание раствора йода с раствором соды не приводит к его обесцвечиванию, в тоже время нейтральной и кислой
средах спиртовой раствор камфары не взаимодействует с йодом.
По разработанной нами методике можно быстро и без значительных затрат приготовить тест для мониторинга NO2 в атмосфере.
Для изготовления индикатора присутствия диоксида азота в воздухе, нами были использованы в качестве реагентов следующие материалы: 1.раствор камфары в этиловом спирте «Камфорный спирт 10%» продажный фармацевтический препарат.
2.натрий двууглекислый, гидрокарбонат натрия (сода пищевая) 3.раствор йода в этиловом спирте 5%.
4.кислота уксусная водный раствор 9%
5.крахмал пищевой.
6.раствор перекиси водорода в воде 3%
7.нитрат кальция (кальциевая селитра, удобрение)
8.медная проволока
9.концентрированная серная кислота В качестве химической посуды были использованы пробирки, мерные
пробирки на 10 мл, стеклянные трубки, пипетки, стеклянные палочки для перемешивания, резиновые пробки, резиновые груши (для клизм).
Разработанная и использованная нами |
методика заключается в |
следующем: |
|
1.Приготовить насыщенный раствор гидрокарбоната натрия в воде
(рН=8,5).
2.Смешать 3 мл полученного раствора с 10 мл раствором камфары в этиловом спирте и 5 мл раствора йода в этиловом спирте.
3.Полученную смесь нагреть до кипения, при этом желтая окраска раствора йода исчезает, – смесь обесцвечивается.
4.Приготовить 2-3 мл жидкого крахмального клейстера и прибавить к нему такой же объем полученной в п. 3 смеси.
Тестирование полученного реагента газообразными смесями
производили с помощью резиновой груши. Оксиды азота получали нагреванием нескольких грамм нитрата кальция в присутствии 1 мл H2SO4 (конц.) и медной проволоки. В результате наблюдали посинение окраски в тестовом растворе - реакционной смеси.
Полученный нами раствор реагентов чувствителен к присутствующему в воздухе диоксиду азота и не реагирует на другие окислители. Это можно
объяснить тем, что содержащийся в нем восстановленный йод окисляется до I2 в кислой среде, а в щелочной и нейтральной реакция окисления не протекает. Вероятно, диоксид азота воздействует на йодсодержащий реагент, т.к. сам проявляет кислотные свойства – в водном растворе он образует азотную и азотистую кислоты:
2NO2 + H2O = HNO2 +HNO3.
При добавлении раствора Н2О2 к тестируемому реагенту в количестве 1мл и более не приводило к появлению окраски, однако, при этом раствор окрашивался в синий цвет при его подкислении уксусной кислотой до рН<5.
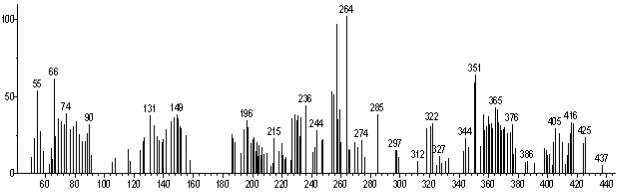
На рисунке 1 приведены результаты хромато-масс-спектрометрических исследований полученной реакционной смеси (масс-спектр).
Рисунок 1. Масс-спектр, полученный на приборе HP-5987A в результате исследований регента, использованного в качестве индикатора NO2 .
Дополнительно авторы проводили определение содержания окислителей в воздухе с применением метода обратного титрования щелочного раствора KI с помощью тест комплекта «Активный кислород» (производство фирмы «Крисмас плюс», Санкт-Петербург) а также скрининг NOx с помощью реактива Грисса по методике, описанной в [10].
3.1.2.Углеводороды и монооксид углерода
а). Перманганатный метод определения.
Реактивы: перманганат калия (KMnO4), 10% водный раствор серной кислоты. Порядок приготовления индикаторной смеси:
к 0,5 г перманганата калия добавляли 150 мл 10% раствора серной кислоты и перемешивали до полного растворения KMnO4. Полученный раствор использовали для пассивного пробоотбора при определении в воздухе непредельных летучих органических соединений (ЛОС) и СО. Индикация – по обесцвечиванию смеси.
б). Хроматный метод определения.
Реактивы: оксид хрома (VI) - CrO3, концентрированная серная кислота. Порядок приготовления индикаторной смеси:
к 0,5 г оксида хрома (VI) добавляли 50 мл H2SO4 (конц.) и перемешивали до полного растворения CrO3. Полученный раствор использовали для пассивного пробоотбора при суммарном определении летучих органических соединений и СО в воздухе. Индикация – переход окраски смеси от оранжевой к светло-зеленой.
Для большей корректности выполнения анализа примесей авторы наблюдали изменение рН воды в узкогорлом сосуде, выставленном на уличный воздух.
3.2. Количественный расчет транспортных источников NO2, СО и углеводородов.
1.Выбирали участок улицы с наиболее интенсивным транспортным потоком и провести учет этого потока за определенный промежуток времени.
Учет производился согласно условному делению автотранспорта на группы:
-грузовые автомобили с бензиновыми двигателями,
-грузовые автомобили с дизельными двигателями,
-автобусы с бензиновыми двигателями,
-автобусы с дизельными двигателями,
-легковые автомашины и микроавтобусы (с бензиновыми двигателями).
2.Расчет выбросов NO2, СО и углеводородов производили по формуле:
|
|
M=м·k·r |
(2), |
|
где |
|
|
|
|
M – масса примеси, в граммах, которая выделяется при работе двигателя |
||||
одного автомобиля в среднем, |
|
|
||
м |
- |
удельный выброс примеси автомобилем |
в г/км, |
приводимый в |
литературе [2,10], |
|
|
||
k |
- |
коэффициент, характеризующий выбросы NO2, СО и |
углеводородов |
|
при работе двигателя данного типа, |
|
|
||
r - коэффициент, учитывающий расход топлива данным типом автомобиля на 1 км пути движения.
3.Оценивали концентрации NO2, СО и углеводородов в городском воздухе исходя из полученного значения M, интенсивности потока автомобилей каждого типа и размеров «уличного каньона» на участке, где производили подсчет интенсивности движения автотранспорта [2].

3.3. Лихеноиндикация.
Рисунок 2. Важнейшие виды эпифитных лишайников [21]. Выполнение работы:
1.Выбрать зону зеленых насаждений, а в ней 5-10 взрослых деревьев одного вида, одного возраста, без повреждений, примерно равного диаметра, расположенных близко друг от друга.
2.Используя прозрачную полиэтиленовую пленку 10х10 см, с нанесенной сеткой из 100 клеток по 1 см, оценить какую площадь в % занимают лишайники на коре дерева.
3.Определить количество видов лишайников на коре деревьев.
4.Оценить степень загрязнения воздуха. Эпифитные лишайники чувствительны к присутствию в воздухе оксидов азота, озона, диоксида серы, фтористого водорода, а так же к присутствию соединений тяжелых металлов. Наличие более 5 видов лишайников и покрытие коры лиственных пород деревьев более чем на 20% соответствует содержанию токсичных примесей в концентрациях не превышающих ПДК, обеднение видового состава до 3 и уменьшение площади покрытия до 10% соответствует концентрациям примесей в районе ПДК, уменьшение количества видов лишайников до 1-2 говорит о некотором (в несколько процентов) превышении ПДК. Полное исчезновение данного типа организмов – лишайниковая пустыня – говорит о многократном (более чем в 2 раза) превышении ПДК опасных примесей в воздухе. (Приложение, иллюстрация 3) [21].
3.4. Методика расчета риска.
Риск интоксикации, по каждому компоненту R, |
рассчитывали по формуле: |
R= R1 • R2 |
(3), |
R1=P1• Q1 |
(4), |
где
R1 – риск хронической (кумулятивной) интоксикации;
P1=C/(C+ПДКсс) – вероятность интоксикации, отношение концентрации примеси к ее сумме со среднесуточной ПДК – кратность превышения (эффект), С – концентрация компонента в воздухе.
Q1=t/24 – отношение времени воздействия на субъект опасной примеси за 1 сутки, в часах, к 24 часам – мера ущерба (экспозиция);
R2=P2•Q2 |
(5), |
где
R2 - риск острой (моментальной) интоксикации;
P2=C/(C+ПДКмр) – вероятность интоксикации, отношение концентрации примеси к ее сумме с максимальной разовой ПДК – кратность превышения (эффект), С – концентрация компонента в воздухе;
Q2=exp(-ПДКмр/C) –мера ущерба в результате моментального токсического эффекта. [19, 20].
Для расчета по формуле (4) приняли для Q1=t/24 (отношение времени воздействия на субъект опасной примеси за 1 сутки, в часах) t= 2 часа. Общий минимальный риск оценивали, перемножая полученные значения R по каждому компоненту.
3.5. Метод расчета ожидаемого уменьшения продолжительности жизни (УПЖ) населения за счет интоксикации.
УПЖ=(П – П’) × R |
(6), |
где П = 68 лет (средняя продолжительность жизни)
П’ = 40 лет (средний возраст), R – оценочное значение риска. Откуда [19]:
УПЖ=28 R |
(7). |
