
- •1. Степени окисления элементов, их связь с положением элементов в Периодической системе. Классы неорганических соединений, номенклатура неорганических соединений.
- •2. Планетарная модель атома водорода Резерфорда; постулаты Бора.
- •3. Уравнение Де-Бройля, корпускулярно-волновые свойства микрообъектов (дуализм), принцип неопределенности Гейзенберга
- •4. Квантовые характеристики состояний электрона в атоме водорода (квантовые числа).
- •5. Электронное строение многоэлектронных атомов. Порядок заполнения орбиталей многоэлектронных атомов: принцип Паули, правило Хунда; s-, p-, d-элементы. Полные и неполные электронные аналоги.
- •6. Форма и пространственное расположение s-, p- и d- орбиталей в атоме.
- •7. Радиусы атомов, их изменение в периодах и группах Периодической системы. Зависимость кислотно-основных свойств соединения от радиуса центрального атома.
- •8.Энергия ионизации; сродство к электрону. Изменение в периодах и группах Периодической системы.
- •9. Электроотрицательность атомов элементов. Относительная электроотрицательность. Изменение в периодах и группах Периодической системы. Полярность химической связи,полярность молекул и ионов.
- •11. Ковалентная химическая связь. Особенности ковалентной связи: направленность и насыщаемость (приведите примеры).
- •12. Понятие о гибридизации атомных орбиталей и его применение для описания конфигурации молекул и ионов. Приведите примеры соединений.
- •2 Вариант:
- •13. Теория отталкивания σ-связывающих и неподелённых электронных пар и её применение для описания геометрической конфигурации молекул и ионов.
- •14. Структура Периодической системы элементов: периоды, группы, подгруппы, вставные декады. Взаимосвязь между электронной структурой атомов элементов и их положением в Периодической системе.
- •Стандартная энергия Гиббса образования δGо298 некоторых веществ
- •22. Динамический характер химического равновесия. Расчет констант химического равновесия, исходные и равновесные концентрации
- •23. Смещение химического равновесия при изменении концентраций реагентов, давления, температуры. Принцип Ле-Шателье.
- •24. Растворы как гомогенные системы. Гидраты, сольваты. Ненасыщенные, насыщенные и пересыщенные растворы
- •25. Электролитическая диссоциация веществ в растворах. Кислоты, основания, амфотерные гидроксиды, соли. Сильные и слабые электролиты.
- •26. Роль молекул растворителя в процессах электролитической диссоциации. Аквакомплексы металлов, их кислотные свойства.
- •27. Электролитическая диссоциация сильных и слабых электролитов в водных растворах. Вычисление концентраций ионов.
- •28. Электролитическая диссоциация воды. Ионное произведение воды. Водородный показатель.
- •29. Основные положения теорий кислот и оснований Аррениуса и Бренстеда-Лоури. Зависимость кислотно-основных свойств соединений от степени окисления центрального иона.
- •30. Амфотерность гидроксидов с точки зрения теории электролитической диссоциации (приведите примеры).
- •31. Равновесия в насыщенных растворах малорастворимых солей. Расчёт растворимости малорастворимой соли. Способы увеличения растворимости малорастворимых солей.
- •32. Гидролиз солей, образованных: а) сильным основанием и слабой кислотой; б) слабым основанием и сильной кислотой. Качественная оценка рН растворов гидролизующихся солей.
- •35. Стандартный ( нормальный) окислительно-восстановительный потенциал, определение напрвления о.-в. Реакции
- •36.Реакции самоокисления - самовосстановления (диспропорционирования). Внутримолекулярные окислительно – восстановительные процессы.
- •37. Уравнение Нерста. Влияние кислотности раствора на величину окислительно - восстановительного потенциала. Выбор среды для проведения окислительно-восстановительного процесса.
- •38. Координационные соединения. Центральный атом и лиганды, внутренняя и внешняя сферы комплексных соединений, координационное число.
- •39. Строение координационных соединений , гибридизация орбиталей центрального атома.
- •40. Изомерия комплексных соединений.
- •41. Равновесия в растворах комплексных соединений.
39. Строение координационных соединений , гибридизация орбиталей центрального атома.
Строение комплексных соединений рассматривают на основе координационной теории, предложенной в 1893 г. швейцарским химиком Альфредом Вернером, лауреатом Нобелевской премии. Его научная деятельность проходила в Цюрихском университете. Ученый синтезировал много новых комплексных соединений, систематизировал ранее известные и вновь полученные комплексные соединения и разработал экспериментальные методы доказательства их строения.
В соответствии с этой теорией в комплексных соединениях различают комплексообразователь, внешнюю и внутреннюю сферы. Комплексообразователем обычно является катион или нейтральный атом. Внутреннюю сферу составляет определенное число ионов или нейтральных молекул, которые прочно связаны с комплексообразователем. Их называют лигандами. Число лигандов определяет координационное число (КЧ) комплексообразователя. Внутренняя сфера может иметь положительный, отрицательный или нулевой заряд.
Остальные ионы, не разместившиеся во внутренней сфере, находятся на более далеком расстоянии от центрального иона, составляя внешную координационную сферу.
Если заряд лигандов компенсирует заряд комплексообразователя, то такие комплексные соединения называют нейтральными или комплексами-неэлектролитами: они состоят только из комплексообразователя и лигандов внутренней сферы. Таким нейтральным комплексом является, например, [Pt(NH3)2Cl2].
Гибридизация орбиталей — гипотетический процесс смешения разных (s, p, d) орбиталей центрального атома многоатомной молекулы с возникновением того же числа орбиталей, эквивалентных по своим характеристикам.
40. Изомерия комплексных соединений.
41. Равновесия в растворах комплексных соединений.
Диссациация комплексного соединения-сильного электролита на составляющие его ионы
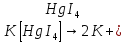 ]
]
[Pt(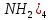 ]
]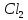 →[Pt(
→[Pt(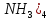 ]+2Cl
]+2Cl
Растворение происходит по ступеням.
Каждой
ступени присуща своя константа не
стойкости (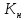 )
)
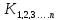 -парциальная
константа
-парциальная
константа
[Pt(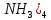 ]→[Pt(
]→[Pt(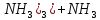 ,К1
,К1
[Pt(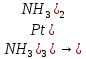 ]+
]+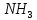 ,K2
,K2
[Pt(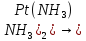 ]+
]+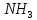 ,K3
,K3
[Pt(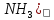 ]→Pt+
]→Pt+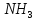 ,K4
,K4
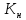 =
=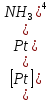 =K1*k2*k3*k4
=K1*k2*k3*k4
Чем меньше константа екустойчивости тем устойчивие соединение.
