
Осмолярность
Важной характеристикой среды является ее осмолярность, определяемая
концентрацией и константами диссоциации ее компонентов. Обычно осмолярность
равняется 285 мОсм/кг воды и соответствует таковой крови. Ооциты и эмбрионы
млекопитающих обычно культивируются в открытых системах с максимально
достижимой влажностью (80 - 90% в зависимости от модели CO2
-инкубатора), что предотвращает сильные колебания осмолярности в процессе
культивирования.
Качество воды
Основой любой культуральной среды является вода, качество которой во многом
определяет успех культивирования. Для питательных сред используется вода,
полученная после двойной дистилляции, ультрафильтрации либо деионизации. При
этом необходимо соблюдение полной стерильности в процессе ее приготовления
и хранения. Эндотоксины, выделяемые бактериями, оставшимися в среде после ее
ультрафильтрации, могут оказать токсическое воздействие на эмбрионы.To же
может произойти и при попадании бактерий в среду в процессе хранения.
Ионный состав
Ионный состав культуральных сред может сильно варьировать. Первые среды для
культивирования ооцитов и эмбрионов млекопитающих представляли собой
модификацию раствора Кребса. Они содержали ионы, необходимые для поддержания
жизни
клеток – Na+,
К+,
Са2+,
Mg2+,
![]()
и
![]() ,
растворенные в
,
растворенные в
бикарбонатном буфере (НCO3). Также добавлялись антибиотики для
предотвращения бактериального заражения и источник белка в форме альбумина или
сыворотки. Наиболее часто в качестве источника белка используется бычий или
человеческий сывороточный альбумин, а также инактивированная человеческая
сыворотка. Примерами таких сред могут служить Ml6, Т6, HTF (человеческая
трубная жидкость), EBSS (сбалансированный солевой раствор Эрла) и др. Более
сложные по составу среды, такие, как Ham's F10 и F12, aМЕМ, М199, хотя и были
разработаны для тканевых культур, но могут использоваться и для культивирования
эмбрионов различных видов млекопитающих.
Энергетическими субстратами для ооцитов и эмбрионов млекопитающих в
культуральной среде обычно служат пируват, лактат и глюкоза, причем
усвоение глюкозы эмбрионы человека начинают лишь до прошествии нескольких
клеточных делений, а до этого предпочтительным источником энергии служит
пируват.
Добавление аминокислот во многие культуральные среды объясняется их
присутствием в жидкости яйцеводов многих видов млекопитающих. Было показано,
что добавление глутамина в культуральную среду оказывает положительное
влияние на развитие эмбрионов многих видов млекопитающих. Однако при
введении в среду аминокислот надо иметь в виду, что не все они остаются
стабильны в условиях культивирования – при температуре 37С многие из них
разрушаются, образуя аммоний, который при накоплении в среде обладает
токсическим эффектом.
Специально для культивирования эмбрионов Menezo с соавт. была разработана
среда В2, гораздо более сложная по составу: помимо солей, она содержит
аминокислоты, витамины, нуклеотиды, микроэлементы и - в ряде случаев – даже
жирные кислоты. Все эти среды применяются в практике ЭКО в различных
лабораториях. При том, что роль многих компонентов сложных сред до сих пор
не была убедительно показана, их применение дает хорошие результаты.
CO2-ИНКУБАТОР
Культивирование ооцитов и эмбрионов человека проводится в присутствии 5% CO
3в воздухе при температуре 37±0,1 °С и влажности 80 – 90%. Эти условия
соблюдаются при использовании CO3-инкубаторов, поддерживающих
необходимую температуру, влажность и уровень CO2 в камере.
Последний параметр поддерживается посредством подачи углекислого газа из
баллона, где он находится в сжиженном состоянии, и воздуха из окружающей среды.
Углекислый газ для культивирования должен соответствовать медицинским
стандартам по чистоте. В некоторых клиниках применяется готовая газовая смесь,
содержащая углекислый газ, азот и кислород в нужной пропорции.
Влажность в камере CO3-инкубаторов поддерживается постоянным
испарением воды со дна камеры либо из специального лотка. Также в некоторых
современных инкубаторах имеется система инжекции воды в циркулирующий воздух,
позволяющая автоматически поддерживать влажность в камере до 90%.
В связи с высоким уровнем влажности в инкубаторах высок риск роста бактерий
и плесени, поэтому необходима регулярная очистка всех поверхностей камеры.
Как правило, для этой цели используют 70% этиловый спирт, однако делать это
надо с большой осторожностью, поскольку известно негативное влияние
этилового спирта на ооциты и ранние эмбрионы.
ИДЕНТИФИКАЦИЯ И ОЦЕНКА КАЧЕСТВА ООЦИТОВ
Во время трансвагинальной пункции (ТВП) преовуляторных фолликулов вместе с
фолликулярной жидкостью в пробирки попадают комплексы ооцит-cumulus. Cumulus
oophorus (яйценосный бугорок) представляет собой часть фолликулярного
эпителия, непосредственно контактирующую с ооцитом в процессе
фолликулогенеза. Помимо прочего фолликулярная жидкость содержит фибриноген,
что приводит к образованию кровяных сгустков уже через несколько минут после
аспирации. Если ооцит находится в таком сгустке, его будет достаточно сложно
обнаружить и впоследствии отмыть. Для преодоления этой проблемы используются
два основных подхода:
1. Фолликулярную жидкость просматривают под микроскопом сразу после
аспирации и найденные ооциты незамедлительно помещают в среду для отмывки.
2. Фолликулярную жидкость собирают в пробирки, содержащие среду с
гепарином, предотвращающую образование кровяных сгустков.
Как правило, в большинстве лабораторий руководствуются вторым подходом. При
этом используется гепарин в концентрации 50 МЕ/мл. Этот раствор в объеме 1 мл
добавляется в пробирки объемом 8 - 10 мл, что дает конечную концентрацию
гепарина в фолликулярной жидкости 5 - 8 МЕ/мл. Известно, что гепарин не
оказывает влияния на оплодотворение и последующее развитие эмбриона.
Комплексы ооцит-cumulus перед помещением в культуральную среду обязательно
отмывают в специальной среде.
После того как аспирированная фолликулярная жидкость попадает в
эмбриологическую лабораторию, она незамедлительно просматривается на
присутствие комплексов ооцит-cumulus. Для этого содержимое пробирок
переливается в чашки Петри диаметром 9 см и исследуется под стереомикроскопом
или инвертированным микроскопом при небольшом увеличении. Как правило,
комплексы ооцит-cumulus видны и невооруженным глазом как блестящие слизистые
комки или тяжи диаметром 0,5 – 1 см.
Найденные ооциты помещаются в среду для отмывки, содержащую HEPES-буфер,
позволяющий манипулировать с ооцитами на воздухе без риска изменения рН в
щелочную сторону (такие среды производятся большинством фирм,
специализирующихся на производстве сред для ЭКО), затем отмываются в
культуральной среде и помещаются в лунку 4-луночной чашки либо в специальную
чашку для ЭКО, где в дальнейшем будет проводиться оплодотворение ооцитов и
культивирование эмбрионов.
Также допускается культивирование в небольших (5 – 10 мкл) каплях среды,
покрытых слоем минерального масла, предварительно эквилиброванного с
культуральной средой в присутствии 5% С02. Преимуществами
культивирования под маслом являются: препятствование попаданию в культуральную
среду микроорганизмов и частичек пыли, возможность культивирования в
небольших каплях среды, что важно при оплодотворении спермой с небольшой
концентрацией активных сперматозоидов, а также замедление испарения воды и
выхода CO2 из среды вне инкубатора. Однако, если капли со средой
под маслом слишком долго находились вне инкубатора, возвращение к исходному
равновесию влажности и концентрации CO2 займет гораздо больше
времени, чем в отсутствие масла.
Манипуляции с ооцитами проводят с помощью оттянутых стерильных пастеровских
пипеток, имеющих небольшую резиновую грушу на конце, либо стеклянных
(пластиковых) капилляров, присоединенных к микроаспиратору. Существуют и
другие способы манипуляций с ооцитами и эмбрионами – выбор зависит от
опыта и желания эмбриолога.
Сразу после помещения ооцитов в культуральную среду необходимо оценить
количество, качество и степень зрелости полученных комплексов ооцит-cumulus.
Классификация комплексов ооцит-cumulus,
применяемая в клинике Bourn Hall, Кембридж
|
|
Ооцит |
Характеристика |
|
1 |
Очень незрелый |
Клетки cumulus и corona radiata плотно упакованы вокруг ооцита. Иногда можно увидеть ядро ооцита - зародышевый пузырек. Такой ооцит находится на стадии профазы первого деления мейоза (GV-germinal vesicle stage), на которой происходит блок мейоза в процессе оогенеза. Полярное тельце еще не сформировалось |
|
2 |
Незрелый |
Клетки corona radiata все еще плотно примыкают к ооциту, cumulus незначительно увеличился. Такой ооцит обычно находится на стадии метафазы первого деления мейоза (М I), блок мейоза уже снят, однако формирование полярного тельца пока не произошло |
|
3 |
Преовуляторный |
Клетки corona radiala расходятся лучами от ооцита, cumulus разросшийся, но имеет клеточную структуру. Ооцит находится на стадии метафазы второго деления мейоза (М II), Полярное тельце уже сформировано |
|
4 |
Перезрелый |
Присутствует небольшое количество клеток corona radiata, уже не примыкающих плотно к ооциту, который хорошо просматривается. Cumulus разросшийся, но все еще имеет клеточную структуру. Полярное тельце обычно хорошо видно |
|
5 |
Лютеинизированный |
Вокруг ооцита клетки cumulus образуют скопления (комки), остальной cumulus представляет собой желеобразную массу с небольшим количеством клеток |
|
6 |
Дегенеративный |
Несколько клеток гранупезы окружают ооцит, cumulus отсутствует или очень маленький. Ооцит обычно темноокрашен |
Оценка степени зрелости ооцитов по состоянию комплексов ооцит-cumulus, как
правило, субъективна и часто не отвечает истинному состоянию ооцита.
Асинхронность в созревании ядра ооцита, ооплазмы и клеток cumulus достаточно
часто встречается в циклах стимуляции суперовуляции при ЭКО. Однако более
точное определение степени зрелости (если клетки corona radiata и cumulus
удаляют ферментативно или механически) может привести к травматизации ооцита
и увеличению риска полиспермии при оплодотворении.
На рис.2 представлены данные по распределению ооцитов, полученных в ходе
стимуляции суперовуляции, по степени зрелости. Оценка производилась после
удаления клеток cumulus.
|

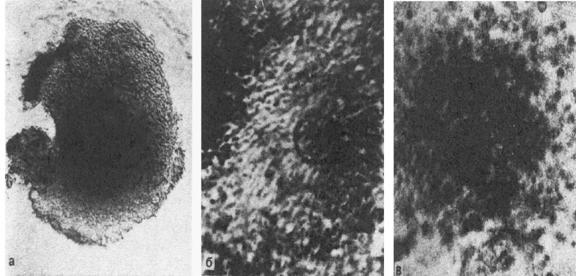
Рис.3. Ооцитарно-фолликулярные комплексы.
а – незрелый; б – зрелый; в – перезревающий. Микрофотографии живых объектов
в фазовом контрасте.
ОБРАБОТКА СПЕРМЫ ПЕРЕД
ОПЛОДОТВОРЕНИЕМ ООЦИТОВ in vitro
Эякулят для ЭКО получают путем мастурбации в стерильный контейнер. После
полного разжижения спермы, происходящего при комнатной температуре через 30 -
60 мин, приступают к ее обработке. Предварительно необходимо провести анализ
концентрации сперматозоидов, их подвижности и морфологических характеристик
по стандартной методике ВОЗ.
Перед тем как добавлять сперму в культуральную среду с ооцитами, необходимо
ее обработать в целях удаления семенной плазмы и получения максимально
полноценной фракции прогрессивно подвижных сперматозоидов. На практике
применяются два основных метода обработки спермы - центрифугирование-
флотация (процедура swim-up) и градиентное центрифугирование.
При использовании методики swim-up 1 – 2 мл спермы помещают в коническую 10 –
15-миллиметровую пробирку, добавляют 5 - 10 мл среды для отмывки
* и центрифугируют 5 – 10 мин при ускорении 1200 g. Затем супернатант
удаляют, осадок ресуспендируют в 2 – 3 мл среды и вновь центрифугируют. После
удаления супернатанта 1 – 2 мл свежей среды осторожно наслаивают на осадок,
пробирку помещают в CO2-инкубатор при 37°С на 30 – 60 мин. В течение
этого времени подвижные сперматозоиды должны мигрировать в наслоенную среду,
оставив на дне пробирки неподвижные сперматозоиды, дебрис и иные клетки. Если
пробирки будут установлены наклонно, увеличится площадь контакта осадка со
средой и, соответственно, выход подвижных сперматозоидов. Для определения
концентрации и подвижности сперматозоидов в надосадочной жидкости берется
аликвота 10 или 50 мкл. Затем необходимое количество чистого супернатанта
используется для инсеминации.
Важным шагом вперед в методике обработки спермы стало внедрение метода
центрифугирования в градиенте Перколла. Перколл представляет собой суспензию
силиконовых гранул 15 – 30 нм в диаметре, покрытых слоем поливинилпирролидона
(PVP), поскольку в чистом виде они токсичны для клеток. Особенностью Перколла
является очень низкая осмолярность – 25 мОсм/л, поэтому при разведении в
среде до различных концентраций, соответствующих различным плотностям (от
1,01 до 1,13 г/л), осмолярность растворов остается постоянной. Растворы
Перколла (40 и 90%) готовятся из 100% раствора, представляющего собой смесь 9
частей Перколла и 1 части 10-кратно концентрированной среды для отмывки.
Прерывистый градиент плотности достигается путем помещения 1,5 мл 40%-го
Перколла на 1,5 мл 90%-го в конической пробирке; сверху аккуратно
наслаивается сперма (1 – 2 мл), и вся эта трехслойная колонка
центрифугируется 15 мин при ускорении 700 g. После центрифугирования в осадок
попадают только функционально нормальные сперматозоиды; неподвижные и
аномальные сперматозоиды, а также лейкоциты и другие клетки спермы
задерживаются на границе 40 и 90%-q фракций. Осадок отбирается пастеровской
пипеткой и два раза отмывается в специальной среде, как и в случае
применения методики swim-up (см. выше).
Последний метод, по мнению многих авторов, является более предпочтительным,
сочетая в себе хорошую сепарацию и высокий выход фертильных сперматозоидов.
Кроме того, описано и защитное действие Перколла: он не позволяет попасть в
осадок дефектным сперматозоидам, лейкоцитам и другим клеткам спермы,
производящим большое количество свободных радикалов, способных повреждать
мембраны сперматозоидов. Таким образом, чем более благоприятно соотношение
жизнеспособных сперматозоидов и дефектных, тем меньше вероятность
повреждений первых.
ОПЛОДОТВОРЕНИЕ ООЦИТОВ in vitro
Много споров и разночтений вызывает вопрос о времени введения сперматозоидов
в среду, где культивируются ооциты. Наиболее общепринятым считается, что
между выделением первого полярного тельца ооцита (достижением стадии М II) и
добавлением спермы должно пройти около 4 ч, тогда способность такого ооцита к
оплодотворению и последующему дроблению будет максимальной.
Преовуляторный фолликул на момент аспирации (обычно 36 ч после введения
хорионического гонадотропина - ХГ, имитирующего пик эндогенного ЛГ в момент
овуляции при естественном цикле), как правило, содержит ооцит на стадии М
II. В естественных условиях овуляция, а значит, и возможность оплодотворения
наступает через 38 - 40 ч после пика ЛГ.
На практике преинкубация ооцитов перед инсеминацией составляет от 2 до 6 ч.
Данные по влиянию времени инкубации на оплодотворяемость ооцитов, дробление
эмбрионов и беременность разноречивы. По данным К. Yanagida с соавт.,
исследовавших такую зависимость при инкубации ооцитов в течение 1 - 11 ч
перед оплодотворением (применялся метод интрацитоплазматической
микроинъекции сперматозоида в яйцеклетку - ИКСИ), способность ооцитов к
оплодотворению, последующему дроблению и имплантации статистически
достоверно снижается при инкубации их более 9 ч. Достоверных различий при
инкубации в течение 1 - 9 ч не было обнаружено. В другом исследовании было
показано, что инкубация более 9 ч перед оплодотворением наиболее оптимальна
для последующего прохождения всех вышеуказанных процессов при ИКСИ;
исследователи предполагают, что это связано с дозреванием цитоплазмы ооцита,
необходимым для его активации при оплодотворении.
Важным моментом в обеих работах является то, что инкубация ооцитов
происходила в присутствии клеток cumulus и corona radiata. Известно, что
созревание ооцита полностью зависит от окружающих клеток фолликулярного
эпителия, поставляющих в ооплазму РНК и белки, необходимые для развития
будущего организма до включения его собственного генома, а также белковые
факторы, отвечающие за процесс оплодотворения. Было показано, что дозревание
ооцитов in Ditro со стадии GV до стадии МII при интактном cumulus
происходило с большей вероятностью, причем последующее их оплодотворение и
дробление было лучше.
Несмотря на расхождение данных, большинство авторов считает, что
преинкубация обязательно необходима, а ее оптимальная длительность
подбирается эмпирически в каждой лаборатории. При этом окно оплодотворения
для зрелого ооцита достаточно широко, однако преждевременное оплодотворение
недозревших ооцитов может негативно повлиять на исход дробления и имплантации
эмбрионов.
Помимо фактора времени, в инсеминации важным является и количественный
фактор. Количество прогрессивно подвижных сперматозоидов обычно должно
составлять 50 - 100 тыс. на 1 мл среды (при культивировании в относительно
большом объеме среды) либо на ооцит (при культивировании в микрокаплях под
минеральным маслом). Подбирая концентрацию сперматозоидов при
оплодотворении ооцитов in vitro, нужно иметь в виду, что при добавлении
менее 50 тыс. активно подвижных сперматозоидов на 1 мл частота оплодотворения
будет существенно снижена, а при использовании очень высоких концентраций
возникают побочные эффекты: полиспермия (проникновение более одного
сперматозоида в ооцит при оплодотворении), снижение жизнеспособности
полученных эмбрионов (за счет повреждения кислородными радикалами, при
попадании погибающих или мертвых сперматозоидов, либо воздействия
избыточного количества литических акросомальных ферментов).
Однако это правило реализуется лишь в случае нормальной морфологии
сперматозоидов, при наличии необходимой концентрации активно подвижных
сперматозоидов в эякуляте, отсутствии дефектов акросомальной реакции или
отсутствии больших концентраций антиспермальных антител в сперме (MAR-тест
менее 50%). При наличии этих и других отрицательных факторов, а также при
неудаче оплодотворения в предыдущей попытке ЭКО концентрация сперматозоидов
может быть повышена путем снижения объема среды культивирования
(культивирование в микрокаплях, соломках для криоконсервации,
микрокапиллярах), однако это далеко не всегда приводит к желаемым
результатам. Для облегчения проникновения сперматозоида в ооцит клетки
cumulus и corona radiata могут быть удалены ферментативно и механически,
однако это повышает риск полиспермии.
