
Тема 4. II закон рауля для растворов неэлектролитов
4–1. Растворитель замерзает при tзам. р-ля °C, а его криоскопическая константа составляет Кк K∙кг/моль. При какой температуре замерзнет раствор, содержащий n моль неэлектролита A в m г растворителя?
Решение.
cm
![]() ,
,
где cm – моляльная концентрация A, моль/кг; n – количество вещества A, моль; 1000 г/кг – пересчетный коэффициент m – физическая масса растворителя, г.
Согласно второму закону Рауля для растворов неэлектролитов
Тзам = Кк∙cm,
где Тзам – понижение температуры замерзания раствора относительно растворителя, К; Кк – криоскопическая константа растворителя, К·кг/моль.
tзам. р-ра = tзам. р-ля – Тзам,
где tзам. р-ра – искомая температура замерзания раствора, °C; tзам. р-ля – температура замерзания растворителя, °C.
4–2. Определите температуру замерзания ω %-ного водного раствора неэлектролита A. Криоскопическая константа воды равна Кк K∙кг/моль.
Решение.
![]()
где m1 – физическая масса A в 100 г раствора, г; ω – массовая доля A, %.
![]()
где n – количество вещества A в 100 г раствора, моль; M – молярная масса A, г/моль.
![]() ,
,
где m – физическая масса воды в 100 г раствора, кг; 1000 г/кг – пересчетный коэффициент.
cm
![]() ,
,
где cm – моляльная концентрация A, моль/кг.
Согласно второму закону Рауля для растворов неэлектролитов
Тзам = Кк∙cm,
где Тзам – понижение температуры замерзания раствора относительно воды, К; Кк – криоскопическая константа воды, К·кг/моль.
tзам. р-ра = tзам. воды – Тзам,
где tзам. р-ра – искомая температура замерзания раствора, °C; tзам. воды – температура замерзания воды, °C.
4–3. Сколько г неэлектролита A надо растворить в V л воды, чтобы приготовленный антифриз замерзал при tзам. р-ра °C? Криоскопическая константа воды равна Кк K∙кг/моль.
Решение.
Тзам = tзам. воды – tзам. р-ра,
где Тзам – понижение температуры замерзания раствора относительно воды, К; tзам. воды – температура замерзания воды, °C; tзам. р-ра – температура замерзания раствора, °C.
Согласно второму закону Рауля для растворов неэлектролитов
Тзам
= Кк∙cm
, откуда
 ,
,
где cm – моляльная концентрация A, моль/кг; Кк – криоскопическая константа растворителя, К·кг/моль.
cm
![]() ,
откудаn
= cm∙V∙ρ,
,
откудаn
= cm∙V∙ρ,
где n – количество вещества A, моль; m2 – физическая масса воды, г; V – объем воды, л; ρ – плотность воды, г/л.
m1 = n∙M,
где m1 – искомая физическая масса A, г; M – молярная масса A, г/моль.
4–4. Раствор, содержащий m1 мг неэлектролита A в m2 г растворителя, замерзает при tзам. р-ра °C. Криоскопическая константа растворителя равна Кк K∙кг/моль, а температура его замерзания составляет tзам. р-ля °C. Найдите молярную массу А.
Решение.
Тзам = tзам. р-ля – tзам. р-ра,
где Тзам – понижение температуры замерзания раствора относительно растворителя, К; tзам. р-ля – температура замерзания растворителя, °C; tзам. р-ра – температура замерзания раствора, °C.
Согласно второму закону Рауля для растворов неэлектролитов
Тзам
= Кк∙cm,
откуда
 ,
,
где cm – моляльная концентрация A, моль/кг; Кк – криоскопическая константа растворителя, К·кг/моль.
cm
![]() ,
откуда
,
откуда ,
,
где M – искомая молярная масса A, г/моль; n – количество вещества A, моль; 1000 г/кг и 1000 мг/г – пересчетные коэффициенты; m2 – физическая масса растворителя, г; m1 – физическая масса А, мг.
4–5. Для приготовления антифриза на V1 л воды взято V2 л неэлектролита A (плотность A равна ρ2 г/мл). Криоскопическая константа воды равна Кк K∙кг/моль. Найдите температуру замерзания антифриза.
Решение.
m1 = V1∙ρ1,
где m1 – физическая масса воды, кг; V1 – объем воды, л; ρ1 – плотность воды, кг/л.
m2 =1000∙V2∙ρ2,
где m2 – физическая масса А, г; 1000 мл/л – пересчетный коэффициент; V2 – объем А, л; ρ2 – плотность А, г/мл.
cm
![]() ,
,
где cm – моляльная концентрация A, моль/кг; n – количество вещества A, моль; M – молярная масса A, г/моль.
Согласно второму закону Рауля для растворов неэлектролитов
Тзам = Кк∙cm,
где Тзам – понижение температуры замерзания раствора относительно воды, К; Кк – криоскопическая константа воды, К·кг/моль.
tзам. р-ра = tзам. воды – Тзам,
где tзам. р-ра – искомая температура замерзания раствора (антифриза), °C; tзам. воды – температура замерзания воды, °C.
4–6. При какой температуре замерзает ω %-ный водный раствор неэлектролита A. Криоскопическая константа воды равна Кк K∙кг/моль.
Решение.
См. 4–2.
4–7. Водный раствор, содержащий m1 г растворенного неэлектролита в m г раствора, замерзает при tзам. р-ра °C. Криоскопическая константа воды равна Кк K∙кг/моль. Найдите молекулярную массу вещества.
Решение.
Тзам = tзам. воды – tзам. р-ра,
где Тзам – понижение температуры замерзания раствора относительно воды, К; tзам. р-ля – температура замерзания воды, °C; tзам. р-ра – температура замерзания раствора, °C.
Согласно второму закону Рауля для растворов неэлектролитов
Тзам
= Кк∙cm,откуда
 ,
,
где cm – моляльная концентрация A, моль/кг; Кк – криоскопическая константа воды, К·кг/моль.
cm
![]() ,
откуда
,
откуда ,
,
где M – молярная масса A, г/моль; n – количество вещества A, моль; 1000 г/кг – пересчетный коэффициент; m и m1 – физические массы раствора и А, г;.
![]() ,
,
где Mr – искомая молекулярная масса А, а.е.м.
4–8. Определите температуру кипения ω %-ного водного раствора неэлектролита A. Эбулиоскопическая константа воды равна Кэ K∙кг/моль.
Решение.
m1 = ω,
где m1 – физическая масса A в 100 г раствора A, г; ω – массовая доля A, %.
n
![]() ,
,
где n – количество вещества А в 100 г раствора A, моль; M – молярная масса A, г/моль.
![]()
где m – физическая масса воды в 100 г раствора, кг; 1000 г/кг – пересчетный коэффициент.
cm
![]() ,
,
где cm – моляльная концентрация A, моль/кг.
Согласно второму закону Рауля для растворов неэлектролитов
Ткип = Кэ∙cm,
где Ткип – повышение температуры кипения раствора относительно воды, К; Кэ – эбулиоскопическая константа воды, К·кг/моль.
tкип. р-ра = tкип. воды + Ткип,
где tкип. р-ра – искомая температура кипения раствора, °C; tкип. воды – температура кипения воды, °C.
4–9. Найдите температуру кипения раствора, содержащего m1 г неэлектролита А в m2 г растворителя. Эбулиоскопическая константа растворителя Кэ K∙кг/моль, а его температура кипения tкип. р-ля °C.
Решение.
![]()
где n1 – количество вещества A, моль; m1 – физическая масса A, г; M1 – молярная масса A, г/моль.
cm
![]() ,
,
где cm – моляльная концентрация A, моль/кг; 1000 г/кг – пересчетный коэффициент; m2 – физическая масса растворителя, г.
Согласно второму закону Рауля для растворов неэлектролитов
Ткип = Кэ∙cm.
где Ткип – повышение температуры кипения раствора относительно растворителя, К; Кэ – эбулиоскопическая константа растворителя, К·кг/моль.
tкип. р-ра = tкип. р-ля + Ткип,
где tкип. р-ра – искомая температура кипения раствора, °C; tкип. р-ля – температура кипения растворителя, °C.
4–10. Раствор, содержащий m1 г неэлектролита А в m2 г воды, кипит при tкип. р-ра °C. Эбулиоскопическая константа воды равна Кэ K∙кг/моль. Определите молекулярную массу вещества.
Решение.
Ткип = tкип. р-ра – tкип. воды,
где Ткип – повышение температуры кипения раствора относительно воды, К; tкип. р-ра – температура кипения раствора, °C; tкип. воды – температура кипения воды, °C.
Согласно второму закону Рауля для растворов неэлектролитов
Ткип
= Кэ∙cm,
откуда
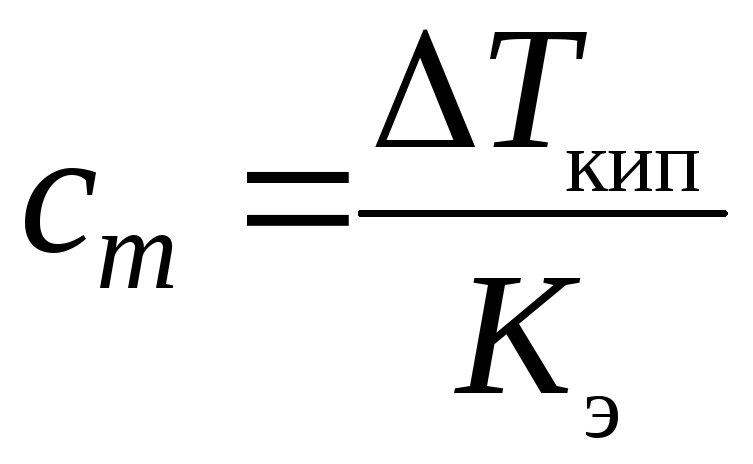 ,
,
где cm – моляльная концентрация А, моль/кг; Кэ – эбулиоскопическая константа, К·кг/моль.
cm
![]() ,
откуда
,
откуда![]() ,
,
где n – количество вещества Ax, моль; 1000 г/кг – пересчетный коэффициент; m2 – физическая масса воды, г.
![]() ,
,
где M – молярная масса A, г/моль.
![]() ,
,
где Mr – искомая молекулярная масса А, а.е.м.
4–11. Раствор, содержащий m1 г неэлектролита Ax в m2 г растворителя, кипит при tкип. р-ра °C. Температура кипения растворителя tкип. р-ля °C, а его эбулиоскопическая константа равна Kэ K∙кг/моль. Определите состав молекулы Ax.
Решение.
Ткип = tкип. р-ра – tкип. р-ля,
где Ткип – повышение температуры кипения раствора относительно растворителя, К; tкип. р-ра – температура кипения раствора, °C; tкип. р-ля – температура кипения растворителя, °C.
Согласно второму закону Рауля для растворов неэлектролитов
Ткип
= Кэ∙cm,
откуда
 ,
,
где cm – моляльная концентрация Ax, моль/кг; Кэ – эбулиоскопическая константа, К·кг/моль.
cm
![]() ,
откуда
,
откуда![]() ,
,
где n – количество вещества Ax, моль; 1000 г/кг – пересчетный коэффициент; m2 – физическая масса растворителя, г.
![]() ,
,
где M – молярная масса Ax, г/моль.
![]() ,
,
где x – число атомов А в молекуле Ax; M(А) – молярная масса A, г/моль.
4–12. Температура кипения раствора, состоящего из m1 неэлектролита A и m2 г растворителя, равна tкип. р-ра °C. Эбулиоскопическая константа растворителя составляет Kэ K∙кг/моль, а кипит растворитель при tкип. р-ля °C. Найдите молярную массу неэлектролита.
Решение.
См. 4–11.
4–13. Определите температуру кипенияраствора, содержащего m1 г неэлектролита А в m2 г растворителя. Эбулиоскопическая константа растворителя Кэ K∙кг/моль, а его температура кипения tкип. р-ля °C.
Решение.
См. 4–9.
4–14. Растворитель кипит при tкип. р-ля °C, а его эбулиоскопическая константа составляет Кэ K∙кг/моль. При какой температуре закипит ω%-ный раствор неэлектролита А в растворителе?
Решение.
m1 = ω,
где m1 – физическая масса A в 100 г раствора A, г; ω – массовая доля A, %.
![]()
где n – количество вещества A в 100 г раствора, моль; M – молярная масса A, г/моль.
![]()
где m – физическая масса растворителя в 100 г раствора, кг; 1000 г/кг – пересчетный коэффициент.
cm
![]() ,
,
где cm – моляльная концентрация A, моль/кг.
Согласно второму закону Рауля для растворов неэлектролитов
Ткип = Кэ∙cm,
где Ткип – повышение температуры кипения раствора относительно растворителя, К; Кэ – эбулиоскопическая константа растворителя, К·кг/моль.
tкип. р-ра = tкип. р-ля + Ткип,
где tкип. р-ра – искомая температура кипения раствора, °C; tкип. р-ля – температура кипения растворителя, °C.
4–15. В скольких граммах воды надо растворить m г неэлектролита А, чтобы приготовленный раствор замерзал при tзам. р-ра °C? Криоскопическая константа воды равна Кк K∙кг/моль.
Решение.
Тзам = tзам. воды – tзам. р-ра,
где Тзам – понижение температуры замерзания раствора относительно воды, К; tзам. воды – температура замерзания воды, °C; tзам. р-ра – температура замерзания раствора, °C.
Согласно второму закону Рауля для растворов неэлектролитов
Тзам
= Кк∙cm,
откуда
 ,
,
где cm – моляльная концентрация A, моль/кг; Кк – криоскопическая константа растворителя, К·кг/моль.
cm
![]() ,
откудаm1
,
откудаm1
![]() ,
,
где m1 – искомая физическая масса воды, г; n – количество вещества A, моль; m – физическая масса неэлектролита А, г; M – молярная масса A, г/моль.
4–16. . Определите температуру замерзания ω %-ного водного раствора неэлектролита A. Криоскопическая константа воды равна Кк K∙кг/моль.
Решение.
См. 4–2.
