
Ado_A_D_Patologicheskaya_fiziologia
.pdfции. Лишенные афферентного контроля нейроны дорсальных рогов ге нерируют длительные самоподдерживающие разряды, что вызывает ощу щение боли.
Таламический синдром развивается при повреждениях таламуса, вызванных чаще всего тромбозом сосудов, снабжающих заднебоковые отделы зрительного бугра. Характеризуется расстройством движений и нарушением (извращением) всех видов соматической чувствительности на стороне, противоположной повреждению. Возникающие при этом боли имеют диффузный характер и чрезвычайно сильную негативную эмоцио нальную окраску. Полагают, что таламические боли появляются в резуль тате нарушения баланса между ноцицептивными и неноцицептивными импульсами, поскольку на таламических нейронах конвергируют пути про ведения различных видов чувствительности.
Боль и мышечный тонус. Вызванное разными причинами длитель ное усиление тонуса скелетных мышц сопровождается болью, которая обусловлена возбуждением мышечных ноцицепторов алгезирующими агентами, накапливающимися в мышце при ее длительном сокращении — брадикинином, серотонином, простагландинами, ионами водорода. Воз буждение ноцицепторов в свою очередь рефлекторно усиливает мышеч ное напряжение, создавая тем самым порочный круг, способствующий сохранению боли. Подобный механизм действует, в частности, при неко торых видах головной боли.
Глава 15. Патологическая физиология эндокринной системы
В зависимости от локализации и характера процесса механизмы нарушения функции желез внутренней секреции могут быть различны ми Можно выделить три основных патогенетических пути.
1)нарушение центральных механизмов регуляции функции железы;
2)патологические процессы в самой железе и
3)периферические (внежелезистые) механизмы нарушения актив ности гормонов.
15.1. Нарушение центральных механизмов регуляции
Частыми причинами, приводящими к нарушению гипоталамической регуляции функции желез внутренней секреции, являются инфек ционные и воспалительные процессы, сосудистые и травматические по вреждения, опухоли. Патологические процессы, первично развивающиеся в гипоталамусе, ведут к нарушению трансгипофизарной и парагипофизарной регуляции функции желез внутренней секре ции. Деятельность гипоталамических центров может нарушаться и вто рично в связи с нарушениями в лимбической системе (гиппокамп, миндалина, обонятельный мозг) и вышележащих этажах центральной нервной системы, которые тесно связаны с гипоталамусом. Здесь не обходимо отметить большую роль психической травмы и других стрес совых состояний. Так, например, под их влиянием угнетается функция половых желез, что может выражаться в снижении половой потенции у мужчин и расстройствах менструального цикла у женщин. С. П. Боткин, подчеркивая особую роль психической травмы в развитии гипертиреоза, рассматривал его как заболевание «центрального черепно-мозго вого характера».
Нарушение трансгипофизарной регуляции. Трансгипофизарная регуляция является основной для функции щитовидной железы, коры надпочечников и половых желез. Первая ступень включает образова ние в нейросекреторных клетках медиобазальной части подбугорья олигопептидов, которые опускаются по аксонам до капилляров срединного возвышения и через венозные сосуды ножки гипофиза достигают аденогипофиза Здесь они либо стимулируют, либо тормозят образование тропных гормонов Стимулирующие олигопептиды получили название либеринов, или рилизинг-факторов (от англ. release — высвобождать). К их числу относятся тиреолиберин, гонадолиберины, соматолиберин и др Тормозящие олигопептиды называют статинами, например тиреос-
359
татин, соматостатин и др. Их соотношение между собой определяет об разование соответствующего тропного гормона. Вторая ступень начи нается с образования в аденогипофизе тройных гормонов — соматотропного (СТГ), гонадотропина (ГТГ) и др. Тропные гормоны, действуя на соответствующие мишени, включают третью ступень. Тиреотропин, гонадотропин, адренокортикотропин стимулируют в соответствующих же лезах внутренней секреции образование гормонов, а СТГ инициирует в тканях образование соматомединов — полипептидных гормонов, через которые и оказывает свое действие. Эти полипептидные гормоны осу ществляют генерализованное и относительно длительное влияние.
Избирательное нарушение образования в гипоталамусе того или иного либерина, а возможно, и усиление продукции статина вызывают нарушение выработки соответствующего тропного гормона в аденогипофизе.
Например, угнетение секреции гонадолиберинов приводит к недо статочному образованию гонадотропинов, угнетение секреции тиролиберина — к недостаточному образованию тиреотропина и т.д.
Первичное поражение лимбических структур головного мозга с рас стройством контроля секреции кортиколиберина и последующим вовле чением аденогипофиза и коры надпочечников лежит в основе развития болезни Иценко—Кушинга и характеризуется усилением секреции кортизола с развитием синдрома гиперкортизолизма. Одновременно при этом заболевании снижается чувствительность соответствующих центров гипоталамуса и аденогипофиза к кортизолу, что нарушает ра боту механизма обратной связи, в результате чего повышенная концент рация кортизола в крови не угнетает секрецию кортиколиберина в гипо таламусе и АКТГ в гипофизе.
Важным фактором нарушения регуляции функций эндокринной си стемы являются сосудистые поражения. Например, при поражении портальных сосудов срединного возвышения иногда возникают ишемия гипофиза и его некроз. Это ведет к развитию гипопитуитаризма и выпа дению второй ступени трансгипофизарной регуляции функций желез.
Нарушение парагипофизарной регуляции. Парагипофизарный путь является в основном нервно-проводниковым. Через этот путь осу ществляется секреторное, сосудистое и трофическое влияние ЦНС на функцию желез внутренней секреции. Для мозгового слоя надпочечни ков, островков Лангерганса и паращитовидных желез это важнейший путь их регуляции; в реализации функции других желез играют роль оба пути регуляции. Так, функция щитовидной железы определяется не толь ко ТТГ, но и симпатической импульсацией. Прямое раздражение сим патических нервов увеличивает поглощение йода железой, образова ние тиреоидных гормонов и их освобождение. Денервация яичников вызывает их атрофию и ослабляет реакцию на гонадотропные гормоны.
Нарушение транс- и парагипофизарной регуляции приводит к дис функции желез внутренней секреции. Выделяют различные варианты на-
360
рушения их функции. Гипофункция — снижение образования гормонов данной железой, гиперфункция — усиление их образования. При на рушении функции одной железы говорят о моногландулярном процес се, расстройство функций нескольких желез обозначают плюригландулярным процессом. Нарушения функции железы могут быть парциальными, когда страдает образование какого-либо одного из не скольких секретируемых железой гормонов (например, в надпочечни ках), либо тотальными, когда изменяется секреция всех гормонов, про дуцируемых данной железой.
Нередко нарушение функций желез сопровождается вовлечени ем в патологический процесс центров вегетативной нервной системы. Примером этого является адипозогенитальная дистрофия. При этой па тологии находят изменения в паравентрикулярных и вентромедиальных ядрах гипоталамуса, что приводит к снижению образования гонадотропинов и развитию гипогонадизма, а также повышенного аппетита с раз витием ожирения.
Патогенез ожирения сложен. В механизме его развития принима ют участие несколько факторов:
• недостаточное образование (или высвобождение) в гипофизе жиромобилизующих полипептидов или тех фрагментов молекул СТГ и АКТГ, которые активируют мобилизацию жира из жировых депо, по вышают содержание жирных кислот в крови и стимулируют их окис ление;
•поражение трофических центров гипоталамуса, что снижает акти вирующее действие симпатической нервной системы на мобилиза цию жира из жировых депо;
•усиление образования или активности инсулина, который стимули рует переход углеводов в жиры.
Роль механизма обратной связи. Независимо от характера пато генетического пути нарушения функций желез внутренней секреции, как правило, в той или иной степени страдает механизм обратной связи, что может стать причиной других расстройств. Механизм обратной свя зи является обязательным звеном в саморегуляции деятельности же лез. Сущность регуляции заключается в том, что регулируемый пара метр оказывает обратное влияние на активность железы. По характеру регулируемого параметра механизмы обратной связи можно разделить на два типа.
Первый тип: регулируемым параметром является концентрация гормона в крови. Механизм саморегуляции заключается в том, что по вышение концентрации гормона в крови тормозит активность гипоталамического центра, секретирующего либерины, и образование последних уменьшается. Это тормозит синтез тройного гормона гипофиза и актив ность соответствующей периферической железы. При уменьшении кон центрации гормона возникает обратная ситуация. Так осуществляется регуляция секреции кортизола, тиреоидных и половых гормонов.
361
Второй тип: регулируемым параметром является не концентрация
гормона, а содержание регулируемого вещества, например концентра
ция глюкозы в крови или ионов кальция. В этих случаях активность желе зы определяется концентрацией регулируемого вещества, которое дей ствует непосредственно на данную железу. Знание принципа механизма обратной связи важно для патофизиологического анализа нарушений.
По принципу механизма обратной связи может возникнуть тормо жение функции (или даже атрофия) железы при лечении теми или иными гормонами. Примером служит применение кортикостероидных гормонов. С лечебной целью их назначают нередко длительно, что вызывает атро фию коры надпочечников.
Известно, что стрессовые состояния в связи с действием на орга низм различных повреждающих факторов (операционная или бытовая травма, холод, токсины, аллергическая альтерация и др.) сопровождают ся активацией функции коры надпочечников и усилением секреции кортикостероидов. Это позволяет организму приспособиться к новым усло виям. Развитие стрессовых состояний после длительного применения кортикостероидов может обусловить острую надпочечниковую недоста точность.
При расстройстве центрального механизма регуляции нарушается и механизм обратной связи, в результате изменение концентрации гор мона в крови уже не влияет на секрецию рилизинг-фактора. Например, при болезни Иценко—Кушинга снижается чувствительность гипоталамических центров, воспринимающих колебания концентрации кортизола в крови. В данном случае обычная концентрация кортизола не тормозит образования кортиколиберина. Это ведет к повышенной его секреции и как следствие — к увеличению продукции АКТГ.
Для оценки функции желез, имеющих трансгипофизарную регуля цию, важно определять концентрацию тропного гормона в крови. Это может помочь установить локализацию патологического процесса. Так, при гипотиреозе значительное увеличение концентрации ТТГ (в 4—10 раз) свидетельствует о поражении щитовидной железы, которая не реагирует на ТТГ, а снижение его концентрации до следовых количеств заставляет предполагать локализацию процесса в гипофизе или центральной нерв ной системе.
15.2. Патологические процессы в железах
Различные патологические процессы могут развиваться в самой железе и тем самым вызывать нарушение ее функции.
Инфекционные процессы и интоксикации. Острые инфекцион ные заболевания могут приводить к нарушению функции желез внутрен ней секреции. Например, менингококковая инфекция может сопровож даться кровоизлиянием в надпочечники, что приводит к разрушению ткани
железы и развитию острой надпочечниковой недостаточности. Подобная
патология может возникать при дифтерии в связи с коагуляционными нек-
362
розами в надпочечниках. Эпидемический паротиту взрослых мужчин часто вызывает орхит, который в 3 0 — 5 0 % случаев заканчивается одноили двусторонней атрофией яичек. Яички могут поражаться и при гонорее в связи с восходящей инфекцией уретры. Такие инфекционные заболева ния, как туберкулез и сифилис, также поражают различные железы. При туберкулезе происходит постепенное разрушение ткани железы в связи створожистым некрозом туберкулезных бугорков, а при сифилисе — в свя зи с некрозом сифилитической гранулемы (гуммы). При локализации про цесса в надпочечных железах развивается хроническая надпочечниковая недостаточность, которая называется аддисоновой болезнью по имени врача Аддисона, впервые описавшего это заболевание. При локализации процесса в тестикулах развивается гипогонадизм, характеризующийся снижением образования андрогенов и нарушением сперматогенеза. Ло кализация в паращитовидных железах вызывает гипопаратиреоз и т.д.
Опухолевые процессы в железах — один из частых патологичес ких процессов в железах внутренней секреции. Опухоль может развиться влюбой железе. Характер расстройств определяется свойством и качест вом секретируемых гормонов и влиянием опухоли на окружающую ткань железы. Некоторые опухоли не секретируют гормона, а лишь сдавливают и приводят к атрофии нормальные участки железы. Клинически это про является гипофункцией соответствующей железы, как, например, при
хромофобных аденомах гипофиза. Среди различных опухолей гипо физа эта опухоль встречается чаще. Она не секретирует гормона, но сдав ливает гипофиз и приводит к его гипофункции. Уменьшается секреция тропных гормонов, что обуславливает гипофункцию половых желез, щи товидной железы и надпочечников. Одновременно она может сдавливать зрительные нервы и хиазму. Это приводит к выпадениям полей зрения вплоть до полной слепоты.
При эозинофильной аденоме гипофиза — опухоли, происходя щей из эозинофильных клеток, продуцируется избыточное количество соматотропина.
В период роста организма это приводит к развитию гигантизма, а после окостенения эпифизарных хрящей — к акромегалии (от греч. акгоБ — крайний, тедаБ — большой). В последнем случае происходит непропорциональное увеличение и утолщение концевых частей скелета (кисти рук, стопы ног) и костей черепа вследствие периостального роста. Одновременно увеличиваются внутренние органы. При базофильной аде номе гипофиза — опухоли, происходящей из базофильных клеток, про дуцируется избыточное количество адренокортикотропина. Это приводит к увеличению секреции кортизола надпочечными железами и развитию синдрома гиперкотизолизма. Этот же синдром может быть вызван и опу холью пучковой зоны коры надпочечников, которая секретирует избыточ ное количество кортизола. Определенную роль в развитии указанных из менений при этом синдроме играет механизм обратной связи. Если при базофильной аденоме избыточная секреция АКТГ вызывает гиперплазию обоих надпочечников, то при опухоли пучковой зоны одного надпочечни-
363

Рис. 15. 1. Механизмы развития гиперкортизолизма.
А — саморегуляция продукции кортизола в норме, Б — при аденоме пучковой зоны коры надпочечников, В — при снижении чувствительности гипоталамических центров, регу лирующих образование кортиколиберина, Г — при базофильной аденоме гипофиза
ка механизм обратной связи выключает секрецию АКТГ и это приводит к атрофии второго — нормального — надпочечника (рис. 15.1).
При опухолях тестикул, происходящих из клеток Лейдига, усили вается образование андрогенов. Если опухоль возникает у мальчиков до 9-летнего возраста, это ведет к преждевременному половому созрева нию, характеризующемуся быстрым ростом тела и развитием вторичных половых признаков. Однако опухолевый процесс не сопровождается спер матогенезом и непораженные участки железы остаются незрелыми.
Опухоли сетчатой зоны коры надпочечников продуцируют гормо ны, обладающие андрогенными и эстрогенными свойствами, и приводят к развитию адреногенитальных синдромов. При этом изменения зависят в значительной степени от пола, возраста и характера секретируемых гормонов. Различают два основных адреногенитальных синдрома:
•гетеросексуальный, когда у данного пола избыточно образуются
половые гормоны противоположного пола;
• изосексуальный, наблюдаемый при раннем или избыточном обра зовании половых гормонов, присущих данному полу.
Чаще гетеросексуальный адреногенитальный синдром развивает ся у женщин, при этом опухоль продуцирует избыточные количества андростендиона и адреностерона. Эти гормоны близки по своему биологи ческому действию к мужскому половому гормону. Образовавшиеся гормоны по механизму обратной связи тормозят продукцию гонадотропинов. Это приводит к атрофии яичников и как следствие — к атрофии вторичных женских половых органов. Под влиянием андрогенов развива ются мужские вторичные половые признаки (маскулинизация), в частно сти рост волос по мужскому признаку (вирилизм). В связи с анаболичес ким действием этих гормонов на белковый обмен происходит усиленное развитие мускулатуры и женщина приобретает мужское телосложение. Соответствующим образом меняется и психика пациентов.
364
Иногда опухоли поражают несколько эндокринных желез. Описа ны аденомы, одновременно разбивающиеся в аденогипофизе, паращитовидных железах и островках поджелудочной железы. Одна или все они могут быть гормонально-активными, и клиника будет зависеть от количест ва и вида секретируемых гормонов. Иногда этот синдром носит семей ный характер и сопровождается развитием пептических язв. Примером является синдром Золлингера—Эллисона (синдром ульцерогенныхаденом островков Лангерганса). Его развитие связано с наличием гастринсекретирующей опухоли поджелудочной железы, вызывающей высокую желу дочную секрецию соляной кислоты, развитие пептических язв и диарею.
Железа внутренней секреции может быть не только источником опу холи, но и местом метастазирования опухолей из других органов. В этих случаях растущая опухоль сдавливает железу, вызывает ее атрофию и гипофункцию. Так, при метастазе рака молочной железы в заднюю долю гипофиза нарушается выделение антидиуретического гормона (АДГ) и развивается несахарный диабет. Рак легкого дает метастазы не только в кости, но и в надпочечники, а ракжелудка — нередко в яичники (так назы ваемый крукенбергский рак яичников).
Иногда опухоли эндокринных желез или даже неэндокринных ор ганов начинают продуцировать гормоны, не свойственные данной же лезе или вообще клеткам данного органа. Например, опухоль щитовид ной железы или бронхогенный рак начинают продуцировать АКТГ с развитием как следствие синдрома гиперкортизолизма. Такое измене ние фенотипа клеток связано с природой их опухолевой трансформации, во время которой происходит депрессия тех участков генома клетки, ко торые у дифференцированных клеток не функционируют.
Генетически обусловленные дефекты биосинтеза гормонов.
Биосинтез любого гормона представляет сложный процесс, в котором принимают участие многие ферменты. Образование же любого фермен та, точнее его апофермента, определяется активностью соответствующе го гена. Мутация гена может привести к нарушению образования апофер мента или такому его изменению, при котором образующийся фермент теряет свою активность. В таком случае будет нарушен последователь ный ход биосинтеза соответствующего гормона. Это приводит к следую щим расстройствам:
•развивается гипофункция железы;
•некоторые промежуточные продукты, образующиеся в процессе ме таболизма, начинают выделяться в кровь и оказывают специфичес кий патофизиологический эффект;
•нарушается механизм обратной связи, что может приводить к воз никновению дополнительных патологических процессов. Иллюстра цией к этому положению служат следующие примеры. На схеме 15.1 в самых общих чертах представлен биосинтез кортизола.
В настоящее время хорошо изучены два механизма нарушения об разования кортизола в связи с дефицитом ферментов — 21 -гидроксила-
365
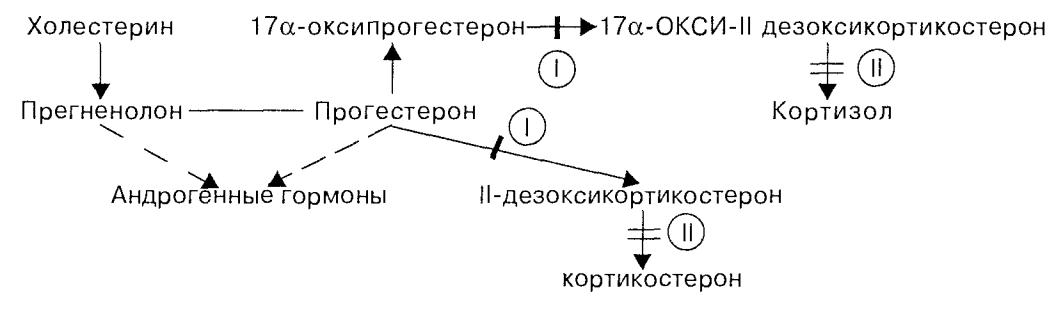
Схема 15.1. Места блокады биосинтеза кортизола.
зы или 11(3-гидроксилазы. При дефиците 21 -гидроксилазы(!) процесс биосинтеза заканчивается образованием прогестерона и 17а-оксипро- гестерона. Кортизол не образуется. Это по механизму обратной связи растормаживает секрецию кортиколиберина в гипоталамусе, что в свою очередь ведет к усилению образования АКТГ. АКТГ стимулирует стероидогенез до места блокады, но так как кортизол не образуется, вся эта стимуляция переключается на образование Д4 -андростен-3,17-диона, обладающего андрогенными свойствами. Его поступление в кровь зна чительно увеличивается. Образующиеся в надпочечниках андрогены, действуя по механизму обратной связи регуляции развития половых же лез, приводят к атрофии последних как у мальчиков, так и у девочек. Де фект выявляется уже в период эмбрионального развития. У эмбриона женского пола к этому периоду внутренние половые органы уже зало жены, поэтому избыток андрогенов вызывает их гипоплазию и разви тие вирилизма. Маскулинизация продолжается и после рождения. У мальчиков же появляются признаки преждевременного полового созре вания.
Подобный механизм включается и при дефекте фермента 11(3- гидроксилазы(Н). В этом случае кортизол также не образуется, но в от личие от предыдущего синдрома накапливается избыточное количество 11-дезоксикортикостерона и 17а-окси-11-дезоксикортикостерона, пер вый из которых обладает минералокортикоидной активностью, что ве дет к повышению кровяного давления. Этот патогенетический механизм можно блокировать введением глюкокортикоидов. Они тормозят обра зование АКТГ, уменьшая тем самым образование андрогенов.
Биосинтез тиреоидных гормонов в клетках фолликулярного эпите лия щитовидной железы также является сложным процессом. В общих чертах он представлен на схеме 15.2.
Установлена возможность блокады йодзахватывающей системы (I). Для этого случая характерна неспособность железы поглощать I131 при соответствующем исследовании. Исправление этого дефекта достига ется введением в организм небольших доз йодида калия, который благо даря повышению его концентрации в крови в силу диффузии проникает в щитовидную железу и, таким образом, компенсирует дефект йодзахваты вающей системы. II —блокада йодирования тирозина. Поглощенный йод
366

Схема 15.2. Места блокады биосинтеза тироидных гормонов.
сохраняется в железе в неорганической форме и не включается в тиро зин. Этот дефект пока компенсируется введением готовых тиреоидных гормонов. III —дефект конденсации йодтирозинов. Характеризуется накоплением промежуточных продуктов — МИТ и ДИТ и следовыми ко личествами Т3 и Т4. Компенсация дефекта проводится также введением гормонов. IV —дефект йодтирозин-дегалогеназы. Характеризуется уг нетением дегалогенизации МИТ и ДИТ. Эти продукты накапливаются, выделяются в кровь и выводятся из организма. Организм теряет йод, развивается йодная недостаточность. Компенсация дефекта может быть обеспечена введением в организм йодистого калия.
Каждый из указанных дефектов приводит к недостаточному обра зованию тиреоидных гормонов. В результате возникает гипофункция щитовидной железы, сопровождаемая развитием зоба (увеличением щитовидной железы) и кретинизма. Последнее объясняется тем, что эти дефекты возникают еще до рождения или в детском возрасте.
15.3. Периферические (внежелезистые) механизмы нарушения активности гормонов
Большую роль в развитии.эндокринных (а также некоторых других) заболеваний играют периферические механизмы, определяющие актив ность выделившихся в кровь гормонов. Эта активность может изменять ся либо в сторону ее повышения, либо снижения, что клинически соот ветствует их гиперили гипофункции соответствующей железы. Чтобы ясно представить себе возможные механизмы нарушения активности гор монов, необходимо рассмотреть некоторые вопросы их метаболизма и механизма действия.
Все выделившиеся из желез гормоны связываются в крови в той или иной степени с определенными белками и циркулируют в крови в двух формах — связанной и свободной. Из этих двух форм связанный гормон биологически неактивен. Активностью обладает только свободная фор ме гормона, которая и оказывает физиологическое действие в клеткахмишенях. Известно связывание белками тироксина, инсулина, гормона роста, стероидных гормонов. Например, в физиологических усло-
367
