
- •Глава 1 история химии белка
- •Глава 2 химический состав белков
- •2.1 Элементный состав белков
- •2.2 Аминокислоты – структурные компоненты белков
- •2.2.1 Классификация аминокислот
- •2.2.2 Номенклатура и изомерия
- •2.2.3 Физические свойства
- •2.2.4 Амфотерность аминокислот
- •2.2.5 Стереохимия аминокислот
- •2.2.6 Способы получения аминокислот
- •2.2.6.1 Способы синтеза -аминокислот
- •2.2.7 Химические свойства аминокислот
- •2.2.8 Биологически важные реакции аминокислот
- •2.2.9 Аналитически важные реакции аминокислот
- •Глава 3 первичная структура пептидов и белков
2.2.7 Химические свойства аминокислот
Химическое поведение аминокислот определяется двумя функциональными группами -NН2 и –СООН. Аминокислотам характерны реакции по аминогруппе, карбоксильной группе и по радикальной части, при этом в зависимости от реагента взаимодействие веществ может идти по одному или нескольким реакционным центрам.
Амфотерный характер аминокислот. Имея в молекуле одновременно кислотную и основную группу, аминокислоты в водных растворах ведут себя как типичные амфотерные соединения. В кислых растворах они проявляют основные свойства, реагируя как основания, в щелочных – как кислоты, образуя соответственно две группы солей:
![]()
![]()
Благодаря своей амфотерности в живом организме, аминокислоты играют роль буферных веществ, поддерживающих определенную концентрацию водородных ионов. Буферные растворы, полученные при взаимодействии аминокислот с сильными основаниями, широко применяются в биоорганической и химической практике. Соли аминокислот с минеральными кислотами лучше растворимы в воде, чем свободные аминокислоты. Соли с органическими кислотами труднорастворимые в воде и используются для идентификации и разделения аминокислот.
Реакции, обусловленные аминогруппой. С участием аминогруппы аминокислоты образуют аммониевые соли с кислотами, ацилируются, алкилируются, реагируют с азотистой кислотой и альдегидами в соответствии со следующей схемой:
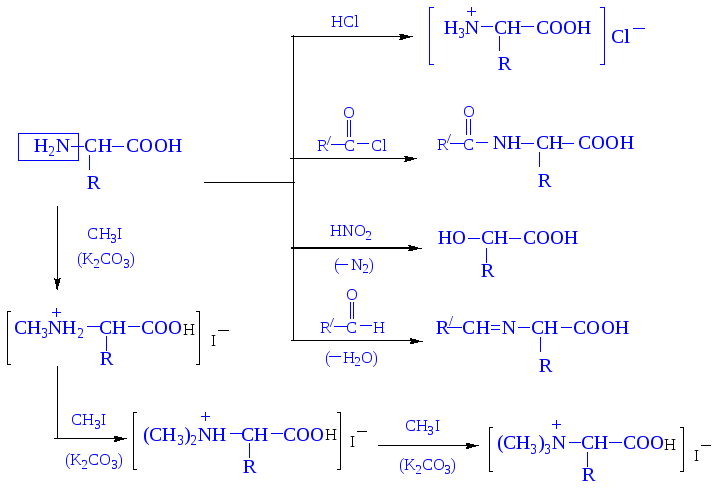
Алкилирование проводится при участии R-На1 или Аr-Наl:
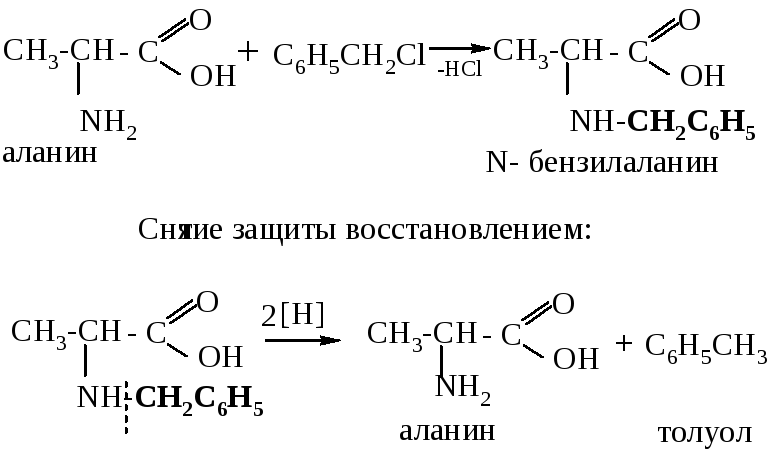
В процессе реакции ацилирования используются хлорангидриды или ангидриды кислот (ацетилхлорид, уксусный ангидрид, бензилоксикарбонилхлорид):
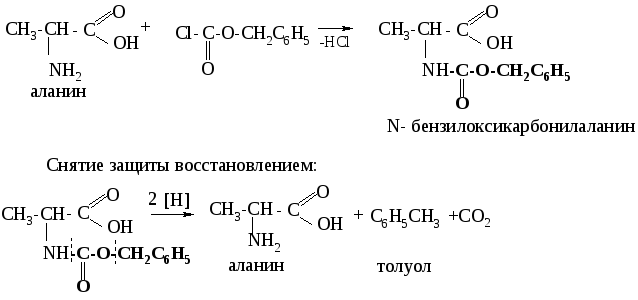
Реакции ацилирования и алкилировнаия применяется для защиты NН2–группы аминокислот в процессе синтеза пептидов.
Реакции, обусловленные карбоксильной группой. При участии карбоксильной группы аминокислоты образуют cоли, сложные эфиры, амиды, хлорангидриды в соответствии со схемой, представленной ниже:
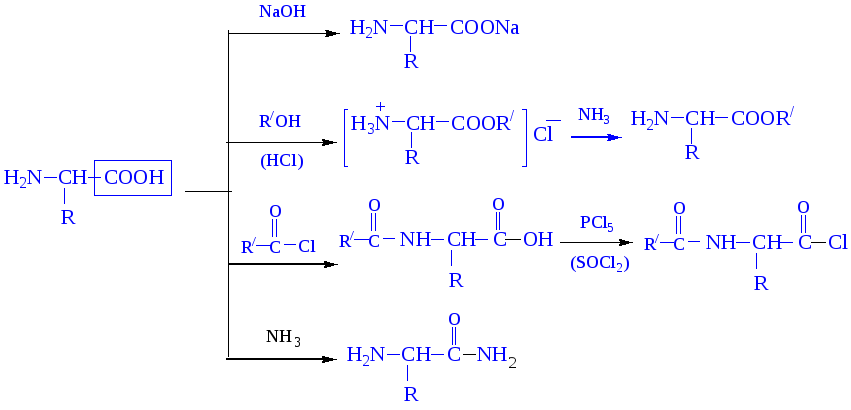
Если при -углеродном атоме в углеводородном радикале имеется электроноакцепторный заместитель (NO2, СС13, СООН, COR и т.д.), поляризующий связь ССООН, то у карбоновых кислот легко протекают реакции декарбоксилирования. Декарбоксилирование -аминокислот, содержащих в качестве заместителя +NH3-группу, приводит к образованию биогенных аминов. В живом организме данный процесс протекает под действием фермента декарбоксилазы и витамина пиридоксальфосфата.
В лабораторных условиях реакцию осуществляется при нагревании -аминокислоты в присутствии поглотителей СО2, например, Ва(ОН)2.
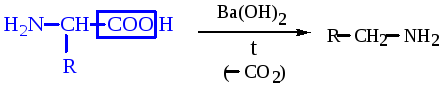
При декарбоксилировании -фенил--аланина, лизина, серина и гистидина образуются, соответственно, фенамин, 1,5-диаминопентан (кадаверин), 2-аминоэтанол-1 (коламин) и триптамин.
Реакции аминокислот с участием боковой группы. При нитровании аминокислоты тирозин азотной кислотой происходит образование динитропроизводного соединения, окрашенного в оранжевый цвет (ксантопротеиновая проба):
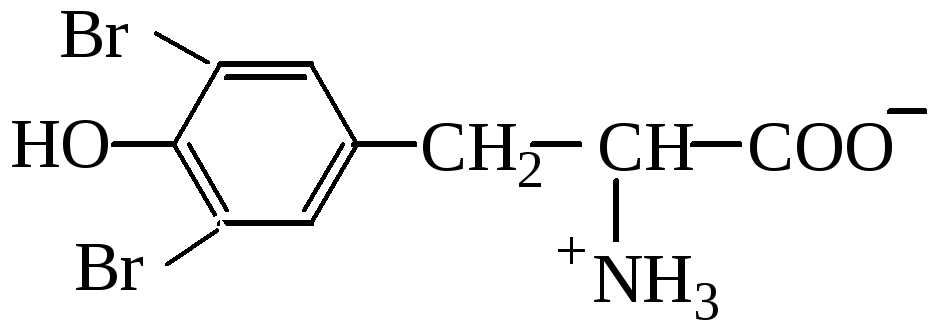
Окислительно-восстановительные переходы имеют место в системе цистеин – цистин:
[ O ]
2НSCH2CH(NH2)COOH HOOCCH(NH2)CH2S–SCH2CH(NH2)COOH
[ H ]
HOOCCH(NH2)CH2S–SCH2CH(NH2)COOH 2 НSCH2CH(NH2)COOH
В некоторых реакциях аминокислоты реагируют по обеим функциональным группам одновременно.
Образование комплексов с металлами. Почти все -аминокислоты образуют комплексы с ионами двухвалентных металлов. Наиболее устойчивыми являются комплексные внутренние соли меди (хелатные соединения), образующиеся в результате взаимодействия с гидроксидом меди (II) и окрашенные в синий цвет:
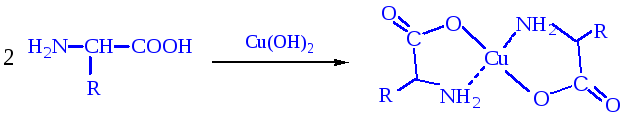
Действие азотистой кислоты на алифатические аминокислоты приводит к образованию гидроксикислот, на ароматические - диазосоединений.
Образование гидроксикислот:
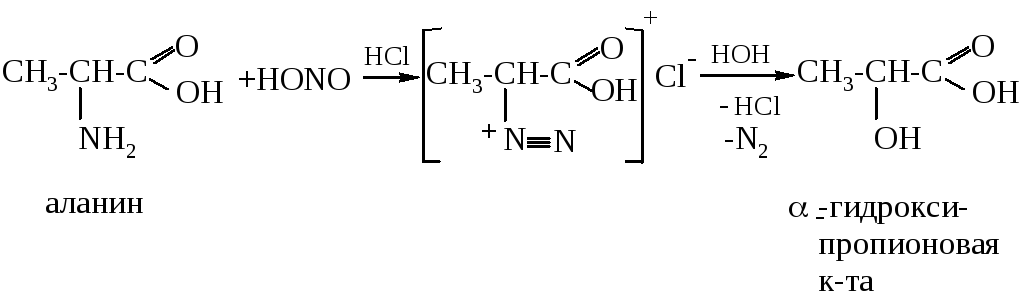
Реакция диазотирования:
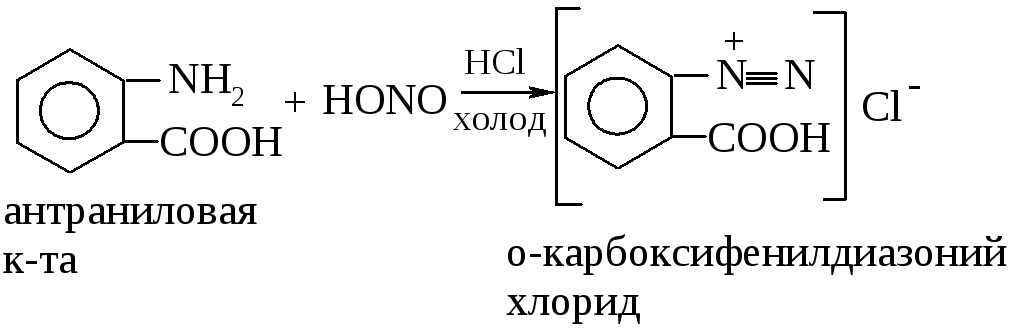
(диазосоединение)
Диазосоединение далее может реагировать по двум направлениям:
с выделением молекулярного азота N2:
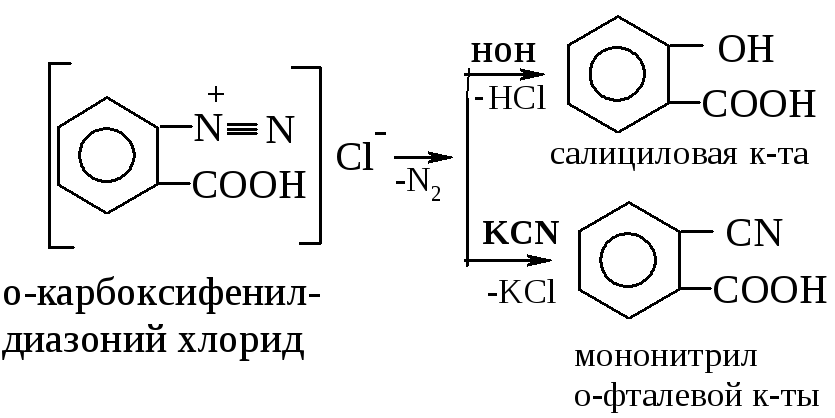
2. без выделения молекулярного азота N2:
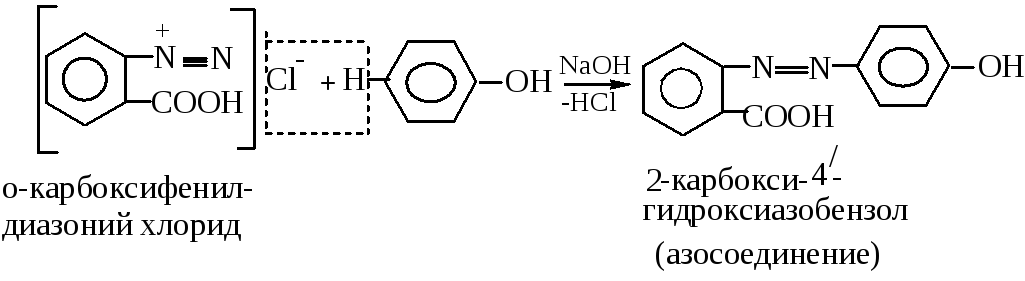
Хромофорная группа азобензола -N=N в азосоединениях обуславливает желтую, желтую, оранжевую или другого цвета окраску веществ при поглощении в видимой области света ( 400-800 нм). Ауксохромная группа
-СООН изменяет и усиливает окраску за счет π, π - сопряжения с π - электронной системой основной группы хромофора.
Отношение аминокислот к нагреванию. При нагревании аминокислоты разлагаются с образованием различных продуктов в зависимости от их типа. При нагревании -аминокислот в результате межмолекулярной дегидратации образуются циклические амиды - дикетопиперазины:
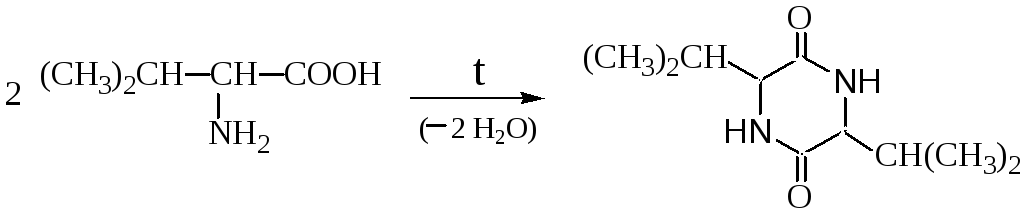
валин (Val) диизопропильное производное
дикетопиперазина
При нагревании -аминокислот от них отщепляется аммиак с образованием α, β-непредельных кислот с сопряженной системой двойных связей:
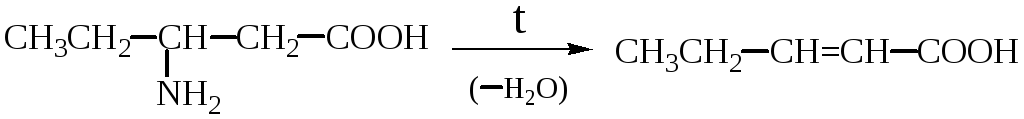
β-аминовалериановая кислота пентен-2-овая кислота
(3-аминопентановая кислота)
Нагревание - и -аминокислот сопровождается внутримолекулярной дегидратацией и образованием внутренних циклических амидов – лактамов:
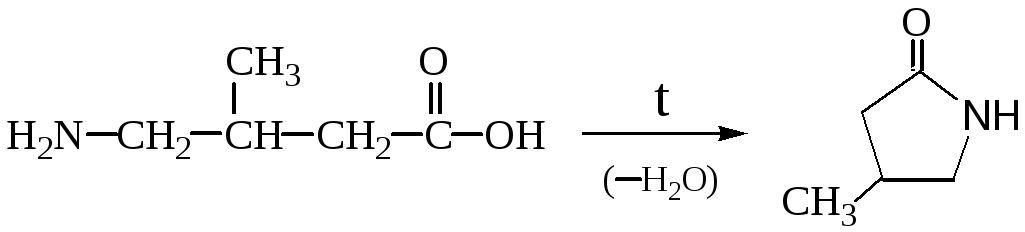
γ-аминоизовалериановая кислота лактам γ-аминоизовалериановой
(4-амино-3-метилбутановая кислота) кислоты
