
- •Глава 1 история химии белка
- •Глава 2 химический состав белков
- •2.1 Элементный состав белков
- •2.2 Аминокислоты – структурные компоненты белков
- •2.2.1 Классификация аминокислот
- •2.2.2 Номенклатура и изомерия
- •2.2.3 Физические свойства
- •2.2.4 Амфотерность аминокислот
- •2.2.5 Стереохимия аминокислот
- •2.2.6 Способы получения аминокислот
- •2.2.6.1 Способы синтеза -аминокислот
- •2.2.7 Химические свойства аминокислот
- •2.2.8 Биологически важные реакции аминокислот
- •2.2.9 Аналитически важные реакции аминокислот
- •Глава 3 первичная структура пептидов и белков
2.2.2 Номенклатура и изомерия
Для наименования аминокислот широко применяются тривиальные названия и буквенные сокращенные символы (см. Приложение 2). По рациональной номенклатуре аминокислоты рассматривают как производные соответствующих карбоновых кислот, положение аминогруппы указывается буквами , , и т. По ИЮПАК для наименования аминокислот группу NH2 называют префиксом (приставкой) «амино» с указанием цифрой номера углеродного атома, с которым она связана, затем следует название соответствующей кислоты. Нумерацию главной цепи осуществляют от углеродного атома карбоксильной группы.
Для аминокислот характерна:
структурная изомерия, связанная с особенностями строения углеродного скелета и взаимным расположением функциональных групп;
пространственная (стереохимическая, оптическая) изомерия, связанная с наличием асимметрических углеродных атомов.
2.2.3 Физические свойства
-Аминокислоты – кристаллические вещества белого или сероватого цвета. Они хорошо растворяются в воде с образованием электролитов, плохо – в спирте, не растворяются в эфире. Аминокислоты в твердом и растворенном состоянии имеют биполярное строение, на что указывает отсутствие в ИК-спектрах отдельных полос поглощения, характерных для – NН2 и –СООН групп, они обладают высокой температурой плавления (См. Приложение 3).
2.2.4 Амфотерность аминокислот
Амфотерность – способность -аминокислот диссоциировать в водном растворе по типу кислоты и основания из-за наличия в их составе групп кислотного (-СООН) и основного (-NH2) характера. Аминокислоты существует в виде равновесной смеси биполярного иона (цвиттериона) катионной и анионной форм, равновесие которых зависит от рН среды:
+H+ +OH–

 NH3+
– СH
– COOH NH3+
– CH – COO–
NH2
– CH – COO–
+ H2O
NH3+
– СH
– COOH NH3+
– CH – COO–
NH2
– CH – COO–
+ H2O
– H+ – OH–
R R R
Катионная форма Биполярный ион Анионная форма
Сильнокислая среда Сильнощелочная среда
р
 Н
1,0 рН 7,0 рН 11,0
Н
1,0 рН 7,0 рН 11,0
Катионные формы пребладают в сильнокислых средах, анионные в
сильнощелочных. Катионная форма -аминокислоты, с позиций теории Бренстеда, является двухосновной кислотой, содержащей две кислотные группы: недиссоциированную карбоксильную группу и протонированную аминогруппу. Характеризуется кислота соответствующими значениямирКа1 ирКа2. Отдавая один протон, двухосновная кислота превращается в слабую одноосновнуюдиполярный ион с одной кислотной+NH3-группой. Депротонирование диполярного иона приводит к получению анионной формы-аминокислотыкарбоксилат-аниона (основание Бренстеда).
Значения рКа1, характеризующие кислотные свойства –СООН группы -аминокислот, лежат в интервале от 1 до 3; значения рКа2, характеризующие кислотность аммониевой группы, от 9 до 10. Положение равновесия (соотношение различных форм -аминокислоты) в водном растворе при определенных значениях рН зависит от наличия в радикале R ионогенных групп, которые играют роль дополнительных кислотных и основных центров.
Значение рН, при котором концентрация диполярных ионов максимальна, а минимальные концентрации катионныхи анионных форм -аминокислоты равны, называется изоэлектрической точкой (pI).
pI = 1/2 . (рКа n + рКа n+1), где
n максимальное число положительных зарядов в протонированной-аминокислоте
В изоэлектрической точке суммарный заряд молекулы -аминокислоты
равен нулю. Биполярные ионы не перемещаются в электрическом поле. При значениях рН ниже рI катион -аминокислоты (аммониевая форма) движется к катоду; при рН выше, чем pI, карбоксилат-анион аминокислоты перемещается к аноду. На этом основано разделение аминокислот методом электрофореза.
Нейтральные а-аминокислоты имеют рI несколько ниже 7,0 (5,5—6,3) из-за большей ионизации карбоксильной группы под влиянием Iэфф +NH3 –группы:
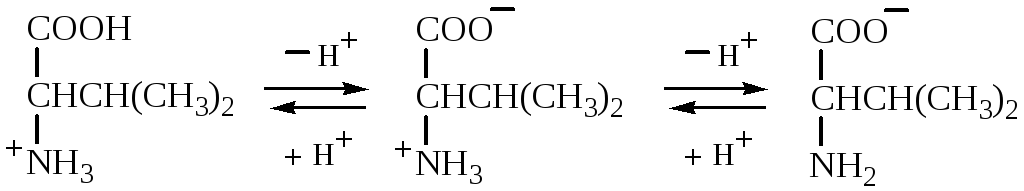
катион биполярный ион анион
pKa 1 = 2,3 СOOH-группы pI = 6,0 рКа2= 9,6+NH3-группы
Кислые а-аминокислоты, имеющие в радикале дополнительную карбоксильную группу, в сильнокислой среде находятся в полностью протонированной форме. Они являются трехосновными кислотами (по Бренстеду), характеризующимися тремя значениями рКа, как это видно на примере глутаминовой кислоты (рI = 3,2):

катион биполярный ион анион дианион
рКа1= 2,2 (-СOOH)pI=3,2pKa2=4,3 (COOHвpKa3=9,7+NH3- радикале группы
Основные а-аминокислоты имеют изоэлектрическую точку выше рН 7. В сильнокислой среде они также представляют собой трехосновные кислоты, этапы ионизации которых выглядят следующим образом:

Дикатион катион биполярный ион анион
лизина pKa1=2,2 (COOH)pKa2=9,0 (-+NH3)pKa3=10,5 (+NH3 в радикале)
Свойство аминокислот диссоциировать на ионы в кислой или щелочной среде лежит в основе методов разделения и идентификации их ионообменной хроматографией и электрофорезом (см. главу 6 ).
