
- •Термодинамика в ХАЙСИС
- •1 Компоненты
- •1.1 Введение
- •1.2 Окно Список компонентов
- •2 Пакет свойств
- •2.1 Введение
- •2.2 Закладка Пакеты свойств
- •2.3 Добавление пакета свойств
- •2.4 Специализированное окно Пакет свойств
- •2.4.1 Закладка Термодинамический пакет
- •2.4.2 Закладка Параметры
- •2.4.3 Закладка Бинарные коэффициенты
- •2.4.5 Закладка Порядок фаз
- •2.4.6 Закладка Реакции
- •2.4.7 Закладка Табличный пакет
- •2.4.8 Закладка Примечания
- •2.5 Окно Пакет свойств с ComThermo
- •2.6 Литература
- •3 Гипотетические компоненты
- •3.1 Введение
- •3.2 Диспетчер гипотетических компонент
- •3.3 Добавление гипотетического компонента
- •3.3.1 Создание этанола
- •3.3.2 Сравнение библиотечного и гипотетического компонентов
- •3.4 Создание группы гипотетических компонент
- •3.4.1 Окно Гипотетические компоненты
- •3.4.2 Задание основной информации
- •3.4.3 Структура UNIFAC
- •3.5 Окно гипотетического компонента
- •3.5.1 Закладка идентификации (ID)
- •3.5.2 Закладка Критические свойства
- •3.5.3 Закладка Дополнительные свойства
- •3.5.4 Закладка Свойства, зависящие от температуры
- •3.6 Твердый гипотетический компонент
- •3.6.1 Закладка идентификации (ID)
- •3.6.3 Закладка Дополнительные свойства
- •3.6.4 Закладка Свойства, зависящие от температуры
- •3.6.5 Закладка PSD
- •3.7 Копирование библиотечных компонент
- •3.8 Управление гипотетическими компонентами
- •3.8.1 Просмотр группы
- •3.8.2 Перемещение компонент
- •3.9 Литература
- •4 Диспетчер нефтяных смесей
- •4.1 Введение
- •4.2 Нефтяной пакет
- •4.2.1 Лабораторные данные
- •4.2.2 Стандартные методы разгонки
- •4.2.3 Единицы измерения
- •4.2.4 Физические свойства
- •4.2.5 Способы задания свойств
- •4.2.6 Поправки лабораторных данных
- •4.2.7 Корреляции по умолчанию
- •4.3 Процедура характеризации нефтяных смесей
- •4.3.1 Введение
- •4.3.2 Первый шаг - Ввод данных
- •4.3.3 Второй шаг - Создание псевдокомпонентов
- •4.3.4 Третий шаг - Инсталляция нефтяного потока
- •4.3.5 Пользовательское свойство
- •4.3.6 Корреляции
- •4.4 Окно Характеризация нефти
- •4.5 Ввод экспериментальных данных
- •4.5.1 Закладка Исходные данные
- •4.5.2 Закладка Параметры по умолчанию
- •4.5.3 Закладка Рабочие кривые
- •4.5.4 Закладка График
- •4.5.5 Закладка Методы расчета
- •4.5.6 Закладка Пользовательские кривые
- •4.5.7 Закладка Заметки
- •4.6 Создание псевдокомпонентов
- •4.6.1 Закладка Данные
- •4.6.2 Закладка Корреляции
- •4.6.3 Закладка Таблицы
- •4.6.4 Закладка Графики свойств
- •4.6.5 Закладка Графики распределений
- •4.6.6 Закладка Композитные графики
- •4.6.7 Закладка Подшивка графиков
- •4.6.8 Закладка Примечания
- •4.7 Пользовательское свойство
- •Закладка Пользовательское свойство
- •Окно Пользовательское свойство
- •4.8 Корреляции и инсталляция
- •4.8.1 Закладка Корреляции
- •4.8.2 Окно Корреляции
- •4.8.3 Закладка Примечания
- •4.8.4 Закладка Инсталляция
- •4.9 Пример - характеризация нефти
- •4.9.1 Начало работы
- •4.9.2 Шаг 1 - Задание экспериментальных данных
- •4.9.3 Шаг 2 - Разбивка на псевдокомпоненты
- •4.9.4 Шаг 3 - Инсталляция смеси в схему
- •4.9.5 Связанный пакет свойств
- •4.10 Пример 2 - Кривая распределения серы
- •4.10.1 Пакет свойств
- •4.10.2 Добавление Пользовательского свойства
- •4.10.3 Ввод данных
- •4.10.4 Разбивка на псевдокомпоненты
- •4.10.5 Результаты
- •4.11 Литература
- •5 Диспетчер реакций
- •5.1 Введение
- •5.2 Компоненты реакций
- •5.2.1 Выбор компонентов из Диспетчера базиса
- •5.2.2 Выбор компонентов внутри Диспетчера реакций
- •5.2.3 Компоненты библиотечных реакций
- •5.3 Реакции
- •5.3.1 Работа с реакциями
- •5.3.2 Конверсионные реакции
- •5.3.3 Равновесные реакции
- •5.3.4 Кинетические реакции
- •5.3.5 Гетерогенная каталитическая реакция
- •5.3.6 Простая реакция
- •5.4 Наборы реакций
- •5.4.1 Работа с наборами реакций
- •5.4.2 Окно Набор реакций
- •5.4.3 Экспорт/Импорт наборов реакций
- •5.4.4 Добавление набора реакций к пакету свойств
- •5.4.5 Доступ к реакциям из расчета
- •5.5 Обобщенная процедура
- •5.6 Демонстрационный пример
- •5.6.1 Добавление компонент
- •5.6.2 Создание реакции
- •5.6.3 Добавление реакции в набор реакций
- •5.6.4 Связывание набора реакций с Пакетом свойств
- •6.1 Введение
- •6.2 Закладка Отображение
- •6.2.1 Отображение компонентов
- •6.2.2 Коллекции
- •6.2.3 Отображения для коллекций
- •6.3 Окно Отображение компонентов
- •7.1 Введение
- •7.2 Закладка Пользовательское свойство
- •7.2.1 Добавление пользовательского свойства
- •7.3 Окно Пользовательское свойство
- •7.3.1 Закладка Данные
- •7.3.2 Закладка Примечания
- •Б.1 Введение
- •Б.2 Методика характеризации
- •Б.2.1 Построение рабочих кривых
- •Б.2.2 Анализ газовой части
- •Б.2.3 Автоматический расчет газовой части
- •Б.2.4 Разбивка кривой ИТК на псевдокомпоненты
- •Б.2.5 Графическое определение свойств компонентов
- •Б.2.7 Корреляции
- •Б.3 Литература
- •Г.1 Введение
- •Г.2 Упругость паров чистых компонент
- •Г.3 Правила смешения
- •Г.3.1 Правила смешения TST
- •Г.3.2 Правила смешения CEOS/AE при нулевом давлении
- •Г.3.3 Модель жидкости GE
- •Г.4 Расчет фазового равновесия
- •Г.5 Расчет энтальпии и энтропии
- •Г.6 Литература
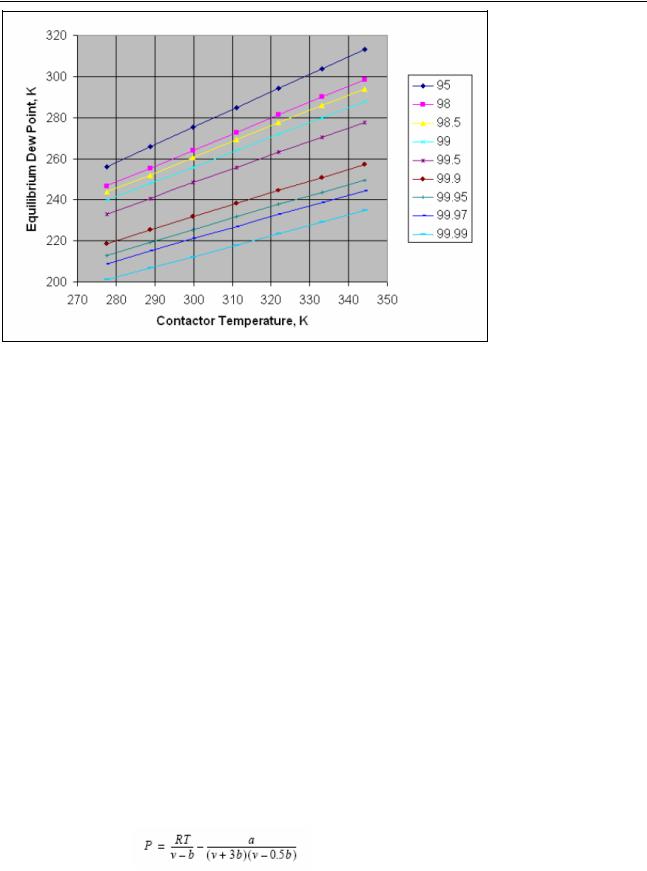
Пакет свойств Гликоли Г - 3
В следующих версиях ХАЙСИС база данных BIP для гликолей будет обновляться. В настоящей версии имеются некоторые ограничения
Г.2 Упругость паров чистых компонент
В пакете Гликоли для расчета упругости паров в базе данных ХАЙСИС используются три параметра функции альфа:
•L в уравнении D6
•M в уравнении D6
•N в уравнении D6
Г.3 Правила смешения
В пакете Гликолей для расчета равновесия смеси пар-жидкость используются три параметра. Параметры бинарного взаимодействия Aij, Aji и αij из уравнений 30 и 31 используются в правиле смешения для расчета AЕ
по уравнению TST (Twu-Sim-Tassone).
Г.3.1 Правила смешения TST
Кубическое уравнение TST (Twu в. 20025) выглядит следующим образом:
(1)
где a, b |
параметры, соответствующие критической температуре |
|
компонента. |

Г - 4 Пакет свойств Гликоли
(2)
(3)
(4)
где |
с – указывает на значение переменной при критических условиях. |
параметр а зависит от температуры. Значения при температуре, отличной от критической, рассчитываются по уравнению:
(5)
где |
- функция приведенной температуры Tr = T/Tc |
• При расчете упругости пара Тью (Twu et al., 19913) использует величину
(6)
где L, M, N – параметры, уникальные для каждого компонента.
•Для небиблиотечных компонент обобщенная функция альфа определяется как функция двух переменных – приведенной температуры и ацентрического фактора.
(7)
•Для небиблиотечных компонент и нефтяных фракций обобщенная функция альфа определяется следующим образом:
(8)
где α0 – соответствует ω = 0,
α1 – соответствует ω = 1
α - это функция только приведенной температуры.
(9)
(10)
где L, M, и N – значения, соответствующие докритическим и сверхкритическим условиям.
Для Тr≤1:
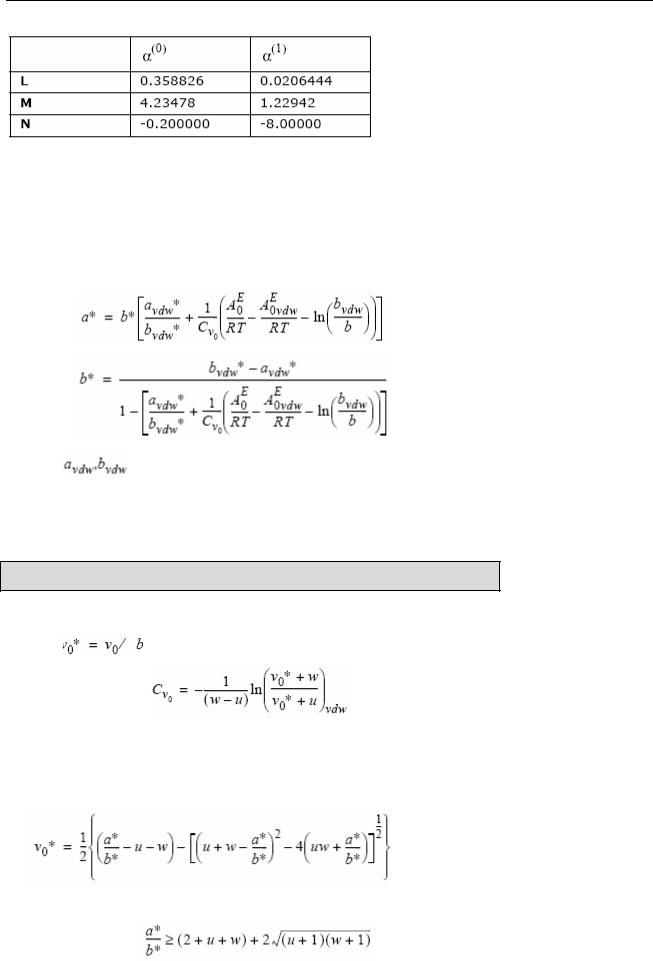
Пакет свойств Гликоли Г - 5
Для Тr>1:
Г.3.2 Правила смешения CEOS/AE при нулевом давлении
Параметры смешения a и b пря нулевом давлении для кубического уравнения состояния определяются следующим образом:
(11)
|
(12) |
где |
- параметры a и b уравнения состояния, полученные из |
правила смешения Ван дер Вальса.
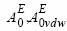 - избыточная энергия Гельмгольца при нулевом давлении.
- избыточная энергия Гельмгольца при нулевом давлении.
Правила смешения 11 и 12 зависят от объема через 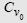 .
.
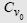 - функция приведенного объема жидкости при нулевом давлении.
- функция приведенного объема жидкости при нулевом давлении.
(13)
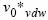 - объем жидкости при нулевом давлении рассчитывается из кубического уравнения состояния с использованием правила смешения Ван дер Вальса для получения параметров a и b, задав давление равным нулю и выбрав наименьший из корней уравнения:
- объем жидкости при нулевом давлении рассчитывается из кубического уравнения состояния с использованием правила смешения Ван дер Вальса для получения параметров a и b, задав давление равным нулю и выбрав наименьший из корней уравнения:
(14)
Уравнение 14 имеет корень при условии:
(15)

Г - 6 Пакет свойств Гликоли
Правило смешения для параметра b в соответствии с уравнением 12 требует, чтобы второй вириальный коэффициент квадратично зависел от состава. В противном случае для параметра b можно воспользоваться простым линейным правилом смешения, что означает, что второй вириальный коэффициент не будет приниматься во внимание.
(16)
Для того, чтобы избежать необходимости расчета 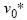 по уравнению состояния, объем Ван-дер-Ваальсовой жидкости при нулевом давлении
по уравнению состояния, объем Ван-дер-Ваальсовой жидкости при нулевом давлении
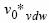 принимается равным константе, r. Уравнение 13 приводится к виду:
принимается равным константе, r. Уравнение 13 приводится к виду:
(17)
где |
- не зависящая от плотности константа, используемая вместо |
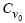 .
.
Уравнения 11 и 12 приводятся к виду:
(18)
(19)
Величина 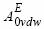 получена по уравнению состояния из предположения постоянства приведенного мольного объема Ван-дер-Ваальсовой жидкости r:
получена по уравнению состояния из предположения постоянства приведенного мольного объема Ван-дер-Ваальсовой жидкости r:
(20)
где  - параметры a и b уравнения состояния, полученные из обычного правила смешения Ван-дер-Ваальса
- параметры a и b уравнения состояния, полученные из обычного правила смешения Ван-дер-Ваальса
(21)
(22)
Избыточная энергия Гельмгольца существенно меньше зависит от давления, чем избыточная энергия Гиббса. Поэтому эту величину для потока Ван-дер-Ваальсовой жидкости при нулевом давлении можно приближенно заменить избыточной энергией Гельмгольца при бесконечно большом давлении:
