
- •1. Основные свойства дисперсных систем
- •2. Классификация дисперсных систем
- •3. Методы получения дисперсных систем
- •4. Основные свойства дисперсных систем определяются нескомпенсированной поверхностной энергией
- •Классификация поверхностных явлений
- •6. Поверхностное явление – адсорбция
- •8. Адсорбция на границе жидкость-газ
- •7. Основные адсорбционные уравнения
- •10. Характеристики твердых адсорбентов. Правила подбора
- •11. Основные теории адсорбции на твердых адсорбентах
- •Основные положения теории мономолекулярной адсорбции Ленгмюра
- •12. Основные положения теории полимолекулярной адсорбции бэт
- •13. Адсорбция в растворах электролитов
3. Методы получения дисперсных систем
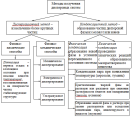
Дисперсные системы получают путем диспергирования (диспергационный метод) или конденсации (конденсационный метод). В первом случае твердые и жидкие вещества тонко измельчают в соответствующей дисперсионной среде, во втором – вызывают образование частиц дисперсной фазы из отдельных молекул или ионов (рис. 3). Необходимым условием получения лиофобной дисперсной системы является нерастворимость или очень малая растворимость вещества дисперсной фазы в дисперсионной среде и наличие в среде веществ, способных стабилизировать частицы дисперсной фазы – стабилизаторов.
4. Основные свойства дисперсных систем определяются нескомпенсированной поверхностной энергией
Наличие значительного избытка свободной поверхностной энергии на межфазной поверхности, значение которой прямо пропорционально удельной поверхности.
Механизм возникновения поверхностной энергии рассмотрим на примере системы жидкость – газ (рис. 2). Для молекул, находящихся в объеме жидкой фазы, силы межмолекулярного взаимодействия симметричны, равнодействующая их равна 0.
Общая поверхностная энергия системы определяется площадью поверхности S и удельной поверхностной энергией , называемой поверхностным натяжением:
Gпов = S. С точки зрения термодинамики, поверхностное натяжение – это работа обратимого процесса образования единицы площади новой поверхности при постоянных температуре Т, давлении р и составе жидкости.
Для образования новой межфазной поверхности необходимо перевести часть молекул из объема жидкости в поверхностный слой, затратив при этом работу против внутреннего давления, стремящегося втянуть молекулы поверхностного слоя внутрь фазы, т. е.
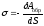 ,
,
где Аобр – термодинамически обратимая работа; она отрицательна, так как совершается над системой.
При р, Т = const
-Aобр = dG,
где G – свободная энергия Гиббса,
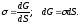
В результате действия текучие системы принимают форму с минимальной поверхностью фазы при заданном объеме – форму сферы. Поэтому такие жидкости называют капельными.
Поверхностное натяжение на границе двух конденсированных фаз называет межфазовым. Оно образуется на поверхности раздела двух взаимно нерастворимых жидкостей, твердого тела с жидкостью и двух твердых тел и обозначается соответственно ж-ж, т-ж, т-т.
Поверхностное натяжение с ростом температуры снижается. Это связано с ростом давления насыщенного пара и уменьшением нескомпенсированности межмолекулярного взаимодействия. Поэтому при оценке значений необходимо указывать температуру.
При 293 К воды составляет 72,75 мДж/м2, подсолнечного масла – 33, сырого молока – 45-60, а сухих вин – 46-52 мДж/м2, что ниже воды.
5.Классификация поверхностных явлений
Дисперсные системы, обладающие большим избытком поверхностной энергии, термодинамически неустойчивы; в них самопроизвольно протекают процессы, приводящие к снижению свободной энергии.
Поверхностные явления – это процессы, происходящие на межфазной поверхности и сопровождающиеся самопроизвольным уменьшением поверхностной энергии Gпов.
Для изобарно-изотермических процессов
Gпов = S.
Снижение поверхностной энергии Gпов может происходить за счет уменьшения поверхности раздела фаз S и поверхностного натяжения .
Поэтому все поверхностные явления в дисперсных системах можно разделить на две группы (схема
.
