
- •Дисциплина: Физическая химия
- •Работа расширения идеального газа.
- •Теплоемкость при постоянном давлении и объеме и связь между ними.
- •Температурная зависимость теплоемкости от температуры.
- •Применение первого закона термодинамики к химическим процессам.
- •Связь между qp и qv.
- •Расчет тепловых эффектов химических реакций по теплотам образования и теплотам сгорания веществ (на примере реакции).
- •4. Зависимость теплового эффекта от температуры. Уравнение Кирхгоффа в дифференциальной и интегральной форме. Зависимость теплового эффекта от температуры.
- •5. Обратимые и необратимые, самопроизвольные и несамопроизвольные процессы. Второй закон термодинамики, его формулировки и математическое выражение. Цикл Карно. Обратимые и необратимые процессы
- •Второй закон термодинамики, его формулировки
- •Цикл Карно
- •Расчет изменения энтропии при различных термодинамических процессах и при протекании химических реакций.
- •Свободная и связанная энергия.
- •7. Основные соотношения между термодинамическими функциями. Уравнение Гиббса-Гельмгольца.
- •Уравнение Гиббса – Гельмгольца
- •Вывод дифференциальной формы уравнения Клаузиуса - Клапейрона для процесса кипения.
- •Интегрирование уравнения Клаузиуса - Клапейрона и его анализ.
- •Признаки равновесных состояний.
- •Закон действующих масс. Вывод константы равновесия для гомогенной реакции.
- •Связь между различными формами выражения констант равновесия.
- •Химическое сродство как мера реакционноспособности системы. Изотерма Вант-Гоффа.
- •Нормальное химическое сродство.
- •11. Зависимость константы равновесия от температуры. Уравнение изобары Вант-Гоффа в дифференциальной и интегральной формах. Уравнение изохоры Вант-Гоффа в дифференциальной и интегральной формах.
- •Метод Темкина–Шварцмана
- •13. Термодинамика и законы разбавленных растворов. Понижение давления пара растворителя над раствором. Закон Рауля.
- •14. Растворимость газов в жидкостях. Закон Генри. Зависимость растворимости газов от различных факторов.
- •15. Замерзание и кипение растворов. Криоскопия и эбуллиоскопия.
Дисциплина: Физическая химия
1. Первой закон термодинамики, основные формулировки и математическое выражение первого закона термодинамики. Применение его к термодинамическим процессам. Работа расширения идеального газа в изохорном, изобарном, изотермическом и адиабатном процессах.
2. Теплоемкость. Виды теплоемкости. Связь между средней и истинной теплоемкостью. Теплоемкость при постоянном давлении и объеме и связь между ними. Температурная зависимость теплоемкости от температуры.
3. Закон Гесса и следствия из него. Применение первого закона термодинамики к химическим процессам. Связь между qp и qv. Расчет тепловых эффектов химических реакций по теплотам образования и теплотам сгорания веществ (на примере реакции).
4. Зависимость теплового эффекта от температуры. Уравнение Кирхгоффа в дифференциальной и интегральной форме.
5. Обратимые и необратимые, самопроизвольные и несамопроизвольные процессы. Второй закон термодинамики, его формулировки и математическое выражение. Цикл Карно.
6. Энтропия как мера неупорядоченности системы. Свободная и связанная энергия. Расчет изменения энтропии при различных термодинамических процессах и при протекании химических реакций.
7. Основные соотношения между термодинамическими функциями. Уравнение Гиббса-Гельмгольца.
8. Применение второго закона термодинамики к фазовым превращениям. Вывод дифференциальной формы уравнения Клаузиуса - Клапейрона для процесса кипения. Интегрирование уравнения Клаузиуса - Клапейрона и его анализ.
9. Химическое равновесие. Классификация равновесных состояний. Признаки равновесных состояний. Закон действующих масс. Вывод константы равновесия для гомогенной реакции. Связь между различными формами выражения констант равновесия.
10. Химическое равновесие в гетерогенных системах. Расчет константы равновесия. Химическое сродство как мера реакционноспособности системы. Изотерма Вант-Гоффа. Нормальное химическое сродство.
11. Зависимость константы равновесия от температуры. Уравнение изобары Вант-Гоффа в дифференциальной и интегральной формах. Зависимость константы равновесия от температуры. Уравнение изохоры Вант-Гоффа в дифференциальной и интегральной формах.
12. Расчет равновесных состояний с помощью таблиц стандартных термодинамических величин и по методу Тёмкина-Шварцмана
13. Термодинамика и законы разбавленных растворов. Понижение давления пара растворителя над раствором. Закон Рауля.
14. Растворимость газов в жидкостях. Закон Генри. Зависимость растворимости газов от различных факторов.
15. Замерзание и кипение растворов. Криоскопия и эбуллиоскопия.
16. Закон распределения. Экстракция.
17. Химический потенциал и общие условия равновесия системы.
18. Термодинамика и законы реальных растворов. Положительные и отрицательные отклонения от закона Рауля. Перегонка. Законы Коновалова.
19. Диаграмма состояния однокомпонентных систем Диаграммы состояния воды .
20. Термический анализ. Построение диаграмм состояния по кривым охлаждения. Анализ диаграмм состояния по конноде и по правилу фаз Гиббса. Анализ диаграмм состояния двухкомпонентных систем с неограниченной растворимостью в твердом и жидком состоянии.
21. Анализ трехкомпонентных систем. Объемные и плоские диаграммы состояния трехкомпонентных систем. Треугольники концентраций. Определение концентраций по методам Гиббса и Розебома.
22. Теория электролитической диссоциация. Степень диссоциации. Изотонический коэффициент. Закон Оствальда.
23. Электролиты. Электролитическая проводимость растворов электролитов: удельная и эквивалентная. Зависимость этих электропроводностей от концентрации.
24. Гальванические элементы. Механизм возникновения электродного потенциала. Строение двойного электрического слоя. Вывод уравнения Нернста. Элемент Якоби-Даниэля.
25. Измерение электродвижущие силы гальванического элемента. Классификация электродов. Типы электродов. Электроды первого, второго и третьего рода. Электроды сравнения.
26. Кинетика химических реакций. Задачи кинетики. Понятие о скорости. Виды скорости. Молекулярность и порядок реакций.
27. Кинетика простых реакций. Вывод кинетического уравнения для реакции первого, второго и третьего порядка. Период полураспада.
28. Порядок реакции. Методы определения порядка реакции.
29. Зависимость скорости реакции от температуры. Правило Вант-Гоффа. Энергия активации и методы её определения.
30. Теория активных столкновений Аррениуса.
1. Первой закон термодинамики, основные формулировки и математическое выражение первого закона термодинамики. Применение его к термодинамическим процессам. Работа расширения идеального газа в изохорном, изобарном, изотермическом и адиабатном процессах.
Содержание и формулировки первого закона термодинамики
Первый закон («первое начало») термодинамики есть частный случай закона сохранения и превращения энергии применительно к процессам, которые сопровождаются выделением, поглощением или преобразованием теплоты. Первый закон был обоснован работами Гесса (1836), Джоуля (1840), Майера (1842), Гельмгольца (1847) и др. Наиболее обычными формулировками первого закона термодинамики являются следующие:
энергия, полученная системой в форме теплоты, может превращаться в работу и, наоборот, полученная в форме работы - в теплоту; если по окончании превращений система возвращается в исходное состояние, то теплота и работа равны друг другу, независимо от характера процесса (Гельмгольц): W= Q;
вечный двигатель первого рода невозможен, т. е. невозможно построить машину, которая совершала бы механическую работу, не затрачивая на это соответствующего количества энергии (Оствальд);
в любой изолированной системе запас энергии остается постоянным (Джоуль):U= const, dU = 0.
Математическое выражение первого закона термодинамики
Взаимосвязь между внутренней энергией, работой и теплотой устанавливается на основе первого закона термодинамики.
Изменение внутренней энергии системы ΔU может происходить за счет обмена теплотой Q и работой А с окружающей средой. В термодинамике условились считать положительными величинами теплоту, полученную системой, и работу, совершенную системой.
Тогда из формулировки первого закона термодинамики следует, что теплота, полученная системой извне, расходуется на приращение внутренней энергии и работу, совершенную системой, т. е.
Q = ΔU+W.
Если эти количества бесконечно малы, то закон записывается в дифференциальной форме:
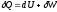 ,
,
где dU- полный дифференциал внутренней энергии системы; δQ и δW - бесконечно малые количества теплоты и работы.
Применение закона к термодинамическим процессам
Изотермический процесс (Т=соnst) в идеальном газе силы межмолекулярного взаимодействия равны нулю. Внутренняя энергия идеального газа зависит от температуры, количества вещества и не зависит от давления и объема, поэтому для данных условий U=соnst; dU=0, dQТ=р·dV ; QТ=W теплота, сообщенная системе, в изотермическом процессе полностью расходуется на совершение работы расширения. используя р=RТ/V и проинтегрировав получим W= RТln(V2/V1) = RТln(Р1/Р2), т.к. по закону Бойля-Мариотта (РV)Т = соnst
Изохорный процесс (V= соnst) при постоянном объеме dV=0, значит работа расширения газа dW= рdV=0 и dQ V = dU или Q = U2- U1 =dd U
В изохорном процессе теплота, сообщенная системе, полностью расходуется на увеличение ее внутренней энергии и характеризует изменение состояния системы.
Изобарный процесс (р= соnst) постоянную величину р можно внести под знак дифференциала, поэтому работа расширения dW = рdV =dW = d(рV) и dQр=dU+d(рV) = d(U +рV)= ΔН
Работа расширения идеальных газов
Идеальный газ – это газ для идеализированной системы, состоящей из частиц, собственный объем которых мал по сравнению со всем объемом системы, и которые находятся в непрерывном хаотическом движении.
Работу принято считать положительной (А > 0), если система производит её над окружающей средой. Различают работу: механическую, поверхностных сил, электрическую и т. п. Механическую работу под действием сил давления называют работой расширения.
Выясним, какое количество работы совершит газ при расширении.
Рассмотрим обратимое расширение газа в цилиндре постоянного сечения S.
Обозначим: р- внешнее давление; dh- бесконечно малое смещение поршня.
Будем
считать, что поршень движется без трения.
Зная, что сила, под действием которой
смещается поршень, будет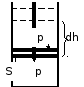
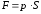 .
.
Тогда работа будет равна:
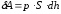 .
.
Так
как произведение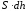 -
это изменение объема
-
это изменение объема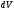 ,
то
,
то![]() ,
и для конечного изменения объема от
,
и для конечного изменения объема от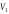 до
до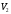
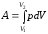 .
.
Четыре частных случая:
1) Изобарный процесс. р=const. Тогда интегрирование приводит к выражению:
![]() ,
,
т.
е. работа изобарного расширения газа
равна произведению давления на увеличение
объема.
На
графике р
- V
эта работа выражается площадью
прямоугольника
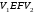 .
.
Для
1-го моля воспользуемся уравнением
Клапейрона - Менделеева
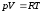 .
Тогда можно записать:
.
Тогда можно записать:
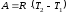 .
.
2) Изотермический процесс. Т=const. Из уравнения Клапейрона - Менделеева

Подставив
которое в выражение
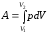 ,
получим:
,
получим:
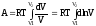 .
.
В результате интегрирования получим:
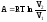 .
.
На графике р-V эта работа выражается площадью V1EF/V2.
Зная
из закона Бойля-Мариотта что
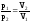 ,
получим:
,
получим:
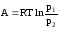 .
.
3) Адиабатное расширение происходит при одновременном изменении температуры и давления, оно отвечает условию: dQ=0.
Газ не получает теплоту, поэтому работа расширения газа происходит за счет внутренней энергии. При этом газ должен охлаждаться. Внутренняя энергия зависит только от температуры.
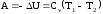 .
.
На графике p-V это площадь V1EF//V2..
4) Изохорный процесс. V = const, dV = 0, А = 0.
