
- •4. Диеновые углеводороды (алкадиehы)
- •4.1. Изомерия и номенклатура диенов
- •4.2. Способы получения диенов
- •4.4. Химические свойства сопряженных диенов
- •4.4.1. Гидрирование
- •4.4.2. Галогенирование
- •4.4.3. Гидрогалогенирование
- •4.4.4. Гипогалогенирование
- •4.4.5. Димеризация диенов
- •4.4.6. Диеновый синтез
- •4.4.7. Теломеризация
- •4.4.8. Полимеризация
- •4.5. Отдельные представители и применение диенов
4. Диеновые углеводороды (алкадиehы)
4.1. Изомерия и номенклатура диенов
Диеновые углеводороды имеют две двойные связи в молекуле, т. е. на четыре атома водорода меньше, чем соответствующие им предельные углеводороды. Общая формула алкадиенов СnН2n-2. Поскольку для образования двух двойных связей необходимо по крайней мере три атома углерода, в этом ряду гомологи с одним и двумя атомами углерода не существуют.
В зависимости от взаимного расположения двойных связей диеновые углеводороды можно разделить на три основных типа:
диены с кумуллированными двойными связями, т.е. с двойными связями у одного углеродного атома (алленовые);
диены с конъюгированными (сопряженными) двойными связями;
3) диены с изолированными двойными связями
Диены по систематической номенклатуре называются так же, как и этиленовые углеводороды, только вместо суффикса -ен ставится суффикс -адиен (так как двойных связей две). Положение двойных связей, как обычно, показывают цифрами. Для некоторых диенов сохранились тривиальные или старые рациональные названия:
СН2=С = СН2 пропадиен, аллен
СН3—СН=С=СН2 1,2-бутадиен, метилаллен
СН2=СН—СН=СН2 1,3-бутадиен, дивинил
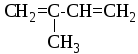 2-метил-1,3-бутадиен,
изопрен
2-метил-1,3-бутадиен,
изопрен
СН3—СН=СН—СН=СН2 1,3-пентадиен, пиперилен
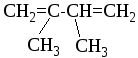 2,3-диметил-1,3-бутадиен
2,3-диметил-1,3-бутадиен
СН2=СН—СН2—СН2—СН=СН2 1,5-гексадиен, диаллил
4.2. Способы получения диенов
Способы получения углеводородов диенов в большинстве случаев не отличаются от способов получения олефинов, только соответствующие реакции необходимо проводить дважды или в качестве исходного вещества применять соединения, уже содержащие двойную связь.
4.2.1. Дегидрирование алкан-алкеновых фракций:
Дегидрирование бутан-бутеновых и пентан-пентеновых фракций над катализаторами (обычно используется Cr2О3) приводят к образованию диенов:

4.2.2. Получение дивинила и изопрена дегидратацией гликолей



4.2.3. Дегидратация непредельных спиртов

4.2.4. Получение дивинила димеризацией ацетилена с последующим гидрированием
![]()
4.2.5. Синтез Реппе
Синтез основан на высокой подвижности водорода у тройной связи, благодаря чему он легко вступает во взаимодействие с карбонильными соединениями, в том числе и с метаналем:

Аналогично получают изопрен (способ Фаворского), используя в качестве карбонильного соединения ацетон.
4.3. Физические свойства и строение диенов
Алены (1,2-диены). В молекуле аллена и других соединений с кумулированными связями, π-связи располагаются в двух взаимно перпендикулярных плоскостях. Плоскости, в которых располагаются две пары водородных атомов, также взаимно перпендикулярны. Два крайних углеродных атома алленовой системы находятся в состоянии sp2-гибридизации, средний – sp-гибридизации (рис. 4).
Эти особенности квантово-механического строения проявляются в физических и химических свойствах алленов. В частности, в ряду алленов при двух различных заместителях у конечных углеродных атомов возможна оптическая активность благодаря молекулярной асимметрии. Два пространственных изомера, относящиеся друг к другу как предмет к своему зеркальному изображению, при наложении не совпадают и, следовательно, представляют собой две различные изомерные молекулы.

Рис. 4. Строения молекулы аллена
Для алленов характерны легкость гидратации разбавленной серной кислотой с образованием кетонов, способность полимеризоваться или конденсироваться с другими непредельными соединениями с образованием четырехчленных циклов (С. В. Лебедев):

Сопряженные диены (1,3-диены). Сопряженные диены отличаются от алкенов большей устойчивостью, а также способностью вступать в реакции присоединения по атомам 1,2 и 1,4 и большей реакционной способностью.
Две сопряженные π-связи образуют общее электронное облако — все четыре углеродных атома находятся в состоянии sp2-гибридизации. Это приводит к укорочению простой связи и к стабилизации молекулы. В молекуле дивинила π-связи образованы за счет перекрывания р-орбиталей атомов С1 и С2, Сз и С3. Также возможно перекрывание р-орбиталей атомов С2 и С3. Возникающая в результате этого делокализация π -электронов делает молекулу более устойчивой, поскольку каждая пара электронов притягивается не двумя, а четырьмя ядрами углерода:

Рис. 5. Строение молекулы дивинила
Связь С2 – С3 приобретает некоторый характер двоесвязанности. Длина ее меньше, чем в алканах (1,48 Å), что вызвано эффектом сопряжения. Это и объясняет поведение диенов в реакциях электрофильного присоединения, где реагент может присоединяться не только к соседним атомам при кратной связи (1,2-присоединение), но и к двум концам сопряженной системы (1,4-присоединение).
Физические свойства диенов. Дивинил при обычных условиях – газ. Изопрен и другие простейшие алкадиены – жидкости. Обычные закономерности, свойственные гомологическим рядам углеводородов, действуют и в этом ряду.
Для алкадиенов с сопряженными двойными связями характерны аномально высокие показатели преломления света. Благодаря этой особенности найденные молекулярные рефракции алкадиенов значительно больше вычисленных. Разница между найденной и вычисленной величинами составляет обычно 1–1,5 единицы. Она называется молекулярной экзальтацией.
Алкадиены поглощают ультрафиолетовое излучение в значительно более длинноволновой области, чем алкены. Например, 1,3-бутадиен поглощает при 217 нм. Накопление в молекуле сопряженных двойных связей ведет к дальнейшему смещению максимума поглощения из ультрафиолетовой области в видимую область: при четырех сопряженных двойных связях появляется желтая окраска.
В ИК-спектрах для 1,3-алкадиенов характерно снижение частоты и увеличение интенсивности полосы валентных колебаний двойных связей (примерно до 1600 см-1).
Наибольшее практическое значение имеют сопряженные диены.
