
- •С.А. Сергеева, в.Е. Рябинин Практикум по химии
- •Рекомендовано
- •Оглавление
- •Введение
- •Общие вопросы выполнения лабораторных работ
- •1.1. Правила работы в химической лаборатории
- •Правила оказания первой помощи пострадавшим в химической лаборатории
- •1.3. Правила ведения лабораторного журнала
- •Тема: Растворы. Способы выражения концентрации растворов. Основы титриметрического анализа. Метод нейтрализации
- •1.Основные правила техники безопасности при работе в химической лаборатории и правила ведения лабораторного журнала.
- •2.Растворы (определение, классификация).
- •3.Титриметрический метод анализа (понятие и виды).
- •4. Метод кислотно-основного титрования (определение, основное уравнение).
- •1. Практическая часть
- •1.3. Контрольные вопросы и задачи
- •2. Экспериментальная часть
- •Экспериментальные данные и результаты измерений
- •Экспериментальные данные и результаты измерений
- •I. Информационный раздел
- •Концентрация кодеина и морфина в моче у 3-х испытуемых
- •II. Аналитический раздел
- •Тема: Коллигативные свойства растворов неэлектролитов и электролитов
- •1. Вода как универсальный биологический растворитель.
- •2. Коллигативные свойства растворов (определение, виды).
- •1. Практическая часть
- •Суточный баланс воды в организме взрослого человека
- •Состав растворов Рингера –Локка и Тироде для теплокровных животных
- •II. Давление пара разбавленных растворов. Закон Рауля
- •2.1.Давление насыщенного пара растворителя
- •1.3. Контрольные задачи
- •2. Экспериментальная часть
- •Криоскопическим методом
- •Экспериментальные данные и результаты измерений
- •4. Вопросы по теме для самостоятельного изучения их студентами.
- •Тема: Протолитические равновесия и процессы. Водородный показатель. Гидролиз
- •1. Электролиты сильные и слабые.
- •3.Гидролиз (определение, причина и следствие, смещение равновесия гидролиза).
- •1. Практическая часть
- •1.3. Контрольные вопросы
- •2. Экспериментальная часть
- •Реакция среды при гидролизе солей
- •4. Вопросы по теме для самостоятельного изучения их студентами.
- •Тема: Буферные системы, классификация и механизм действия
- •1. Практическая часть
- •2. Экспериментальная часть
- •Ацетатного буферного раствора по кислоте и щелочи
- •Экспериментальные данные и результаты измерений
- •4. Вопросы по теме для самостоятельного изучения их студентами.
- •5. Практические навыки, которыми должен овладеть студент по теме занятия.
- •Десятичные приставки к названиям единиц
- •Содержание газов в артериальной и венозной крови, л/1 л крови
- •Парциальное давление и напряжение газов, кПа (мм рт. Ст.)
- •Проверка ёмкости мерной посуды
- •Формулы перехода от одних выражений концентраций растворов к другим
- •Константы некоторых жидкостей, применяемых в качестве растворителей
- •Ионное произведение воды при температуре от до:
- •Константы диссоциации некоторых слабых электролитов в водных растворах при
- •Характеристика важнейших индикаторов
- •Средние значения водородного показателя (рН) биологических жидкостей
- •Расчет в растворах кислот и оснований
- •Состав смешанной слюны человека
- •Список литературы Основная литература
- •Дополнительная литература
2. Экспериментальная часть
Лабораторная работа. Определение буферной ёмкости
Ацетатного буферного раствора по кислоте и щелочи
Цель работы. Экспериментально сопоставить буферную ёмкость ацетатного буфера по кислоте и по основанию.
Оборудование: набор пробирок в штативе; бюретки вместимостью 25 мл; воронки диаметром 30 м; колбы конические вместимостью 250 мл ; градуированные пипетки на 10 мл
Реактивы: соляная кислота, растворы уксусной кислоты, гидроксида и ацетата натрия (все по 0,1 моль/л); растворы метилового оранжевого и лакмоида в этаноле.
Ход работы:
В колбах 1 и 3 приготовьте по 10 мл исследуемого ацетатного буферного раствора, смешивая по 5 мл
 и
и с равными молярными концентрациями
(0,1 М) компонентов.
с равными молярными концентрациями
(0,1 М) компонентов.В колбах 2 и 4 приготовьте буферные растворы-свидетели с соотношением концентрацией (0,1 М) соли и кислоты, равными 9:1 (в колбе 2) и 1:9 (в колбе 4).
В колбы 1 и 2 (определение буферной ёмкости по кислоте) добавьте по 2-3 капли раствора метилового оранжевого, растворы перемешивайте. Запишите окраску обоих буферных растворов, а затем оттитруйте 1- колбу 0,1 М раствором соляной кислоты
 до получения окраски одинаковой с
окраской раствора свидетеля.
до получения окраски одинаковой с
окраской раствора свидетеля.

В колбы 3 и 4 (определение буферной ёмкости по основанию) добавьте по 2-3 капли раствора лакмоида, растворы перемешивайте. Запишите окраску растворов и оттитруйте 3- колбу 0,1 М раствором натрий гидроксида
 до
получения окраски одинаковой с окраской
свидетеля.
до
получения окраски одинаковой с окраской
свидетеля.Результаты внесите в таблицу № 5.1.
Таблица 5.1
Экспериментальные данные и результаты измерений
|
№ колбы |
Содержимое колбы |
Состав раствора |
рН до титрования |
рН после титрования |
Окраска |
Объем титранта
|
| ||
|
|
после добавления индикатора |
после титрования |
HCl |
NaOH | |||||
|
1 |
Исследуемый раствор |
По кислоте (с метиловым оранжевым) | |||||||
|
5:5 |
|
|
|
|
|
|
| ||
|
| |||||||||
|
2 |
Раствор-свидетель |
9:1 |
|
|
|
|
|
|
|
|
3 |
Исследуемый раствор |
По основанию (с лакмоидом) | |||||||
|
5:5 |
|
|
|
|
|
|
| ||
|
| |||||||||
|
4 |
Раствор-свидетель |
1:9 |
|
|
|
|
|
|
|
Рассчитайте буферную ёмкость по кислоте и по основанию по формулам:
п
 о
кислоте
о
кислоте

по основанию

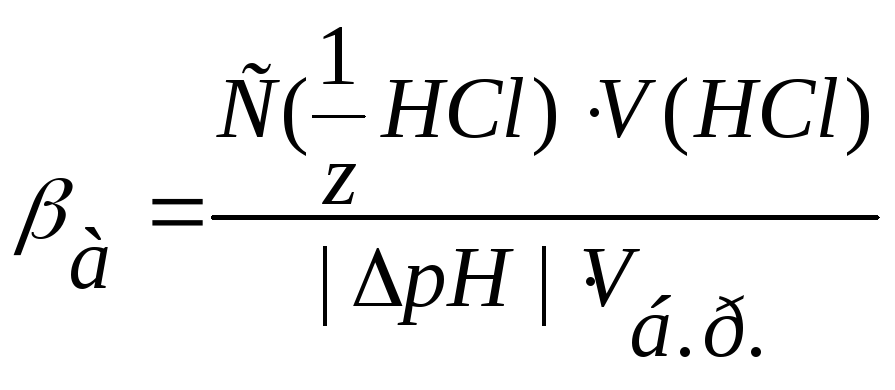

Выводы. Согласуется ли полученное значение водородной функции с литературными данными? Чем может быть вызвано отклонение, если оно есть? Используя соотношение концентраций компонентов, находящихся в сыворотке крови буферных систем:
 объясните, почему ее буферная ёмкость
по кислоте больше, чем по основанию?
объясните, почему ее буферная ёмкость
по кислоте больше, чем по основанию?
3. Контроль усвоения темы (тесты для самоконтроля уровня текущих знаний).
Образец теста
Наибольшей кислотопродуцирующей активностью обладает микрофлора зубного и язычного налета, в этой связи для выявления величины [H+] кислотного буферного раствора справедливо выражение _____.
1) ![]()
2) ![]()
3) ![]()
4) [H+]
=
![]()
Многие продукты, главным образом белоксодержащие, имеют в своем составе вещества (мочевина, нитраты, нитриты, глутамин и др.), которые при диссоциации в ротовой жидкости образуют ионы, главным образом
 ,
связывающие
Н+.
При этом наблюдается незначительный
сдвиг рН
в
щелочную
сторону, который не превышает 8,0.
В
этой связи
для
выявления величины
рН основного
буферного раствора
справедливо выражение _____.
,
связывающие
Н+.
При этом наблюдается незначительный
сдвиг рН
в
щелочную
сторону, который не превышает 8,0.
В
этой связи
для
выявления величины
рН основного
буферного раствора
справедливо выражение _____.
1) ![]()
2) ![]()
3) ![]()
4) ![]()
Для проведения биохимических исследований необходимо приготовить буферную систему путем смешивания строго рассчитанных количеств
 и
и
 .
Таким способом полученный буферный
раствор относится к типу систем –
_____.
.
Таким способом полученный буферный
раствор относится к типу систем –
_____.
1) кислотным
2) основным
3) солевым
4) амфотерным
Для диагностики заболевания необходимо установить кислотно-основное состояние ротовой жидкости, которое определяется количественным содержанием компонентов гидрокарбонатного буфера. В этой связи для оценки данного состояния рекомендуют воспользоваться уравнением Гендерсона-Гассельбаха – ______.
1) ![]()
2) ![]()
3) ![]()
4) ![]()
При проведении клинических исследований к образцу ротовой жидкости больного было добавлено небольшое количество
 .
Однако это не привело к изменениюрН,
а вызвало увеличение концентрации
одного из неорганических компонентов
– _____.
.
Однако это не привело к изменениюрН,
а вызвало увеличение концентрации
одного из неорганических компонентов
– _____.
1) ![]()
2) ![]()
3) ![]()
4) ![]()
Для определения влияния различных факторов (например, влияние кислой реакции желудочного сока) на кинетическую активность фермента карбогидразы слюны, необходимо приготовить гидрокарбонатный буфер, который моделирует основную буферную систему ротовой жидкости. Компонентами этой системы являются – _____.
1) ![]()
2) ![]()
4) ![]()
5) ![]()
При случайном попадании аммиачного буфера в глаз (среда щелочная), то глаз необходимо промыть большим количеством холодной воды, стараясь держать глаза все время открытыми и _____.
1) наложить марлевую повязку
2) закапать 3%- ный раствор гидрокарбоната натрия
3) закапать 2% -ный раствор борной кислоты.
4) наложить марлевую повязку, смоченную раствором сульфата меди.
Для подтверждения буферного действия растворов альбуминов крови, к двум образцам были добавлены небольшие количества неорганической кислоты и щелочи. При этом изменения рН не наблюдалось. Этим объясняются _____ свойства белков.
1) растворимые
2) амфотерные
3) кислотные
4) основные
Максимальной буферной ёмкостью обладает буферная система, у которой _____.
1)
![]()
2)
![]()
3)
![]()
4)
![]()
Ацидоз – это ______.
1) постоянство буферной емкости крови по кислоте
2) уменьшение кислотной буферной емкости крови
3) уменьшение щелочных резервов крови
4) повышение щелочных резервов крови
Один из нижеуказанных факторов – _____ сильней влияет на величину рН буфера.
1) соотношение концентраций компонентов
2) величина рКа или рКв
3) концентрация акцептора протонов
4) концентрация донора протонов
