
- •Экспериментальные подтверждения
- •2. Некоторые свойства волн де Бройля
- •3. Соотношения неопределенностей
- •4. Волновая функция и ее статистический смысл
- • Волновая функция; постоянная Планка; m масса частицы; оператор Лапласа; u ( X, y, z, t ) потенциальная энергия частицы в силовом поле; мнимая единица.
- •5. Уравнение Шрёдингера для стационарных состояний
- •Глава 6. Физика атома и атомного ядра
- •Глава 6. Физика атома и атомного ядра
Лекция 11
Элементы квантовой механики
Вопросы
1. Корпускулярно-волновой дуализм свойств веществ.
2. Некоторые свойства волн де Бройля.
3. Соотношения неопределенностей.
4. Волновая функция и ее статистический смысл.
1. Корпускулярно-волновой дуализм свойств веществ
Рис.
1. Иллюстрация
идеи де Бройля возникновения стоячих
волн на стационарной орбите для случая
n = 4.
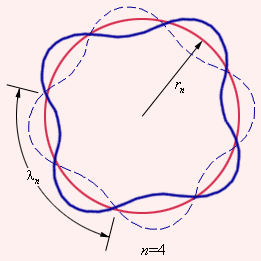
Луи де Бройль выдвинул в 1923 г. гипотезу об универсальности корпускулярно-волнового дуализма: с каждым микрообъектом (не только фотоном, но и электроном и др. частицами) связаны с одной стороны корпускулярные характеристики (энергия Е, импульс Р), а с другой стороны волновые характеристики (частота и длина волны ).
![]()
![]()
![]() ;
;
![]() ;
;
![]()
![]()
![]() .
(1)
.
(1)
Это длина волны де Бройля, отвечающая движению частицы вещества.
Экспериментальные подтверждения
Американские физики К. Дэвиссон (1881 – 1958) и Л. Джермер (1896 – 1971) обнаружили в 1927 году, что пучок электронов, рассеиваясь от естественной дифракционной решетки (кристалла никеля) дает отчетливую дифракционную картину, соответствующую формуле Вульфа – Брэггов.
2. В 1928 году английский физик Дж. Томсон (сын Дж. Томсона, открывшего за 30 лет до этого электрон) получил новое подтверждение гипотезы де Бройля. В своих экспериментах Томсон наблюдал дифракционную картину, возникающую при прохождении пучка электронов через тонкую поликристаллическую фольгу из золота.
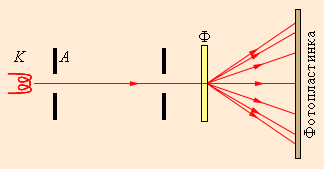
Рис. 2. Упрощенная схема опытов Дж. Томсона по дифракции электронов.
K – накаливаемый катод, A – анод,
Ф – фольга из золота.
Рис. 3. Картина дифракции электронов на поликристаллическом образце при длительной экспозиции (a) и при короткой экспозиции (b).

В 1948 году советский физик В.А. Фабрикант (р. 1907) показал, что волновые свойства присущи не только пучку, но и каждому электрону в отдельности. Для слабого пучка (промежуток времени между электронами больше в 104 раз времени прохождения электроном прибора) при длительной экспозиции была получена дифракционная картина.
Открытие волновых свойств микрочастиц привело к новым методам исследования: электронографии, нейтронографии, к новой отрасли науки – электронной оптики.
Для макроскопического тела m = 1 г, v = 1 м/c:
![]() ,
такая длина волны не обнаруживается
решеткой.
,
такая длина волны не обнаруживается
решеткой.
2. Некоторые свойства волн де Бройля
Рассмотрим свободно движущуюся частицу массой m со скоростью v.
![]()
![]()
 ,
(2)
,
(2)
т.е. фазовая скорость может быть больше скорости света.
3. Соотношения неопределенностей
Из-за двойственной природы частиц необходимо внести ограничения в применение к объектам микромира законов и понятий классической механики.
В классической механике частица имеет траекторию, в любой момент времени зафиксирована ее координата и импульс.
Микрочастица из-за волновых свойств существенно отличается от классической частицы. Нельзя говорить о траектории и одновременно точных координатах и импульсе. Понятие «длина волны» лишено физического смысла, т.к. импульс выражается через длину волны (Р = h/).
В связи с этим немецкий физик Вернер Гейзенберг сформулировал в 1927 г общий принцип, получивший название принципа неопределенности: микрочастица не может иметь одновременно и определенную координату (x) и определенную соответствующую проекцию импульса (Рx), причем неопределенности этих величин удовлетворяют условию
![]()
![]()
![]() .
(3)
.
(3)
Смысл (3) состоит в том, что, чем больше масса частицы, тем меньше неопределенность ее координаты и скорости, тем с большей точностью может быть найдена ее траектория.
Пример 1. Пылинка массой m = 10-12 кг размером l = 10-6 м, координата определена с точностью 0,01 ее размера (x = 10-8м). Неопределенность скорости
![]()
мала и не будет сказываться на скорости движения пылинки. Для описания ее движения можно пользоваться законами классической механики.
Пример 2. Пучок электронов в трубке осциллографа движется со скоростью v = 108 м/c, определяемой с точностью 0,01% (vx = 104 м/c). Неопределенность координаты электрона
![]()
значительно меньше разрешающей способности глаза (0,1 мм = 110-4 м), поэтому движение пучка электронов можно описывать законами классической механики.
Пример 3. Электрон в атоме водорода. Неопределенность координат электрона равна размеру атома (x 10-10 м)
![]() ,
,
неопределенность скорости в несколько раз больше самой скорости (v 2,3 106 м/c). Т.о., нельзя пользоваться законами классической механики для описания движения электрона.
Соотношение неопределенностей для энергии и времени: система, имеющая среднее время жизни t, не может быть охарактеризована определенным значением энергии; разброс энергии Е=h/t возрастает с уменьшением среднего времени жизни:
![]() (4)
(4)
Соотношения неопределенностей предмет дискуссий. Идеалистическое толкование соотношение неопределенностей устанавливает границу познаваемости мира. На самом деле это соотношение не ставит предела познанию микромира, а указывает, насколько применимы к нему понятия классической механики.
Идея де Бройля послужила исходным пунктом квантовой механики, созданной в 1926 - 1927 г. трудами В. Гейзенберга, М. Борна, Э. Шредингера, и П.Дирака.
