
Химсопрмат
.pdf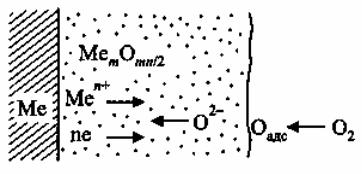
представлена схема образования сплошной оксидной пленки при окислении металла кислородом из газовой фазы.
Рис. 1.4. Схема процесса образования пленки на металле
Процесс окисления металла протекает в несколько стадий [24]:
1)ионизация металла и переход его в форме ионов и электронов в слой оксида;
2)перемещение ионов металла Меn и электронов в слое оксида;
3)перенос кислорода из газового потока к поверхности оксида;
4)адсорбция кислорода на поверхности;
5)превращение адсорбированного кислорода в ион О2 ;
6)перемещение ионов кислорода О2 в слое оксида;
7)реакция образования оксида.
В некоторых случаях отдельные стадии процесса могут выпадать или трансформироваться. Но в целом все стадии процесса взаимосвя-
заны и протекают последовательно. Суммарная скорость процесса определяется скоростью самой медленной реакции. Например, если медленно протекает стадия (3), то процесс лимитируется внешней диффузией, если (1), (2) или (6) – имеет место контроль процесса за счет внутренней диффузии.
Отличительной особенностью газовой коррозии металла в от-
дельных случаях является затухание процесса во времени. Это про-
исходит тогда, когда на поверхности металла образуется защитная пленка. Если эта пленка является сплошной и имеет хорошую адге-
39
зию к поверхности, то она изолирует металл от контакта с агрессив-
ной средой, и коррозия прекращается.
Главным этапом процесса газовой коррозии можно считать адсорбцию окислителя на поверхности металла. Она может быть мономолекулярной и полимолекулярной [1].
Молекулы O2 адсорбируются на поверхности металла обратимо.
Количество адсорбата на единицу поверхности возрастает с увеличением отношения давления кислорода над адсорбатом к давлению насыщенного пара кислорода при соответствующей температуре.
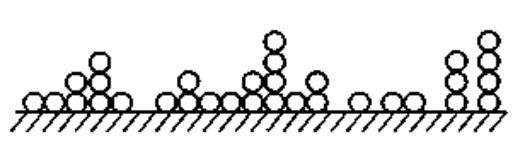
Первоначально происходит мономолекулярная адсорбция, а затем имеет место многослойная физическая адсорбция [24] (рис. 1.5).
Рис. 1.5. Схема заполнения поверхности адсорбента при многослойной адсорбции
В первый момент кислород поглощается с выделением значительного количества теплоты (понижением изобарного потенциала), т.е. самопроизвольно, в дальнейшем кислород поглощается с меньшим тепловым эффектом.
Химическая связь между адсорбированным кислородом и металлом имеет ионный характер. Электроны металла притягиваются к атомам кислорода, которые превращаются в отрицательные частицы
O2 . Оксид формируется, когда взаимное расположение катионов металла и анионов кислорода будет отвечать структуре кристаллической решетки оксида.
Адсорбированные ионы O2 могут проникать под поверхность металла и формировать оксид в его глубине (рис. 1.6) [24].
40
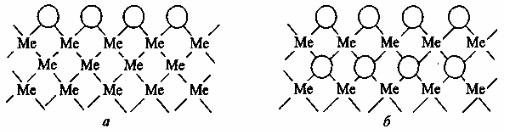
Рис. 1.6. Схема строения слоя хемосорбированного кислорода на металле (а) и строения оксида (б):
Ме– металл; О– кислород
Образование хемосорбированного слоя кислорода происходит быстро, а стадия проникновения ионов кислорода в глубь и формиро-
вание оксида – более медленно.
Тонкий слой оксида имеет мелкокристаллическую структуру, ко-
торая с ростом температуры может переходить в более крупные заро-
дыши. Такие зародыши охватывают всю поверхность металла, и мел-
кокристаллическая пленка оксида перекристаллизовывается в более крупные кристаллы.
Так, при химическом взаимодействии углеродистых сталей с ки-
слородом воздуха на поверхности образуется окалина – оксидная пленка, в состав которой при умеренно высоких температурах входит гематит (Fe2O3 ) и магнетит (Fe3O4 ), при более высоких температурах нагрева (более 575° С) на поверхности раздела окалина-металл воз-
никает еще один оксид железа – вюстит (FeO) (рис. 1.7). Одновре-
менно с процессом окисления железа идет процесс обезуглерожива-
ния поверхности стали, в результате чего цементитная фаза «вымыва-
ется» с поверхности стали. При увеличении времени нагрева глубина обезуглероженного слоя увеличивается и может достигнуть несколь-
ких миллиметров, что приведет к снижению прочности и твердости поверхности металла.
С повышением давления скорость коррозии резко возрастает вследствие наличия в газовой среде водорода, который при повы-
шенном давлении вызывает водородное охрупчивание стали.
41

а |
б |
Рис.1.7. Схема (а) и строение (б) окалины, образующейся на железе
при его окислении на воздухе
1.5. Защитные пленки на металлах
Большинство металлов при взаимодействии с кислородом возду-
ха или другими окислителями покрывается пленкой окисла или дру-
гого соединения.
Первой стадией взаимодействия металлов с коррозионной средой является адсорбция окислительного компонента среды (О2, H2O, CO2, SO2 и Cl2) на поверхности металла. После насыщения поверхности металла хемосорбированным окислителем, что происходит почти мгновенно и приводит к образованию окислителя, при низких темпе-
ратурах может иметь место и физическая адсорбция окислителя за счет сил Ван-дер-Ваальса поверх хемосорбированного слоя.
При наличии химического сродства между металлом и окислите-
лем хемособированная пленка быстро переходит в состояние оксид-
ной пленки в результате протекания химической реакции [1]:
mMe |
mn |
mMen |
mn |
2 Me |
|
. |
(1.9) |
|
|
mn/ 2 |
|||||
2 |
2 |
m |
|
|
|||
|
|
|
|
||||
42
Таким образом, при химическом взаимодействии окислительный компонент внешней среды, отнимая у металла валентные электроды,
одновременно вступает с ним в химическое соединение – продукт коррозии, который в большинстве случаев образует на поверхности корродирующего металла пленку.
Толщина пленок продуктов коррозии на металлах h изменяется в широких пределах. Пленки по толщине принято подразделять на три группы [1-4, 15, 20, 24]:
1)тонкие (невидимые) пленки толщиной от мономолекулярного слоя до 40 нм;
2)средние пленки (видимые благодаря интерференционному ок-
рашиванию как цвета побежалости – см. табл. 1.1), имеющие толщи-
ну от 40 нм до 500 нм; 3) толстые (видимые) пленки толщиной более 500 нм.
|
Цвета побежалости материалов |
Таблица 1.1 |
|||
|
|
||||
|
|
|
|
|
|
Углеродистые стали |
Коррозионностойкие стали и жаропрочные |
||||
|
сплавы |
|
|||
|
|
|
|
||
Температура, |
Цвета побежалости |
Температура, |
Цвета побежалости |
||
°С |
°С |
12Х18Н10Т |
ХН756БТЮ |
||
|
|||||
220 |
светло-желтый |
300 |
светло- |
– |
|
соломенный |
|||||
|
|
|
|
||
240 |
темно-желтый |
400 |
соломенный |
светло- |
|
желтый |
|||||
|
|
|
|
||
265 |
красно-коричневый |
500 |
красновато- |
желтый |
|
коричневый |
|||||
|
|
|
|
||
275 |
пурпурно-красный |
600 |
фиолетово- |
коричневый |
|
синий |
|||||
|
|
|
|
||
285 |
фиолетовый |
700 |
– |
синий |
|
295 |
васильково-синий |
800 |
– |
голубой |
|
315 |
светло-синий |
– |
– |
– |
|
330-350 |
серый |
– |
– |
– |
|
Цвета побежалости [14] – это не коррозионное, а оптическое явление, они появляются в результате интерференции лучей света, отраженных от поверхности металла (рис. 1.8).
43

Рис. 1.8. Возникновение цветов побежалости
Погасание происходит, если лучи смещены один относительно другого на нечетное число полуволн. Смещение определяется разницей в длине путей лучей, отраженных от поверхности пленки и металла.
Если коэффициент преломления света в пленке принять равным коэффициенту преломления в воздухе, то условия погасания луча с длиной волны будут выполняться при
1 , 3 , 5 и т.д. 4 4 4
По мере роста пленки затухают лучи света с наиболее короткой длиной волны, т.е. голубые, и отраженный свет, лишенный голубых лучей, кажется желтым или желто-коричневым. При дальнейшем увеличении толщины пленки затухают лучи с большей длиной вол-
ны, т.е. зеленые, и кажется, что поверхность металла красного цвета.
Затем интерферируют желтые лучи, и поверхность окрашивается в голубые и синие цвета.
При увеличении толщины пленки последовательность цветов снова повторяется. В толстой пленке цвета побежалости исчезают, так как происходит поглощение света вследствие малой прозрачности пленки.
Таким образом, по изменению цвета поверхности металла, по-
крытого пленкой, и последовательности повторения цветов, вызван-
ного увеличением толщины оксидной пленки и интерференцией лу-
чей света с различной длиной волны, можно определить толщину пленки [14].
44

Если пленки затрудняют проникновение реагентов к поверхности металла, они обладают защитными свойствами.
Возможность образования пленки, покрывающей сплошным сло-
ем всю поверхность металла, определяется условием сплошности Пиллинга и Бедворса [1, 4]: молекулярный объем соединения, возни-
кающего из металла и окислителя Vок , должен быть больше объема металла VМе , израсходованного на образование молекулы соединения.
В противном случае образующегося соединения не хватает, чтобы покрыть сплошным слоем всю поверхность металла, в результате че-
го пленка продукта коррозии металла получается рыхлой, пористой.
Таким образом, если Vок <1 – пленка не может быть сплошной,
Vме
если Vок >1 – пленка может быть сплошной. Данные по отношениям
Vме
Vок для ряда металлов приведены в табл. 1.2.
Vме
Отношение объемов соединения металла с окислителем и металла можно рассчитать по формуле
Vок |
|
Mок Ме |
, |
(1.10) |
|
|
|||
VМе |
m ок AМе |
|
||
где Mок – молекулярная масса соединения;
AМе – атомная масса металла;
ок – плотность соединения;
Ме – плотность металла;
m – число атомов металла в молекуле соединения.
Однако в реальных условиях в толстых пленках могут возникать такие внутренние напряжения, которые разрушают ее частично или полностью, нарушая сплошность. Таким образом, ориентировочно можно считать, что защитные свойства будут наблюдаться в следующих пределах [1, 4]:
45

2,5 |
Vок |
1. |
(1.11) |
|
VМе
Таблица 1.2
Отношение объемов оксида и металла
Металл |
Оксид |
Vок VMe |
|
Li |
Li2O |
0,57 |
|
|
|
|
|
K |
K2O |
0,48 |
|
|
|
|
|
Mg |
MgO |
0,79 |
|
|
|
|
|
Ca |
CaO |
0,63 |
|
|
|
|
|
Sr |
SrO |
0,66 |
|
|
|
|
|
Cu |
Cu2O |
1,67 |
|
|
|
||
CuO |
1,74 |
||
|
|||
|
|
|
|
Ag |
Ag2O |
1,58 |
|
|
|
|
|
Be |
BeO |
1,67 |
|
|
|
|
|
Zn |
ZnO |
1,58 |
|
Cd |
CdO |
1,27 |
|
|
|
|
|
U |
UO2 |
1,96 |
|
|
|
||
U3O8 |
3,12 |
||
|
|||
|
|
|
|
Al |
Al2O3 |
1,31 |
|
|
|
|
|
Ti |
TiO2 |
1,76 |
|
|
|
|
|
Zr |
ZrO2 |
1,60 |
|
|
|
|
|
Sn |
SnO2 |
1,33 |
|
|
|
|
Металл |
Оксид |
Vок VMe |
|
Pb |
PbO |
1,15 |
|
|
|
|
|
Nb |
NbO |
1,57 |
|
|
|
||
Nb2O5 |
2,81 |
||
|
|||
|
|
|
|
Ta |
Ta2O5 |
2,32 |
|
|
|
|
|
Cr |
Cr2O3 |
2,02 |
|
|
|
|
|
Mo |
MoO2 |
2,18 |
|
|
|
||
MoO3 |
3,45 |
||
|
|||
|
|
|
|
W |
WO2 |
1,86 |
|
|
|
||
WO3 |
3,36 |
||
|
|||
|
|
|
|
|
FeO |
1,77 |
|
Fe |
Fe3O4 |
2,09 |
|
|
|
|
|
|
Fe2O3 |
2,14 |
|
|
|
|
|
|
CoO |
1,75 |
|
Co |
|
|
|
Co3O4 |
2,00 |
||
|
|
|
|
|
Co2O3 |
2,42 |
|
|
|
|
|
Ni |
NiO |
1,52 |
|
|
|
|
|
Pt |
PtO |
1,56 |
|
|
|
|
Уравнение (1.11) не может обеспечивать защитные свойства пленки, существуют дополнительные условия, такие как хорошая адгезия к металлу и физико-химические свойства. Поверхность пленки должна быть прочной, эластичной и иметь с основным металлом близкие значения коэффициентов термического расширения (рис. 1.9
и 1.10).
46
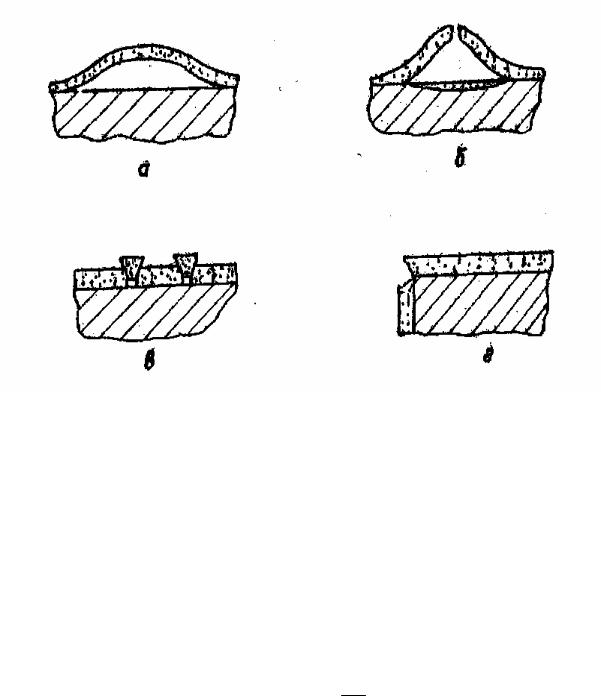
Рис.1.9. Некоторые типы разрушений оксидных пленок при их росте на металлах:
а – прочность пленки велика, адгезия к металлу мала;
б– прочность пленки и адгезия к металлу малы;
в– прочность пленки мала, адгезия к металлу велика;
г– растрескивание на углах и кругах изгибов
Взащитных пленках на металлах по разным причинам могут возникать следующие напряжения (см. рис. 1.10) [1]:
– внутренние сжимающие напряжения (рис. 1.10, а), возникаю-
щие при росте оксидной пленки, когда Vок >1;
Vме
–внутренние напряжения сжатия на неровной поверхности металла, образующие отрывающие усилия (рис. 1.10, б);
–внутренние напряжения, возникающие при изменении температуры за счет разных коэффициентов линейного и объемного расширения металла и оксидной пленки;
–механические напряжения, формирующиеся при работе изделия
вконструкции и ухудшающие сохранность защитных пленок на металле.
47
а б
Рис. 1.10. Напряжения в защитных пленках
Скорость газовой коррозии наиболее часто выражают через ско-
рость роста оксидной пленки, т.е. [1, 4, 5]
v |
dh |
, |
(1.12) |
|
|||
|
d |
|
|
где v – скорость процесса;
h– толщина оксидной пленки;
– время процесса.
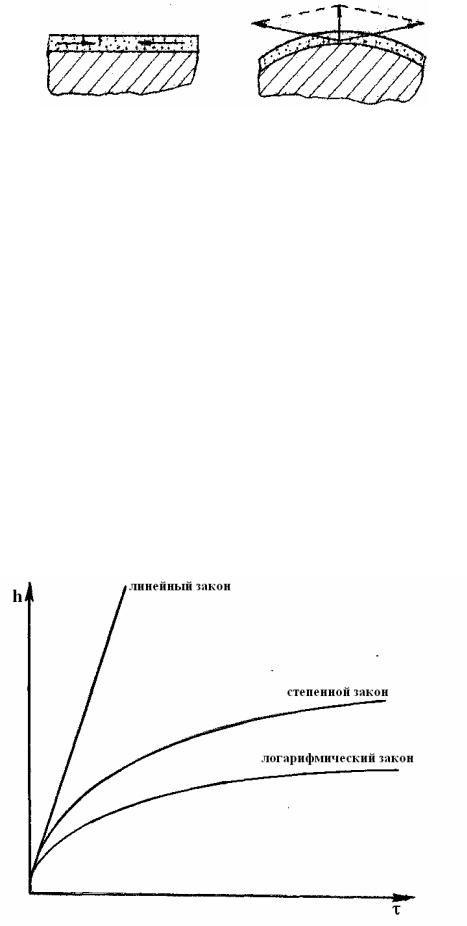
Существует несколько законов роста пленки во времени [1]: ли-
нейный, степенной, логарифмический и др. (рис. 1.11).
Рис. 1.11. Графическая интерпретация законов роста пленок
48
