Лекции по ФХ 1 семестр / Лекция 7
.docxЗАВИСИМОСТЬ КОНСТАНТ РАВНОВЕСИЯ ОТ ДАВЛЕНИЯ.
УРАВНЕНИЯ ПЛАНКА
Константа равновесия KN зависит от давления
KN=f(P);
KP= KN *P∆n; KN= KP* P-∆n
Прологарифмируем это уравнение:
lnKN= lnKP-∆n*lnP
Далее продифференцируем его по давлению, учитывая, что Кр не зависит от давления и является лишь функцией температуры:
 ,
где
,
где
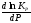 =0,
Кр≠f(P)
=0,
Кр≠f(P)
Уравнение Планка:
 ,
,
где ∆n=c+d-a-b
aA + bB = cC + dD – в газовой фазе.
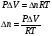
Уравнение Планка:

АНАЛИЗ УРАВНЕНИЯ ПЛАНКА
-
Если изменение объема ∆n(∆V)˃0, то
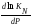 ˂0,
при увеличении давлении константа
равновесии KN
уменьшается
(P↑,
KN↓
), равновесие реакции смещается в
обратную сторону (влево).
˂0,
при увеличении давлении константа
равновесии KN
уменьшается
(P↑,
KN↓
), равновесие реакции смещается в
обратную сторону (влево). -
Если изменение объема ∆n(∆V)˂0, то
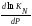 ˃0,
при увеличении давлении константа
равновесии KN
увеличивается
(P↑,
KN↑
), равновесие реакции смещается в сторону
продуктов реакции (вправо).
˃0,
при увеличении давлении константа
равновесии KN
увеличивается
(P↑,
KN↑
), равновесие реакции смещается в сторону
продуктов реакции (вправо). -
Если изменение объема равна нулю ∆n(∆V)=0, то изменение давления не влияет на направление реакции,
 =0,
Kp
≠
f(P).
=0,
Kp
≠
f(P).
Пример: N2(г)+3H2(г)=2NH3(г)
∆n=2-1-3=-2;
∆n˂0,
значит
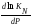 ˃0,
т.е. с ростом давления растет константа
равновесия KN,
реакция идет в прямом направлении.
˃0,
т.е. с ростом давления растет константа
равновесия KN,
реакция идет в прямом направлении.
УРАВНЕНИЕ ИЗОБАРЫ-ИЗОХОРЫ ВАНТ-ГОФФА И УРАВНЕНИЕ ПЛАНКА КАК КОЛИЧЕСТВЕННОЕ ВЫРАЖЕНИЕ ПРИНЦИПА ЛЕ ШАТЕЛЬЕ
Уравнение Планка и изобары-изохоры позволяют количественно рассчитать Кр, Кс и KN. По величине этих констант судить о направлении смещения равновесия реакции при изменении температуры и давления, а также о составе равновесных смесей.
В общей формуле достаточно быстро направление сдвига равновесия при изменении внешних условий определяется с помощью принципа Ле Шателье - Брауна, который гласит:
Если на систему, находящуюся в устойчивом равновесии, подействовать извне, изменяя какое-либо из условий равновесия, то равновесие сместиться в том направление, которое ослабляет данное воздействие.
Рассмотрим пример: N2(г)+3H2(г)↔2NH3(г) (∆H˂0)-экзотермическая.
-
Влияние температуры (Т).
Увеличиваем температуру: реакция экзотермическая, идет с выделение теплоты. При повышении температуры система будет стремиться уменьшить температуру, т.е. равновесие сместится в тк сторону, где тепло будет поглощаться (в обратную сторону для примера).
Влияние температуры на смещение равновесия можно иллюстрировать при помощи графика:
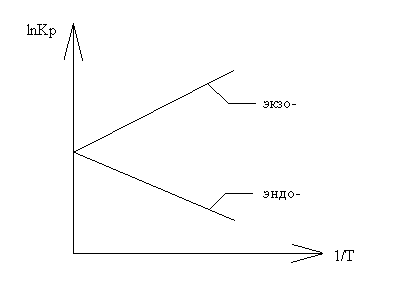
Величина
 ˂0
для экзотермических процессов.
Отрицательное значение означает, что
˂0
для экзотермических процессов.
Отрицательное значение означает, что
 и сама константа равновесия уменьшается
при увеличении температуры. Поэтому
равновесие реакции сдвигается в сторону
образования исходных веществ.
и сама константа равновесия уменьшается
при увеличении температуры. Поэтому
равновесие реакции сдвигается в сторону
образования исходных веществ.
Величина
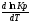 ˃0
для эндотермических процессов.
Положительное значение означает, что
˃0
для эндотермических процессов.
Положительное значение означает, что
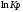 и сама константа равновесия увеличивается
при повышении температуры, и равновесие
смещается в сторону продуктов реакции.
и сама константа равновесия увеличивается
при повышении температуры, и равновесие
смещается в сторону продуктов реакции.
Итак, повышение температуры экзотермических реакций способствует увеличению количества исходных веществ, а рост температуры эндотермических реакций приводит к обогащению продуктами реакции.
-
Влияние давления (Р).
Увеличиваем давления: равновесие реакции будет смещаться в прямом направлении, т.к. из 4х молекул образуется 2 молекулы аммиака.
В общем случае при повышении давления равновесие смещается в сторону меньшего числа молей.
Когда число молей исходных веществ равно числу молей продуктов реакции, т.е. ∆n=0, то смещения равновесия при увеличении давления не произойдет.
-
Влияние концентраций.
Увеличиваем концентрацию N2, т.е. добавляем его в смесь. Система будет стремиться избрать азот, т.е. равновесие реакции сместится в прямом направлении.
В общем случае увеличение концентрации приводит к смещению равновесия в сторону увеличения расхода тех компонентов, концентрация которых увеличивается.
ХИМИЧЕСКОЕ РАВНОВЕСИЕ В ГЕТЕРОГЕННЫХ СИСТЕМАХ
Гетерогенными называют реакции, в которых реагирующие вещества и продукты находятся в разных фазах.
Fe2O3(кр)+3H2(г)=2Fe(кр)+3H2O(г)
Если какое-либо вещество, участвующее в реакции, находится в жидкой или твердой фазе, то его парциальное давление будет величиной постоянной и неизменной в ходе всего процесса.
Для данной реакци константа равновесия через парциальное давление запишется в виде:
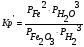
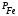 (чистое
железо)=const
(чистое
железо)=const
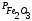 =const
=const
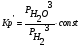 ̷const
̷const
 -
-
В выражение Кр –концентрация и парциальное давление жидких и твёрдых веществ не входит.
Возможны случаи, когда только один реагент находится в газовой фазе, например:
СаСО3(тв) = СаО (тв)+СО2(г)
Тогда
константа равновесия этой реакции
запишется:
 -
равновесное давление данного вещества
(СаСО3).
-
равновесное давление данного вещества
(СаСО3).
В этом случае равновесное давление одного из продуктов реакции есть величина постоянная при данной температуре, и является константой равновесия.
Равновесное
давление
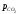 называют
давлением диссоциации.
называют
давлением диссоциации.
Тогда уравнение изобары Вант- Гоффа для этой реакции запишется в виде: