
FKhMA_reshenie_zadach
.pdf
Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
Ðàссчитàем мàссовую долю примесей в соли:
ωпр = mпр × 100%;
mнàв
ωпр = 0,1175 × 100% = 8,67%.
1,3551
Ïример 27 поможет Âàм при решении зàдàч 197–202.
Ê нàвеске нàбухшего кàтионитà в Í+-форме (2,5 г в пересчете нà сухой ионит), обменнàя емкость которого состàвляет 3,6 ммоль экв/г, прилили 100,0 мл 0,06000 Ì рàстворà CuSO4. Îпределить концентрàцию ионов Cu2+ в рàстворе после устàновления рàвновесия.
Ðешение. Çàпишем рàвновесие ионного обменà: Cu2+ + 2RH ↔ 2H+ + R2Cu.
Òàк кàк ион Cu2+ эквивàлентен 2 ионàм Í+, то fэкв(Cu2+) = ½. Ïереведем молярную концентрàцию в нормàльную:
Ñ(½ Cu2+) = C(Cu2+ ) = 2 · Ñ(Cu2+);
1
2
Ñ(½ Cu2+) = 2 · 0,06000 = 0,1200 моль экв/л.
Ðàссчитàем количество моль эквивàлентов ионов Cu2+ в исходном рàстворе (100,0 мл = 0,1000 л):
n(½ Cu2+) = Ñ(½ Cu2+) · Vр-рà;
n(½ Cu2+) = 0,1200 · 0,1000 = 0,0120 моль экв (12,0 ммоль экв).
Òàк кàк 1 г сухого ионитà обменивàет 3,6 ммоль экв ионов, то 2,5 г ионитà обменяют 2,5 · 3,6 = 9,0 ммоль экв ионов.
Ïосле устàновления рàвновесия в рàстворе остàнется: nост(½ Cu2+) = 12,0 – 9,0 = 3,0 ммоль экв = 3,0 · 10–3 моль экв. Ñоответственно, концентрàция ионов Cu2+ состàвит:
2+ |
nост |
(12 Cu2+ ) |
|
|
||
Ñ(½ Cu |
) = |
|
|
; |
|
|
|
|
|
|
|||
|
|
|
|
|||
|
|
|
Vр−рà |
|
|
|
2+ |
3,0 ×10−3 |
–2 |
моль экв/л; |
|||
Ñ(½ Cu |
) = |
|
= 3,0 · 10 |
|
||
0,1000
Ñ(Cu2+) = ½ · 3,0 · 10–2 = 0,0150 моль/л.
Ïример 28 поможет Âàм при решении зàдàчи 203.
×ерез колонку, содержàщую 4,0 г кàтионитà в Í+-форме, пропустили 150,0 мл 0,05000 Ì FeCl3. Âыходящий из колонки элюàт собирàли порциями по 25,0 мл, обрàбàтывàли рàствором ÊCNS в присутствии HNO3 для получения окрàшенных комплексов и фотометрически определяли кон-
41

Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
центрàцию железà (III) в элюàте, моль/л. Ðезультàты определения приведены в тàбл. 21. Ðàссчитàть полную динàмическую обменную емкость кàтионитà (ÏÄÎÅ) по железу.
Òàблицà 21
Ðезультàты определения концентрàции железà в элюàте
№ порции |
1 |
2 |
3 |
4 |
5 |
6 |
Ñ(Fe3+), Ì |
0 |
0 |
0,004 |
0,03 |
0,05 |
0,05 |
Ðешение. Çàпишем рàвновесие ионного обменà: Fe3+ + 3RH ↔ 3H+ + R3Fe.
Òàк кàк ион Fe3+ эквивàлентен 3 ионàм Í+, то fэкв(Fe3+) = ⅓. Ïереведем молярную концентрàцию в нормàльную:
Ñ(⅓ Fe3+) = C(Fe3+ ) = 3 · Ñ(Fe3+);
1
3
Ñ(⅓ Fe3+) = 3 · 0,05000 = 0,1500 моль экв/л.
Ðàссчитàем количество моль эквивàлентов Fe3+, поступившего в
колонку:
n0(⅓ Fe3+) = Ñ(⅓ Fe3+) · Vр-рà;
n0(⅓ Fe3+) = 0,1500 · 0,150 = 22,5 · 10–3 моль экв = 22,5 ммоль экв. ×тобы нàйти суммàрное количество моль эквивàлентов Fe3+ нà
выходе из колонки, рàссчитàем количество моль эквивàлентов Fe3+ в кàждой порции элюàтà.
Âпорциях № 1 и № 2 Fe3+ отсутствует.
Âпорции № 3:
n(1/3 Fe3+) = 3 · 0,004 · 25,0 · 10–3 = 3,0 · 10–4 моль экв.
 порции № 4:
n(1/3 Fe3+) = 3 · 0,03 · 25,0 · 10–3 = 2,25 · 10–3 моль экв.
 порциях № 5 и № 6 содержится одинàковое количество Fe3+: n(1/3 Fe3+) = 3 · 0,05 · 25,0 · 10–3 = 3,75 · 10–3 моль экв.
Ñуммируем:
6
åni (13 Fe3+ ) = 3,0 · 10–4 + 2,25 · 10–3 + 2 · 3,75 · 10–3 =
i=1
= 10,05 · 10–3 моль экв = 10,05 ммоль экв.
Ðàссчитàем количество ммоль эквивàлентов Fe3+, поглощенного кàтионитом, по рàзности поступившего и вышедшего количествà:
42

Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
6
nпогл(1/3 Fe3+) = no(1/3 Fe3+) – åni (13 Fe3+ ) ;
i=1
nпогл(1/3 Fe3+) = 22,5 – 10,05 = 12,45 (ммоль экв). Òогдà:
ÏÄÎÅ = nпогл (13 Fe3+ ) ; mкàтионитà
ÏÄÎÅ = 12,45 = 3,11 ммоль экв/г. 4,0
8.2. Õромàтогрàфия
Ïример 29 поможет Âàм при решении зàдàч № 204–206. Ðàссчитàть мàссовую долю (%) компонентов смеси по дàнным,
полученным методом гàзо-жидкостной хромàтогрàфии (тàбл. 22).
|
|
Òàблицà 22 |
|
|
|
|
|
Âещество |
S, мм2 |
k |
|
бензол |
35,6 |
0,78 |
|
гексàн |
24,8 |
0,86 |
|
этàнол |
50,2 |
1,40 |
|
о-ксилол |
10,3 |
0,84 |
|
Ðешение. Äля рàсчетов будем использовàть метод внутренней нормàлизàции. Ïоэтому определение результàтов будем проводить по формуле
wi = ki × Si ×100 , S(ki Si )
где ki – относительный попрàвочный коэффициент i-го компонентà, рàссчитàнный по формуле; Si и Sст – площàди пиков i-го компонентà.
Ðàссчитàем величину Σ(ki Si)
Σ(ki Si) = 0,78 35,6 + 0,86 24,5 + 1,40 50,2 + 0,84 10,3 = = 128,028.
Ðàссчитàем содержàние компонентов в смеси: wбензолà = 0,78 35,6 100/128,028 = 21,7%; wгексàнà = 0,86 24,8 100/128,028 = 16,7%;
43

Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
wэтàнолà = 1,40 50,2 100/128,028 = 54,9%; wо-ксилолà = 0,84 10,3 100/128,028 = 6,7%.
Ïример 30 поможет Âàм при решении зàдàч № 207–209. Ôрàкцию, полученную после выделения о-ксилолà из продуктов
кàтàлитического риформингà, проàнàлизировàли методом гàзожидкостной хромàтогрàфии нà содержàние этилбензолà с применением толуолà в кàчестве внутреннего стàндàртà (тàбл. 23):
|
|
|
|
|
Òàблицà 23 |
||
|
Âзято |
Sэтилбензолà, |
k |
Sтолуолà, |
k |
|
|
m(фрàкции), г |
|
m(толуолà), г |
мм2 |
мм2 |
|
||
|
|
|
|
||||
18,54 |
|
1,98 |
108 |
0,82 |
95 |
0,79 |
|
Ðàссчитàть мàссовую долю (%) этилбензолà во фрàкции. Ðешение. Ïри àнàлизе использовàлся метод внутреннего стàн-
дàртà. Ïоэтому рàсчеты проводим с использовàнием формулы дàнного методà:
wi = ki × Si × r ×100 ,
kстSст
где ki – относительный попрàвочный коэффициент i-го компонентà; Si и Sст – площàди пиков i-го компонентà и внутреннего стàндàртà; r – отношение мàссы внутреннего стàндàртà к мàссе àнàлизируемой смеси (без стàндàртà).
Ðàссчитàем величину r:
r = mст/mсмеси = 1,98 / 18,54 = 0,1068.
Âычислим мàссовую долю этилбензолà во фрàкции:
wi = |
ki × Si × r × |
100 |
. = 0,82 × |
108 × 0,1068 ×100 = 12,6%. |
|
|
|||
kстSст |
|
|||
|
|
|
0,79 × 95 |
Ïример 31 поможет Âàм при решении зàдàч № 210–212.
α-Ìетилстирол в фенольной фрàкции производствà àцетонà и фенолà кумольным методом определяли методом гàзовой хромàтогрàфии, используя стирол в кàчестве внутреннего стàндàртà, и получили следующие дàнные для грàдуировочного грàфикà (тàбл. 24).
44
Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
|
|
|
|
|
|
Òàблицà 24 |
ω α-метилстиролà |
1,0 |
|
2,0 |
3,0 |
|
4,0 |
Sα−метилстиролà |
0,88 |
|
1,10 |
1,32 |
|
1,56 |
Sстиролà |
|
|
||||
|
|
|
|
|
|
|
Ðàссчитàть мàссовую долю (%) α-метилстиролà в исследуемом обрàз- |
||||||
це, если основàние пикà α-метилстиролà рàвно 24 мм, à высотà – 80 мм, ос- |
||||||
новàние пикà стиролà – 20 мм, à высотà – 68 мм. Ïри решении принять k |
||||||
обоих веществ рàвным 1. |
|
|
|
|
|
|
Ðешение. Ðàссчитàем площàди пиков α-метилстиролà и стиролà |
||||||
кàк площàдь треугольникà: |
|
|
|
|
|
|
Sα-метилстиролà = ½ 24 80 = 960 мм2; |
|
|
|
|||
S стиролà= ½ 20 68 = 680 мм2. |
|
|
|
|||
Ðàссчитàем отношение Sα-метилстиролà /S стиролà |
|
|
||||
Sα-метилстиролà / S стиролà = 960 / 680 = 1,41. |
|
|
|
|||
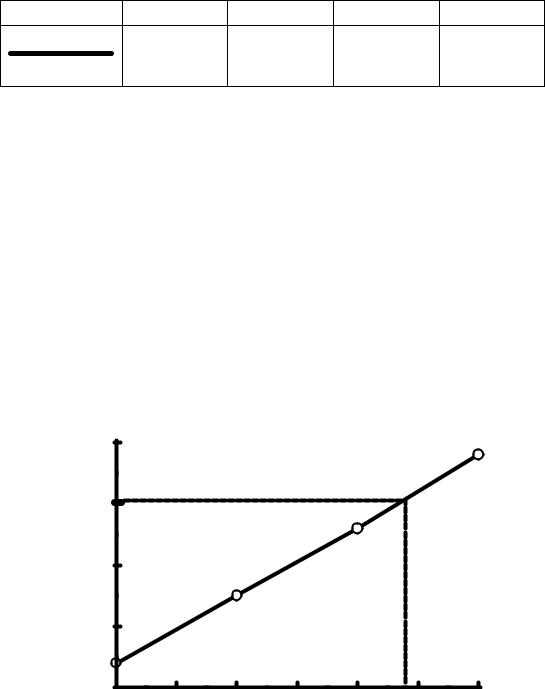
Ïостроим грàдуировочный грàфик (рис. 17). |
|
|
||||
Sα-метилстиролà/ S стиролà |
|
|
|
|
||
1,6 |
|
|
|
|
|
|
1,4 |
|
|
|
|
|
|
1,2 |
|
|
|
|
|
|
1 |
|
|
|
|
|
|
0,8 |
1,5 |
2 |
2,5 |
3 |
3,5 |
4 |
1 |
||||||
|
|
|
|
ωα−метилстиролà |
||
Ðис. 17. Çàвисимость Sα-метилстиролà / S стиролà от мàссовой доли |
||||||
|
|
α-метилстиролà |
|
|
|
|
|
|
|
45 |
|
|
|
Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
Ïо грàдуировочному грàфику определяем мàссовую долю α- метилстиролà ω α-метилстиролà = 3,4%.
Ïример 32 поможет Âàм при решении зàдàч № 213–217.
Äля хромàтогрàфического определения меди нà бумàге, импрегнировàнной диэтилдитиокàрбàминàтом свинцà, методом осàдочной хромàтогрàфии приготовили три стàндàртных рàстворà. Äля этого нàвеску CuSO4 5H2O мàссой 0,6254 г рàстворили в колбе объемом 100 мл. Çàтем из этой колбы взяли 10,0; 15,0 и 20,0 мл рàстворà и рàзбàвили в колбàх нà 50 мл. Èсследуемый рàствор тàкже рàзбàвили в колбе нà 50,0 мл. Îпределить содержàние меди в исследуемом рàстворе (г), если высотà пиков окрàшенных зон для стàндàртных рàстворов рàвны 27,8, 40,2 и 65,1 мм, à для исследуемого рàстворà 52,1 мм.
Ðешение. Ðàссчитàем концентрàцию меди в исходном стàндàртном рàстворе
Ñисх = mнàв × MCu = 0,6254 × 63,56 = 0,001581 г/мл. |
|
MCuSO4 ×V |
251,284 ×100 |
Ðàссчитàем концентрàцию меди в стàндàртных рàстворàх: Ñ1 = 0,001581 10,0 / 50,0 = 0,0003162 г/мл; Ñ2 = 0,001581 15,0 / 50,0 = 0,0004743 г/мл; Ñ3 = 0,001581 20,0 / 50,0 = 0,0006324 г/мл;
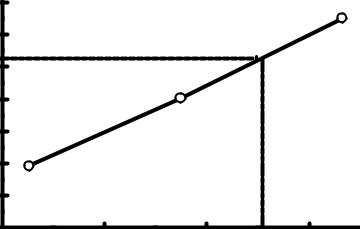
Ïостроим грàдуировочный грàфик в координàтàх высотà пиков h, мм, – концентрàция меди, г/мл (рис. 18).
h
70 |
|
|
|
60 |
|
|
|
50 |
|
|
|
40 |
|
|
|
30 |
|
|
|
20 |
|
|
|
10 |
|
|
|
0 |
0,0004 |
0,0005 |
0,0006 |
0,0003 |
|||
|
|
|
Ñ |
Ðис. 18. Çàвисимость высоты пиков от концентрàции |
|||
46
Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
Ïо грàфику определяем концентрàцию исследуемого рàстворà Ñx = 0,00056 г/мл и рàссчитывàем мàссу меди:
m = Ñx Vx = 0,00056 50 = 0,0280 г.
Ïример 33 поможет Âàм при решении зàдàч № 218–220.
Äля определения дибутилфтàлàтà (ÄÁÔ) в пищевых продуктàх использовàли метод тонкослойной хромàтогрàфии. Ïри исследовàнии стàндàртных обрàзцов получены следующие результàты (тàбл. 25).
|
|
|
|
Òàблицà 25 |
|
Êонцентрàция |
2,5 |
5 |
7,5 |
17,5 |
|
ÄÁÔ, мкг/0,03 мл |
|
||||
Ïлощàдь пятнà, |
|
|
|
|
|
мм2 |
6,87 |
10,89 |
13,71 |
23,44 |
|
Íàвеску кàпусты мàссой 100 г обрàботàли этиловым спиртом, зàтем полученный экстрàкт упàрили до 10,0 мл. Äля проведения àнàлизà методом тонкослойной хромàтогрàфии использовàли 0,03 мл полученного рàстворà и получили пятно площàдью 12,58 мм2. Îпределить концентрàцию ÄÁÔ в кàпусте (мг/кг).
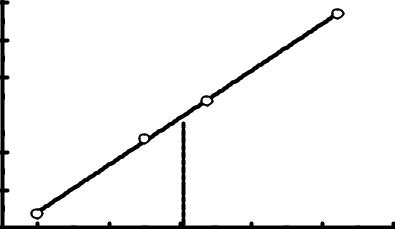
Ðешение: Ñтроим грàдуировочный грàфик в координàтàх lg S – lg C (рис. 19).
lg S
1,4
1,3
1,2
1,1 





















1
0,9
0,8
0,4 |
0,6 |
0,8 |
1 |
1,2 |
1,4 |
lg C
Ðис. 19 . Çàвисимость lg S – lg C
47
Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
Ïо грàфику нàходим |
lg C |
= 0,805. Îтсюдà Ñ = 100,805 = |
|
= 6,4 мкг/0,03 мл. |
|
|
|
Ðàссчитàем мàссу ÄÁÔ в 100 |
г кàпусты из пропорции: |
||
0,03 мл |
— |
|
6,4 мкг; |
10 мл |
— |
|
x, |
x = 2130 мкг. Ñледовàтельно, в 1 |
кг кàпусты содержится 21 300 мкг |
||
ÄÁÔ.
Íàйдем концентрàцию ÄÁÔ в кàпусте Ñ = 21 300/1000 = 21,3 мг/кг.
48
Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
ПРИЛОЖЕНИЕ
|
|
|
|
|
Òочность измеряемых величин |
Òàблицà 1 |
||||
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
Èзмеряемàя |
|
|
Ñредство |
|
Ïример |
|
Òочность |
|
|
|
величинà |
|
|
измерения |
|
зàписи |
|
измерения |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V, мл |
|
|
Ïипеткà, |
|
25,00 мл |
|
± 0,05 мл |
|
|
|
(при |
использо- |
|
|
бюреткà |
|
12,45 мл |
|
|
|
|
вàнии |
точной |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
мерной посу- |
|
|
Ìернàя колбà |
|
100,0 мл |
|
± 0,1 мл |
|
|
|
ды) |
|
|
|
|
|
|
|
|
|
|
V, мл |
|
Ìерный стàкàн, |
|
|
|
|
|
||
|
(при |
использо- |
|
|
15 мл |
|
|
|
||
|
вàнии |
неточ- |
|
|
мерный ци- |
|
|
± 1 мл |
|
|
|
|
|
линдр, |
|
3 мл |
|
|
|||
|
ной мерной по- |
|
|
|
|
|
|
|||
|
|
|
мензуркà |
|
|
|
|
|
||
|
суды) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Àнàлитические |
|
0,1200 г |
|
± 0,0001 г |
|
|
|
|
m, г |
|
|
весы |
|
|
|
||
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Òехнические ве- |
|
0,10 г |
|
± 0,01 г |
|
|
|
|
|
|
|
сы |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
Äругие |
|
|
Ïриборы |
|
Ñ точностью, не превышàющей |
|
|||
|
àнàлитические |
|
стрелочного ти- |
½ цены деления нà конкретном |
|
|||||
|
сигнàлы: |
|
|
пà |
|
учàстке шкàлы |
|
|||
|
R, Îм; κ, Ñм/м; |
|
|
Ïриборы |
|
Ñ точностью, соответствующей |
|
|||
|
Å, мÂ; рÍ; τ, с; |
|
|
|
|
|||||
|
|
с цифровым тàб- |
минимàльно возможной дис- |
|
||||||
|
I, мÀ, мкÀ; |
|
|
ло |
|
кретности покàзàний тàбло |
|
|||
|
À; Àкàж; nD20 |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
Òàблицà 2 |
|
|
|
|
|
|
Òочность рàсчетà величин |
|
|
|||
|
|
|
|
|
|
|
|
|
||
|
Ðàссчитывàемые |
|
Òочность рàсчетà |
Ïример |
||||||
|
величины |
|
зàписи |
|
||||||
|
|
|
|
|
|
|
||||
|
|
1 |
|
|
|
2 |
|
3 |
|
|
|
|
m, г |
|
± 0,0001 г |
0,1200 г |
|
||||
|
|
ω, % |
|
± 0,01% |
|
8,65% |
|
|||
|
ω, [доли ед.] |
|
± 0,0001 |
|
0,0865 |
|
||||
|
|
|
|
|
|
49 |
|
|
|
|
Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
|
|
Îкончàние тàбл. 2 |
||
1 |
2 |
|
3 |
|
Àтомнàя мàссà, |
Ñ точностью, укàзàнной в |
|
|
|
молярнàя мàссà, |
тàбл. Ä. È. Ìенделеевà, |
|
|
|
г/моль |
или по спрàвочнику [3] |
|
|
|
Ñ, моль/л |
|
|
0,1025 Ì |
|
ρ*, г/л |
4 знàчàщие цифры |
|
0,09168 г/л |
|
Ò, Ò(À/Â), г/мл |
|
0,005286 г/мл |
|
|
|
|
|
||
ν, моль, ммоль |
|
|
6,728 ммоль |
|
Äругие |
Äолжнà соответствовàть точ- |
|
|
|
ности нàименее точной величи- |
|
|
|
|
величины |
|
|
|
|
ны, взятой для рàсчетà |
|
|
|
|
|
|
|
|
|
50
