
- •Пояснительная записка Курсового проекта
- •Реферат
- •Введение
- •1 Обоснование и описание технологической схемы
- •2 Литературный обзор
- •2.1 Теоретические основы ректификации
- •2.1.1.Материальный баланс
- •Поскольку:
- •Отсюда следует, что
- •Делая подстановку в уравнение, получим
- •2.2. Основные технологические схемы.
- •2.2.1. Непрерывно действующие установки
- •2.2.2. Периодически действующие установки
- •2.2.3 Ректификация многокомпонентных смесей
- •2.2.4.Специальные виды ректификации.
- •2.3 Типовое оборудование для проектируемой установки
- •2.3.1.Барботажные колонны
- •2.3.2. Насадочные колонны.
- •2.3.3.Теплообменники.
- •2.3.4. Насосы.
- •2.3.4.1.Поршневой насос.
- •3 Расчёт ректификационной колонны
- •3.1 Материальный баланс колонны и рабочее флегмовое число
- •3.2 Скорость пара и диаметр колонны
- •3.3 Высота колонны.
- •3.4. Гидравлическое сопротивление тарелок колонны.
- •Для верхней части колонны:
- •Для нижней части колонны:
- •3.5 Тепловой расчет колонны
- •4 Подбор вспомогательного оборудования
- •4.3 Подбор дефлегматора
- •4.4 Подбор насоса для подачи исходной смеси в колонну
3 Расчёт ректификационной колонны
3.1 Материальный баланс колонны и рабочее флегмовое число
Производительность колонны по дистилляту GD и кубовому остатку GW определим из уравнений материал ьного баланса колонны [2]:
 (3.1)
(3.1)
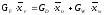 (3.2)
(3.2)
где:
GF,
GD,
GW
– массовые расходы исходной смеси,
дистиллята и кубового остатка
соответственно, кг/с;
 – мольные доли легколетучего компонента
в исходной смеси, дистиллята и кубового
остатка соответственно кмоль/кмоль.
– мольные доли легколетучего компонента
в исходной смеси, дистиллята и кубового
остатка соответственно кмоль/кмоль.
Переведем мольные доли, данные в задании, в массовые [3].
 , (3.3)
, (3.3)
где
 – массовая доля легколетучего компонента
в смеси, кг / кг; х – молярная доля
легколетучего компонента в смеси,
кмоль/кмоль; МА
и ММ
– молярные массы ацетона (легколетучего)
и метанола (труднолетучего) компонентов,
кг / кмоль.
– массовая доля легколетучего компонента
в смеси, кг / кг; х – молярная доля
легколетучего компонента в смеси,
кмоль/кмоль; МА
и ММ
– молярные массы ацетона (легколетучего)
и метанола (труднолетучего) компонентов,
кг / кмоль.
Температура кипения ацетона равна 56,1°С, а метанола – 64,7°С, следовательно, легколетучий компонент ацетон. [4].
Следовательно, МА = 58 кг / кмоль и ММ = 32 кг / кмоль – молярные массы ацетона (легколетучего компонента) и метанола (труднолетучего компонента) соответственно; xF = 0,28 кмоль/кмоль; xw = 0,02кмоль/кмоль; xD = 0,8 кмоль/кмоль.
 кмоль
/ кмоль смеси;
кмоль
/ кмоль смеси;
 кмоль
/ кмоль смеси;
кмоль
/ кмоль смеси;
 кмоль
/ кмоль смеси.
кмоль
/ кмоль смеси.
Решая совместно выражения 3.1 и 3.2 находим расходы дистиллята и кубового остатка, предварительно переведя расход исходной смеси в кг / с.
GD = 9500 / 3600 = 2,64 кг / с.

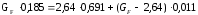
Решив
уравнение найдем;
 =10,3
кг/с ►GW=10,3-2,64=7,66
кг∕с
=10,3
кг/с ►GW=10,3-2,64=7,66
кг∕с
Нагрузки ректификационной колонны по пару и жидкости определяются рабочим флегмовым числом R, его оптимальное значение Rопт можно найти путем технико-экономического расчета. Так как отсутствуют надежные методики оценки Rопт используют приближенные вычисления, основанные на определении коэффициента избытка флегмы (орошения) β, рассчитываемый по формуле: [2]:
β = R / Rmin, (3.4)
где Rmin – минимальное флегмовое число, определяемое по уравнению: [2]:
 (3.5)
(3.5)
где xF, xD, – молярные доли легколетучего компонента в исходной смеси, и дистилляте соответственно, кмоль/кмоль смеси; yF* – концентрация легколетучего компонента в паре, находящегося в равновесии с исходной смесью, кмоль / кмоль смеси.
Для дальнейших расчетов необходимо построить диаграммы равновесия между паром и жидкостью при постоянном давлении в координатах у – х (рис. 3.1) и t – х - у (рис. 3.2).Чтобы их построить нужно воспользоваться данными из таблицы 1.
|
x, кмоль/кмоль |
0 |
5 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
100 |
|
y, кмоль/кмоль |
0 |
10,2 |
18,6 |
32,2 |
42,8 |
51,3 |
58,6 |
65,6 |
72,5 |
80 |
- |
100 |
|
t, °С |
64,5 |
63,6 |
62,5 |
60,2 |
58,7 |
57,6 |
56,7 |
56 |
55,3 |
55,05 |
- |
56,1 |
Таблица 1.Равновесные составы жидкости (х) и пара (у) в мол. долях (в %) и температуры кипения (t) в °С бинарной смеси метанол-этанол при давлении 760 мм. рт. ст.
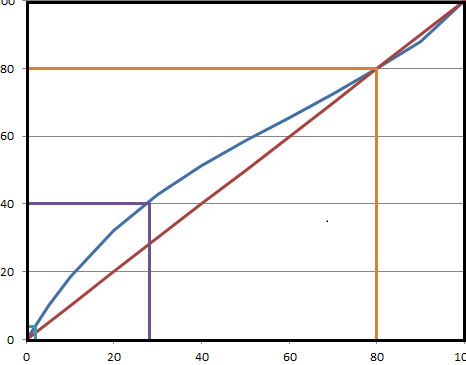
Рисунок 3.1 Диаграмма равновесия между паром и жидкостью в координатах х-у

Рисунок 3.2 Диаграмма равновесия между паром и жидкостью в координатах t-x-y
Один из способов расчета R заключается в нахождении такого флегмового числа, которому соответствует минимальное произведение N(R+1), пропорциональное объему ректификационной колонны (N – число ступеней изменения концентрации или теоретических тарелок, определяющее высоту колонны, а R + 1 расход паров и, следовательно, сечение колонны).
При расчетах процесса ректификации принимают следующие допущения:
1 Разделяемая смесь следует правилу Трутона, согласно которому отношение мольной теплоты испарения или конденсации r к абсолютной температуре кипения Т для всех жидкостей является приближенно величиной постоянной.
2 Состав пара уD, удаляющегося из колонны в дефлегматор, равен составу дистиллята хD. При этом допускается, что укрепляющим действием дефлегматора в процессе конденсации в нем паров можно пренебречь и принять уD = уD = xD, где уD − состав дистиллята в паровой фазе.
3 Состав пара уW, поднимающегося из кипятильника в колонну равен составу жидкости xW, стекающей в кипятильник из нижней части колонны. Принимая уW = xW, пренебрегают исчерпывающим действием кипятильника, т.е. изменением состава фаз при испарении в нем жидкости.
4 Теплоты смешения компонентов разделяемой смеси равны нулю [1].
Исходя из этих допущений и уравнений для рабочих линий колонны строятся рабочие линии при различных значениях коэффициента избытка флегмы. При этом для построения рабочих линий достаточно воспользоваться одним из уравнений рабочих линий (например, для верха колонны), так как рабочие линии для верхней и нижней части колонны пересекаются в точке, которая описывает состав исходной смеси (т.е. значения концентраций легколетучего компонента в жидкой и паровой фазе соответственно – xF; уF). Так как концентрация легколетучего компонента в жидкой фазе известна из задания, то остается рассчитать концентрацию легколетучего компонента в паровой фазе. Для этого подставим рассчитанные значения флегмового числа из уравнения 3.4 в уравнение рабочей линии для верха колонны. Далее из точек с координатами (xD; уD) и (xW; уW) проводим прямые, которые являются рабочими линиями для верха и низа колонны. Эти линии пересекутся в точке (xF; уF). Построение теоретических тарелок начинается из точки (xD; уD). Проводится горизонтальная линия из этой точки до пересечения с равновесной кривой. Этот отрезок показывает изменение концентрации легколетучего компонента в жидкой фазе. Далее проводится вертикальная линия из точки пересечения горизонтальной линии с равновесной кривой до пересечения с рабочей линией. Этот отрезок показывает изменение концентрации легколетучего компонента в паровой фазе. Построение таких ступенек ведется до пересечения линией отвечающей составу жидкости удаляемой из куба.
Для каждого значения R определяем количество теоретических тарелок N.
Определение рабочего флегмового числа Rоп ведется путем построения графика N(R+1) от R. Минимальное значение N(R+1) будет соответствовать рабочему флегмовому числу (рис. 3.8).
Результаты расчетов рабочего флегмового числа представлены в таблице 3.2 и на рисунках 3.3 –3.7 определение числа теоретических тарелок, соответствующих каждому значению R. Оптимальное значение флегмового числа Rоп соответствует минимальному значению произведения N(R+1).
В=xD/(R+1) (3.6)
|
Β |
1,02 |
1,2 |
1,5 |
1,8 |
2,1 |
|
R |
3,39 |
3,99 |
4,99 |
5,99 |
6,99 |
|
В |
0,1822 |
0,1603 |
0,1335 |
0,1144 |
0,1001 |
|
N |
31 |
21 |
20 |
16 |
17 |
|
N(R + 1) |
136,09 |
104,79 |
119,82 |
111,84 |
135,83 |
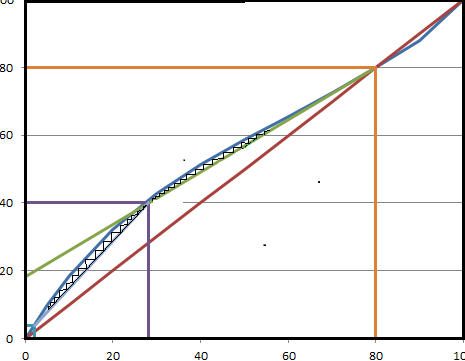
Рисунок 3.3 Флегмовое число R=1,02

Рисунок 3.4 Флегмовое число R=1,2

Рисунок 3.5 Флегмовое число R=1,5

Рисунок 3.6 Флегмовое число R=1,8

Рисунок 3.7 Флегмовое число R=2,1

Рисунок 3.8 Определение оптимального флегмового числа
Согласно построенному графику N(R+1) от R минимальное значение N(R+1) соответствует Rопт = 4,15.

Рисунок 3.9 R=4,15
Уравнение рабочих линий
1 Верхней части колонны:

2 Нижней части колонны:

Средние массовые расходы по жидкости для верхней и нижней частей колонны определяются по уравнениям [2]:
Lв = GD*R*Mв / MD (3.7)
Lн = GD*R*Mн / MD + GF*Mн / MF, (3.8)
где MD и MF – молярные массы дистиллята и исходной смеси, кг / кмоль; Mв и Mн – средние молярные массы жидкости в верхней и нижней частях колонны, кг/кмоль.
Средние молярные массы жидкости в верхней и нижней частях колонны соответственно равны [2]:
Mв = MА*хср.в + MМ*(1 – хср.в) (3.9)
Mн = MА*хср.н + MМ*(1 – хср.н), (3.10)
где MА, MМ – молярные массы ацетона и метанола соответственно, кг / кмоль; хср.в, хср.н – средний молярный состав жидкости в верхней и нижней частях колонны соответственно кмоль / кмоль смеси.
хср.в = (xD + xF) / 2 = (0,8 + 0,28) / 2 = 0,54 кмоль / кмоль смеси;
хср.н = (xW + xF) / 2 = (0,02 + 0,28) / 2 = 0,15 кмоль / кмоль смеси.
Подставляем полученные значения в уравнения (3.9) и (3.10):
Mв = 58*0,54 + 32*(1 – 0,54) = 46,04 кг / кмоль;
Mн = 58*0,15 + 32*(1 – 0,15) = 35,9 кг / кмоль.
Молярная масса дистиллята:
MD = MА*хD + MМ*(1 – хD) = 58*0,8 + (1 – 0,8)*32 = 52,8 кг / кмоль; (3.11)
Молярная масса исходной смеси равна:
МF = MА*хF + MМ*(1 – хF) = 58*0,28 + 32*(1 – 0,28) = 39,28 кг / кмоль.
Тогда массовые расходы по жидкости равны:
Lв = 2,64*4,15*46,04 / 52,8 = 9,55 кг / с;
Lн = 2,64*4,15*35,9 / 52,8 + 10,3*35,9 / 39,28 = 16,86 кг / с.
Рассчитаем средние массовые потоки пара в верхней и нижней частях колонны по уравнениям [2]:
Gв = GD*(R + 1)*Мв/ / МD (3.12)
Gн = GD*(R + 1)*Мн/ / МD (3.13)
где: Мв/, Мн/ – средние молярные массы паров в верхней и нижней частях колонны, кг / кмоль.
Мв/ = MА*уср.в + MМ*(1 – уср.в) (3.14)
Мн/ = MА*уср.н + MМ*(1 – уср.н), (3.15)
где: уср.в, уср.н – средний молярный состав паров в верхней и нижней частях колонны соответственно, кмоль / кмоль смеси.


Получаем:
уср.в = 0,81*0,54+0,16=0,60 кмоль / кмоль смеси;
уср.н = 1,39*0,15-0,008=0,22кмоль / кмоль смеси.
Подставляем полученные значения в уравнения 3.14 и 3.15:
Mв/ = 58*0,60 + 32*(1 – 0,60) = 47,63 кг / кмоль;
Mн/ = 58*0,22 + 32*(1 – 0,22) = 37,72 кг / кмоль.
Тогда массовые потоки пара равны:
Gв = 2,64*(4,15 + 1)*47,6 / 52,8= 12,26 кг / с;
Gн = 2,64*(4,15 + 1)*37,72 / 52,8 = 9,7кг / с.
