- •Неорганическая химия наука о природе
- •Природные явления
- •Чистые вещества и смеси
- •Химический элемент
- •Химический символ обозначает
- •Химический состав
- •Химическая формула и расчет по формулам
- •Схемы строения атомов химических элементов побочных подгрупп
- •Периодичность изменения химических и физических свойств элементов главных подгрупп
- •Валентность
- •Составление химических формул по валентности
- •Электроотрицательность
- •Относительная электроотрицательность химических элементов
- •Степень окисления
- •Химическая связь
- •Типы кристаллических решеток
- •Взаимосвязь основных химических понятий
- •Свойства и применение кислорода
- •Классификация сложных неорганических веществ
- •Генетические связи между классами неорганических веществ
- •Классификация кислот
- •Номенклатура кислот и средних солей
- •Химические свойства сложных неорганичеких веществ
- •Примеры уравнений химических реакций
- •Химические свойства воды ()
- •Очистка воды
- •Растворы
- •Растворимость веществ
- •Количество растворенного вещества
- •Концентрации растворов
- •Химические реакции классификация химических реакций
- •Окислительно-восстановительные реакции
- •Составление уравнений окислительно-восстановительных реакций методом электронного баланса
- •Форма записи о.В.Р.
- •Гидролиз солей количественные соотношения при химических реакциях
- •2. Кислоты, основания, амфотерные
- •3. Реакции ионного обмена
- •Металлы
- •1. Ме — химический элемент
- •2. Ме — простое вещество
- •3. Химические свойства металлов
- •Промышленные способы получения металлов
- •Электрохимический ряд напряжений металлов
- •Электролиз
- •Применение электролиза
- •Металлы I группы главной подгруппы (щелочные) Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Металлы II группы главной подгруппы (щелочно-земельные) Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Характер соединений оксидов ме
- •II группы главной подгруппы
- •Жесткость воды
- •Элементы III группы главной подгруппы Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Неметаллы
- •1. НеМе—химический элемент
- •2. НеМе — простое вещество
- •Углерод (с). Аллотропия углерода (с)
- •Угольная кислота
- •Соли угольной кислоты
- •Аллотропия кремния
- •Соединения кремния (si)
- •Силикатная промышленность
- •Простые вещества, образованные элементами
- •V группы главной подгруппы
- •Азот — простое вещество
- •Получение азота (n2)
- •Синтез аммиака в промышленности
- •Получение аммиака в лаборатории
- •Химические свойства
- •Оксиды азота (n)
- •Азотная кислота
- •Нитраты
- •Аллотропия форфора (р)
- •Химические свойства фосфора (р)
- •Соединения фосфора (р)
- •Фосфорная кислота
- •Элементы VI группы главной подгруппы
- •Простые вещества элементов VI группы главной подгруппы
- •Аллотропия кислорода ("о")
- •Аллотропия серы (s)
- •Соединения серы (s)
- •Кислоты серы (s)
- •Производство
- •Элементы VII группы главной подгруппы (галогены) Сравнительная характеристика химических элементов
- •Простые вещества элементов VII группы главной подгруппы
- •Химические свойства простых веществ на примере
- •Соляная кислота (hCl)
- •Химические свойства соляной кислоты
- •Медь (Cu) — представитель химических элементов побочных подгрупп
- •Железо (Fe) — представитель химических элементов побочных подгрупп
- •Железо (Fe) — простое вещество
- •Химические свойтсва () — восстановитель
- •Соединения железа в степени окисления
- •Производство чугуна
- •Производство стали
- •Способы получения стали
- •Реакции, лежащие в основе производства стали кислородно-конвертерным и мартеновским способами
- •Хром (Cr) — представитель химических элементов побочных подгрупп
- •Хром (Cr) — простое вещество
- •Химические свойства Cro
- •Соединения хрома (Cr)
Угольная кислота
|
Формула |
H
— O
слабая
C
= O H
— O
существует только в растворе |
|
Диссоциация |
В растворе — слабый электролит: 1.
2.
|
|
Химические свойства |
|
Соли угольной кислоты
|
Карбонаты Щелочных
Ме и
|
Гидрокарбонаты Щелочных,
|
|
Получение | |
|
|
|
|
Гидролиз по аниону | |
|
|
СО2↑
|
Продолжение
|
+ | |
|
|
|
|
Качественная реакция | |
|
на
|
на
НС |
недост. помутнение |
помутнение избыток раствор |
|
Применение | |
|
|
Na |
Аллотропия кремния
|
Алмазоподобная структура |
Аморфный кремний |
|
Sp3— гибридизация атома "Si" металлический блеск, полупроводник, химически инертен |
Белый порошок, более реакциоспособен |
Соединения кремния (si)
|
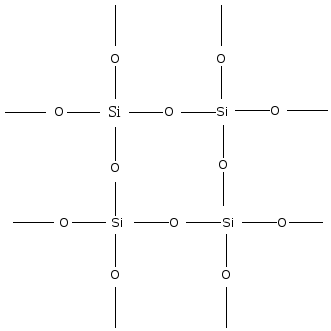
Оксид кремния |
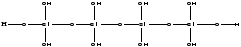
Кремниевая кислота |
Соли кремниевой кислоты |
|
Ткип.
= 2950 Тпл.
= 1713
Бесцветное кристаллическое вещество, тугоплавкое, инертное |
Поликислота —
xSi Ортокремниевая —
Студенистый осадок, очень слабая, слабее угольной кислоты
В растворе образует коллоид и слабо диссоциирует
H
2NaOH
+
|
Силикаты
жидкие стекла, растворимые в воде Силикаты других металлов (кроме щелочных) не растворяются в воде |
|
Гидролиз солей | ||
|
по аниону кислотного остатка
Сильный гидролиз:
диметосиликат | ||
|
Получение | ||
|
| ||
|
Кислотный оксид |
Получение | |
|
|
| |
|
Применение: в силикатной промышленности |
Силикатная промышленность
|
Стекло |
Цемент |
|
Твердый прозрачный элемент
Сырье:
сплавление
|
Серый порошок, при смешивании с водой затвердевает
Сырье:
Обжиг
при
Состав:
CaO,
|
|
Добавки к составу |
Применение |
+ +CaO — синий
+ +CdS — желтый и т. д. |
Цемент
+
Цемент и бетон — важные строительные материалы |
|
Особый вид стекла — кварцевое | |
|
Стеклообразная форма чистого кремнезема
|

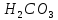
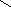
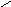
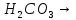 СО2↑
+
СО2↑
+
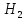 О
О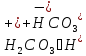 — гидрокарбонат ион
— гидрокарбонат ион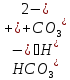 — карбонат ион
— карбонат ион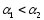
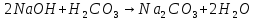
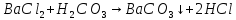
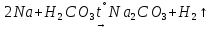

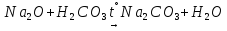
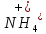 —
хорошо растворяются вводе.
Щелочно-земельных Ме—
плохо растворяются вводе.
—
хорошо растворяются вводе.
Щелочно-земельных Ме—
плохо растворяются вводе.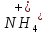 ,
щелочно-земельных Ме—
хорошо растворяются вводе.
,
щелочно-земельных Ме—
хорошо растворяются вводе.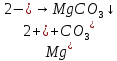
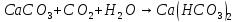
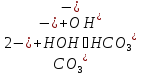

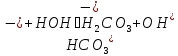

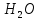
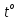
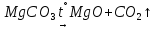
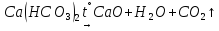
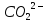
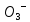
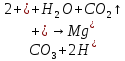
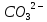 +
+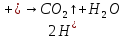
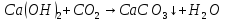
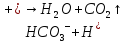
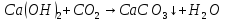
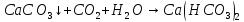
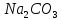 —белый
порошок. (В производстве стекла,
мыла, бумаги...)
—белый
порошок. (В производстве стекла,
мыла, бумаги...)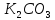 —поташ —
белый порошок. (В производстве
жидкого мыла, стекла...)
—поташ —
белый порошок. (В производстве
жидкого мыла, стекла...)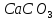 —мел,
мрамор, известняк. (В строительстве)
—мел,
мрамор, известняк. (В строительстве)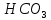 —
белый порошок, питьевая сода. (В пищевой
промышленности, в медицине)
—
белый порошок, питьевая сода. (В пищевой
промышленности, в медицине)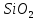


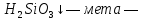
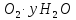
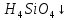
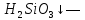 условная
формула
условная
формула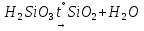
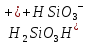 —гидросиликат
ион
—гидросиликат
ион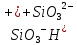 —
силикат ион
—
силикат ион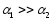
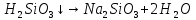
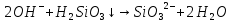
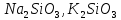
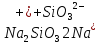
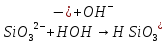
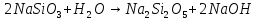
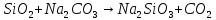
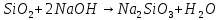
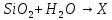
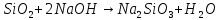
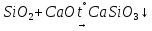
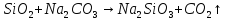
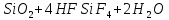 травление
стекол
травление
стекол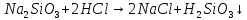
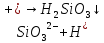
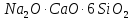 —обычное
стекло
—обычное
стекло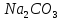 —
сода
—
сода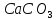 —известняк
—известняк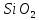 —белый
песок
—белый
песок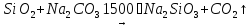


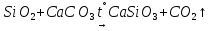
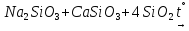
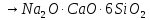
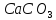 —
известняк, глина, добавки
—
известняк, глина, добавки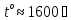
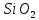 ,
,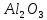
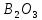 —
увеличивает термостойкость и оптические
свойства
—
увеличивает термостойкость и оптические
свойства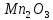 —
фиолетовый
—
фиолетовый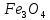 —
зеленый
—
зеленый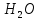 + песок → бетон
+ песок → бетон