- •Неорганическая химия наука о природе
- •Природные явления
- •Чистые вещества и смеси
- •Химический элемент
- •Химический символ обозначает
- •Химический состав
- •Химическая формула и расчет по формулам
- •Схемы строения атомов химических элементов побочных подгрупп
- •Периодичность изменения химических и физических свойств элементов главных подгрупп
- •Валентность
- •Составление химических формул по валентности
- •Электроотрицательность
- •Относительная электроотрицательность химических элементов
- •Степень окисления
- •Химическая связь
- •Типы кристаллических решеток
- •Взаимосвязь основных химических понятий
- •Свойства и применение кислорода
- •Классификация сложных неорганических веществ
- •Генетические связи между классами неорганических веществ
- •Классификация кислот
- •Номенклатура кислот и средних солей
- •Химические свойства сложных неорганичеких веществ
- •Примеры уравнений химических реакций
- •Химические свойства воды ()
- •Очистка воды
- •Растворы
- •Растворимость веществ
- •Количество растворенного вещества
- •Концентрации растворов
- •Химические реакции классификация химических реакций
- •Окислительно-восстановительные реакции
- •Составление уравнений окислительно-восстановительных реакций методом электронного баланса
- •Форма записи о.В.Р.
- •Гидролиз солей количественные соотношения при химических реакциях
- •2. Кислоты, основания, амфотерные
- •3. Реакции ионного обмена
- •Металлы
- •1. Ме — химический элемент
- •2. Ме — простое вещество
- •3. Химические свойства металлов
- •Промышленные способы получения металлов
- •Электрохимический ряд напряжений металлов
- •Электролиз
- •Применение электролиза
- •Металлы I группы главной подгруппы (щелочные) Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Металлы II группы главной подгруппы (щелочно-земельные) Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Характер соединений оксидов ме
- •II группы главной подгруппы
- •Жесткость воды
- •Элементы III группы главной подгруппы Сравнительная характеристика химических элементов
- •Сравнительная характеристика физических свойств простых веществ
- •Неметаллы
- •1. НеМе—химический элемент
- •2. НеМе — простое вещество
- •Углерод (с). Аллотропия углерода (с)
- •Угольная кислота
- •Соли угольной кислоты
- •Аллотропия кремния
- •Соединения кремния (si)
- •Силикатная промышленность
- •Простые вещества, образованные элементами
- •V группы главной подгруппы
- •Азот — простое вещество
- •Получение азота (n2)
- •Синтез аммиака в промышленности
- •Получение аммиака в лаборатории
- •Химические свойства
- •Оксиды азота (n)
- •Азотная кислота
- •Нитраты
- •Аллотропия форфора (р)
- •Химические свойства фосфора (р)
- •Соединения фосфора (р)
- •Фосфорная кислота
- •Элементы VI группы главной подгруппы
- •Простые вещества элементов VI группы главной подгруппы
- •Аллотропия кислорода ("о")
- •Аллотропия серы (s)
- •Соединения серы (s)
- •Кислоты серы (s)
- •Производство
- •Элементы VII группы главной подгруппы (галогены) Сравнительная характеристика химических элементов
- •Простые вещества элементов VII группы главной подгруппы
- •Химические свойства простых веществ на примере
- •Соляная кислота (hCl)
- •Химические свойства соляной кислоты
- •Медь (Cu) — представитель химических элементов побочных подгрупп
- •Железо (Fe) — представитель химических элементов побочных подгрупп
- •Железо (Fe) — простое вещество
- •Химические свойтсва () — восстановитель
- •Соединения железа в степени окисления
- •Производство чугуна
- •Производство стали
- •Способы получения стали
- •Реакции, лежащие в основе производства стали кислородно-конвертерным и мартеновским способами
- •Хром (Cr) — представитель химических элементов побочных подгрупп
- •Хром (Cr) — простое вещество
- •Химические свойства Cro
- •Соединения хрома (Cr)
Неорганическая химия наука о природе
Все вещества состоят из атомов и молекул
Природные явления
физические химические
|
Состав истроение молекул не меняются, новые вещества не образуются |
|
Состав истроение молекул меняются, образуются новые вещества |
|
ВЕЩЕСТВА |
|
ЧИСТЫЕ |
|
СМЕСИ |
|
Простые |
|
Сложные |
|
Гомогенные |
|
Гетерогенные |
|
аМеталлы Fe, Cu, Al
|
|
Неметаллы S,
|
|
Неорганические |
|
Органические |
|
Воздух |
|
Соленая вода |
|
Молоко |
|
Мутная вода |
Чистые вещества и смеси
|
Простое
вещество
отдельные молекулы |
|
Сложное
вещество
отдельные молекулы |
|
Смесь
|
Химический элемент
Это определенный вид атомов, характеризующийся определенным зарядом
атома и строением электронных оболочек.
|
Формы существования химического
элемента |
|
одиночные атомы |
|
простое вещество |
|
сложное вещество |
Химический символ обозначает
Название элемента: O— кислород, Fe— железо
Один атом этого элемента — H или несколько атомов — 5Cu
(5 атомов меди)
Относительную атомную массу элемента
Химический состав
АТОМ МОЛЕКУЛА
химически
|
неделимая частица
атомы
водорода Н
химический
знак
атомы кислорода О |
делимая часть
вещества
молекулы
воды
формула |
|
размер | |
|
атома: |
молекулы:
от
|
|
масса | |
|
атома:
атом
углерода С
|
молекулы:
от
углерода = 1 а.е.м.
|
|
относительная | |
|
атомная масса
|
молекулярная масса
|
Химическая формула и расчет по формулам
знаки
химических элементов 1)
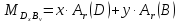
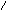
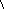
nDxBy
индекс (кол-во
2)
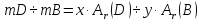
атомов
в молекуле) 3)
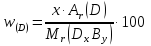
коэффициент (кол-во молекул)
ЗАКОН ПОСТОЯНСТВА СОСТАВА ВЕЩЕСТВА
ОСНОВНЫЕ ЧАСТИЦЫ, СОСТАВЛЯЮЩИЕ
ВЕЩЕСТВО. ЭЛЕМЕНТАРНЫЕ ЧАСТИЦЫ
|
протон
р+ |
|
нейтрон
no |
|
электрон
|
Физическая связь
|
Ядро | ||
|
|
|
Атом |
Химическая связь
|
Молекулы, существующие в свободном виде |
|
Атомные (или иные "комплексы"), не существующие в свободном виде |
|
Вещества молекулярного строения (сера, сахар, кислород, вода) |
|
Вещества немолекулярного строения (металлы, алмаз, соль) |
СТРОЕНИЕ АТОМА
|
Порядковый номер элемента |
|
Массовое
число элемента |
|
заряд
ядра |
|
число р+ |
|
число
|
|
число р+ + число no |
р+= 7
|
массовое
число порядковый
номер |
|
no = (14 – 7) = 7 |
Электроны в атоме распределяются на соответствующих
энергетических уровнях и подуровнях согласно их энергии
|
Номер энергетического уровня N (определяется номером периода) |
Максимальное
число
|
Подуровни |
|
1 |
2
|
s2 |
|
2 |
8
|
s2p6 |
|
3 |
18
|
s2p6d10 |
|
4 |
32
|
s2p6d10f14 |



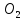 ,
C
,
C




























































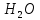 —химическая
—химическая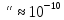 м
м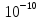 м до ∞
м до ∞ г
г



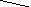
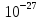 г
до ∞
г
до ∞














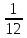 часть
атома
часть
атома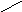
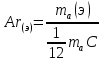









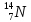
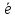 =
7
=
7