
- •М о д у л ь 1. Основні поняття і закони хімії т е м а 1 (вступна). Основні поняття і закони хімії.
- •1.4. Список рекомендованої літератури
- •2.1. Рекомендації до вивчення теоретичного матеріалу
- •2.4. Лабораторна робота
- •2.5. Список рекомендованої літератури
- •3.1.Рекомендації до вивчення теоретичного матеріалу
- •3.2. Приклади розвязування типових задач
- •3.3. Задачі для самостійного рішення: 182, 183, 190, 208
- •3.4. Лабораторна робота
- •3.5. Список рекомендованої літератури
- •4.1. Рекомендації до вивчення теоретичного матеріалу
- •4.2. Приклади розвязування типових задач.
- •4.3. Задачі для самостійного рішення: 720, 724, 736
- •4.4. Лабораторна робота
- •Дослід 3. Утворення сольватокомплексів
- •Дослід 6. Стійкість комплексів
- •4.5. Список рекомендованої літератури
- •М о д у л ь 2. Основні закономірності протікання хімічних реакцій т е м а 5. Енергетика хімічних процесів
- •5.1. Рекомендації до вивчення теоретичного матеріалу
- •5.2. Приклади розвязування типових задач
- •Розв’язок: Температуру початку реакції розрахуємо за формулою:
- •5.3. Задачі для самостійного рішення: № 283, 285, 303, 311
- •5.4. Лабораторна робота
- •5.5. Список рекомендованої літератури
- •Тема 6. Швидкість протікання хімічних реакцій та хімічна рівновага
- •6.2.Приклади розвязування типових задач
- •6.3. Задачі для самостійного рішення: 330, 332, 334, 352
- •6.4. Лабораторна робота
- •Загальні вказівки
- •М о д у л ь 3. Розчини т е м а 7. Розчинність. Способи вираження концентрації
- •8.1. Рекомендації до вивчення теоретичного матеріалу
- •8.3. Задачі для самостійного розвязування: 1030, 1031, 1035, 1037
- •8.4. Лабораторна робота
- •8.5. Список рекомендованої літератури
- •Т е м а 9. Властивості розчинів. Рівноваги у розчинах електролітів
- •9.1. Рекомендації до вивчення теоретичного матеріалу
- •9.2. Приклади розвязування типових задач
- •9.3. Задачі для самостійного рішення: № 516, 544, 586
- •9.4. Лабораторна робота
- •9.5. Список рекомендованої літератури
- •Тема 10. Окисно-відновні реакції
- •10.1. Рекомендації до вивчення теоретичного матеріалу
- •10.2. Приклади рішення типових задач
- •10.3. Задачі для самостійного рішення: 624, 625, 626, 640
- •10.4. Лабораторна робота
- •10.5. Список рекомендованої літератури
- •М о д у л ь 4. Електрохімічні процеси
- •Т е м а 11. Гальванічні елементи
- •11.1. Рекомендації до вивчення теоретичного матеріалу
- •11.2. Приклади розвязування типових задач
- •1.3. Задачі для самостійного рішення: 658, 660, 661
- •11.4. Лабораторна робота
- •11.5. Список рекомендованої дітератури
- •12.1. Рекомендації до вивчення теоретичного матеріалу
- •12.2. Приклади розв’язку типових задач
- •12.4. Лабораторна робота
- •12.5. Список рекомендованої літератури
- •13.1. Рекомендації до вивчення теоретичного матеріалу
- •13.2. Приклади рішення типових задач
- •13.3. Задачі для самостійного рішення 689, 690, 695, 709
- •13.4. Лабораторна робота
- •13.5. Список рекомендованої літератури
- •Тема 14. Властивості неметалів viiа групи (f, Cl, Br, I)
- •14.1. Рекомендації до вивчення теоретичного матеріалу
- •14.2. Приклади розв’язку типових задач
- •14.3. Задачі для самостійного розв’язування: 823, 824, 831.
- •14.4. Лабораторна робота
- •14.5. Список рекомендованої літератури
- •Тема 15. Властивості неметалів viа групи (o, s, Se, Te)
- •15.1 Рекомендації до вивчення теоретичного матеріалу
- •15.2. Приклади розв’язку типових задач
- •15.3. Задачі для самостійного розв’язку
- •15.4. Лабораторна робота
- •15.5. Список рекомендованої літератури
- •Тема 16. Властивості неметалів vа групи (n, p, As, Sb)
- •16.1. Рекомендації до вивчення теоретичного матеріалу
- •16.2. Приклади розв’язування типових задач
- •16.3. Задачі для самостійного розв’язку: 901, 902, 917
- •16.4. Лабораторна робота
- •Дослід 8. Гідроліз фосфатів
- •16.5. Список рекомендованої літератури
- •Тема 17. Властивості неметалів іvа групи (с, Sі)
- •17.1. Рекомендації до вивчення теоретичного матеріалу
- •17.2. Приклади розв’язування типових задач
- •17.3. Задачі для самостійного розв`язку: № 944, 949, 964.
- •17.4. Лабораторна робота
- •17.5. Список рекомендованої літератури
- •М о д у л ь 5. Властивості конструкційних і інструментальних металів і їхніх сполук. Полімерні матеріали
- •18.1. Рекомендації до вивчення теоретичного матеріалу
- •18.2. Приклади розвязування типових задач
- •18.3. Задачі для самостійного рішення: 1009, 1051, 1053
- •18.4. Лабораторна робота
- •Дослід 6. Окисно-відновні властивості сполук титана
- •Дослід 7. Електрохімічне оксидування (анодирування) алюмінію (елементи ндрс)
- •Сполуки водних розчинів для фарбування анодируваного алюмінію
- •18.5. Список рекомендованої літератури
- •Т е м а 19. Властивості заліза, кобальту, нікелю
- •19.1. Рекомендації до вивчення теоретичного матеріалу
- •19.2. Приклади розвязування типових задач
- •19.3. Задачі для самостійного рішення: 1113,1114, 1117, 1118
- •19.4. Лабораторна робота
- •19.5. Список рекомендованої літератури
- •Т е м а 20. Властивості металів підгрупи Cr і Mn і їх сполук
- •20.1. Рекомендації до вивчення теоретичного матеріалу
- •20.2. Приклади розвязування типових задач
- •20.3. Задачі для самостійного рішення: 1084, 1096, 1097
- •20.4. Лабораторна робота
- •20.5. Список рекомендованої літератури
- •21. Властивості металів vb групи (підгрупи ванадію)
- •21.1 Рекомендації до вивчення теоретичного матеріалу
- •21.2. Приклади розв’язування типових задач
- •21.3. Задачи для самостійного розв’язування : №1081, 1082
- •21.4. Лабораторна робота
- •21.5. Список рекомендованої літератури
- •22.1. Рекомендації до вивчення теоретичного матеріалу
- •22.2. Приклади розвязування типових задач
- •22.3. Задачі для самостійного рішення: 1071, 1072, 1077
- •2.4. Лабораторна робота
- •Дослід 3. Окисно-відновні властивості сполук станума і плюмбума
- •Дослід 6. Електролітичне лудіння (з елементами ндрс)
- •22.5. Список рекомендованої літератури
- •Т е м а 23. Властивості конструкційних металів ib і iib груп
- •23.1. Рекомендації до вивчення теоретичного матеріалу
- •23.2. Приклади розвязування типових задач
- •22.3. Задачі для самостійного рішення 995, 984, 1025
- •23.4. Лабораторна робота
- •23.5. Список рекомендованої літератури
- •24.1. Рекомендації до вивчення теоретичного матеріалу
- •24.2. Лабораторна робота
- •24.3. Список рекомендованої літератури
- •Питання до колоквіуму за темами «Будова атома. Періодичний закон. Властивості елементів. Хімічний зв'язок. Комплексні сполуки. Типи взаємодії молекул»
- •Тиск водяної пари при різних температурах
- •Добуток розчинності (др) важкорозчинних сполук (25оС)
- •Індивідуальні завдання до теми «Основні поняття і закони хімії»
- •Індивідуальні завдання до теми : "Електролітична дисоціація, рН, гідроліз солей"
- •Тема 1. (вступна). Основні поняття і закони хімії
- •Тема 2. Закон еквівалентів…………………………………………………………………....7
- •Тема 3. Будова атома. Періодичний закон. Властивості елементів..................................10
- •Тема 4. Хімічний зв'язок. Комплексні сполуки……………………….....................................15
- •Тема 5. Енергетика хімічних процесів………………………………….................................21
- •Тема 6. Швидкість хімічних реакцій і хімічна рівновага……................................................29
- •Тема 7. Розчинність. Способи вираження концентрації……………..................................33
- •Тема 18. Властивості легких конструкційних металів
Тиск водяної пари при різних температурах
-
Температура,
˚С
Тиск,
кПа/мм рт.ст
Температура,
˚С
Тиск,
кПа/мм рт.ст.
Температура,
˚С
Тиск,
кПа/мм рт.ст.
14
15
16
17
18
1,598/12,0
1,705/12,8
1,817/13,6
1,935/14,5
2,061/15,5
19
20
21
22
23
2,189/16,5
2,339/17,5
2,486/18,6
2,643/19,8
2,841/21,1
24
25
26
27
28
2,902/22,4
3,170/23,8
3,362/25,2
3,561/26,7
3,779/28,4
Т а б л и ц я Д 2.2
Відносна електронегативність елементів ( χ ) по Л. Полінгу
|
Групи
| |||||||
|
I
|
II
|
III |
IV |
V |
VI |
VII |
VIII |
|
H 2,1 |
|
|
|
|
|
|
|
|
Li 1,0 |
Be 1,5 |
B 2,0 |
C 2,5 |
N 3,0 |
O 3,5 |
F 4,0 |
|
|
Na 0,9 |
Mg 1,2 |
Al 1,5 |
Si 1,8 |
P 2,1 |
S 2,5 |
Cl 3,0 |
|
|
K 0,8 |
Ca 1,0 |
Sc 1,3 |
Ti 1,5 |
V 1,6 |
Cr 1,6 |
Mn 1,5 |
Co; Ni 1,9; 1,9 |
|
|
Zn 1,6 |
Ga 1,6 |
Ge 1,8 |
As 2,0 |
Se 2,4 |
Br 2,8 |
|
|
Pb 0,8 |
Sr 1,0 |
Y 1,2 |
Zn 1,5 |
Nb 1,6 |
Mo 1,8 |
Te 1,8 |
Ru; Rh; Pd 2,2; 2,2; 2 |
|
|
Cd 1,7 |
In 1,7 |
Sn 1,8 |
Sb 1,9 |
Te 2,1 |
I 2,5 |
|
|
Cs 0,7 |
Ba 0,9 |
La – Lu 1,0 – 1,2 |
Hg 1,3 |
Ta 1,5 |
W 1,7 |
Re 1,9 |
Os; Ir; Pt 2,2; 2,2; 2,2 |
|
|
Hg 1,9 |
|
Pb 1,9 |
Bi 1,9 |
Po 2,0 |
At 2,2 |
|
|
Fr 0,7 |
Ra 0,9 |
|
|
|
|
|
|
Т а б л и ц я Д. 2.3
Константи нестійкості (Кн) деяких комплексних іонів
-
Схема дисоціації іона
Кн
РК
Галогеніди
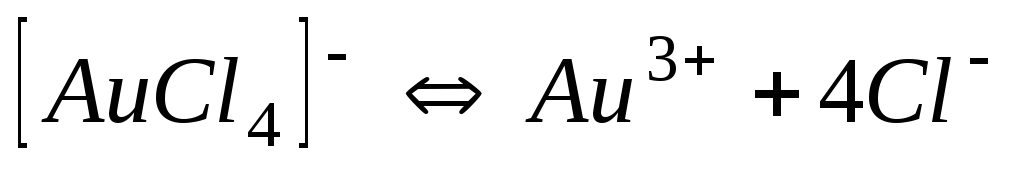
5,010-22
21,30

9,310-3
2,0
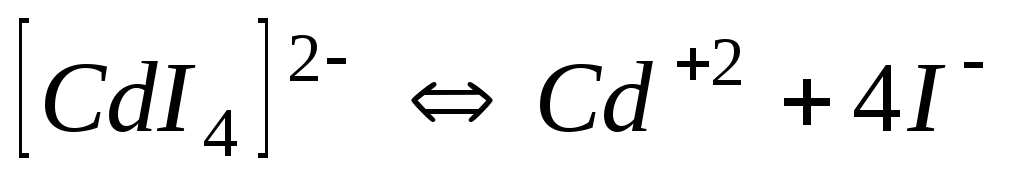
7,910-7
6,10

2,610-3
2,58
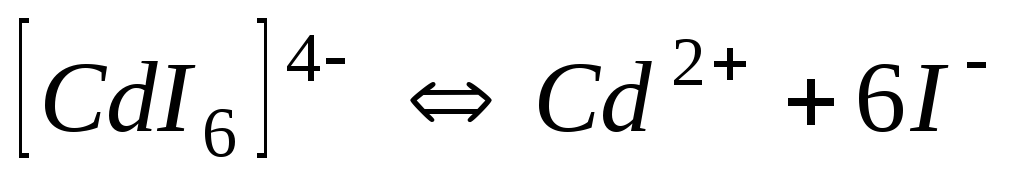
1,010-6
6,00
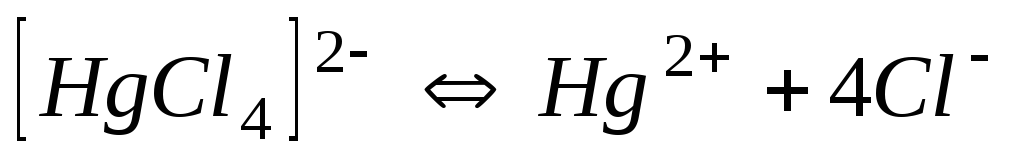
6,0310-16
15,22

1,010-21
21,00
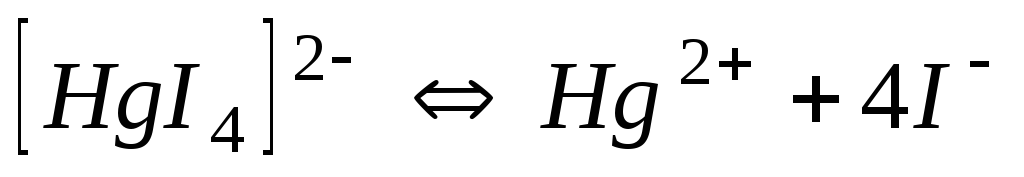
1,3810-30
29,86

1,4210-4
3,85
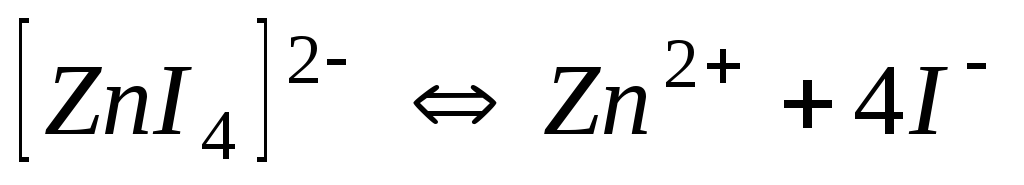
220,0
-2,34
Роданіди
Схема дисоціації
Кдисс
РК
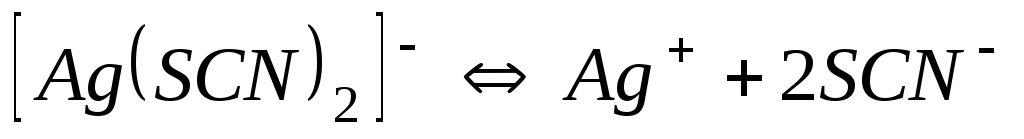
2,710-8
7,57
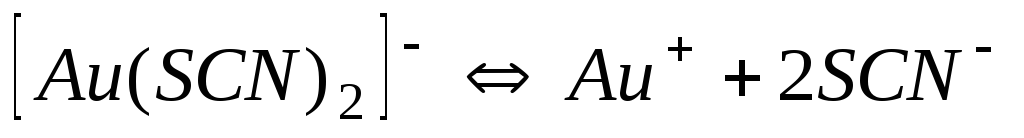
1,010-23
23,0
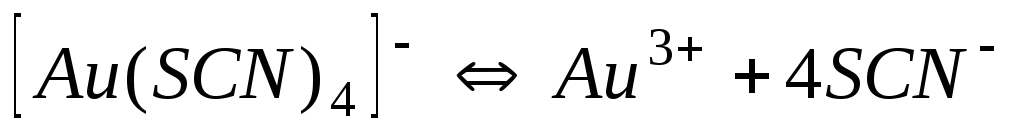
1,010-42
42,00
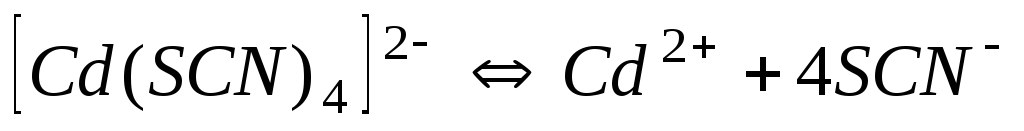
1,6710-2
1,78

5,010-2
1,30
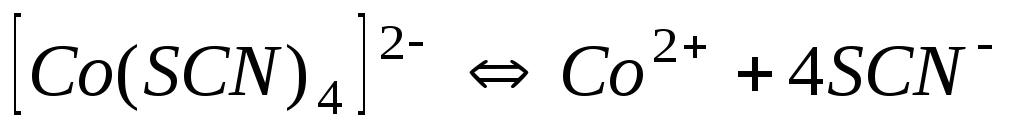
5,510-3
2,26

1,2910-22
21,89
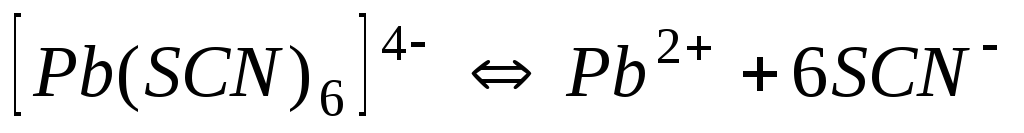
20
-0,30
Ціаніди
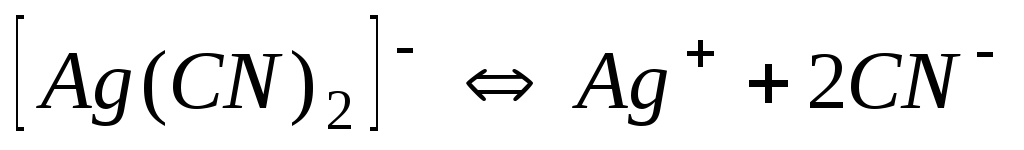
1,010-21
21,00
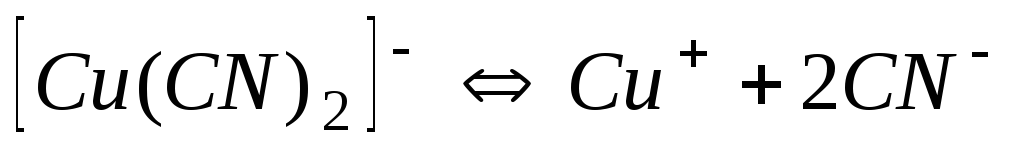
1,010-24
24,00
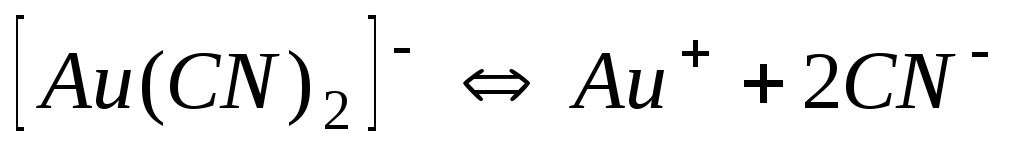
5,010-39
38,30
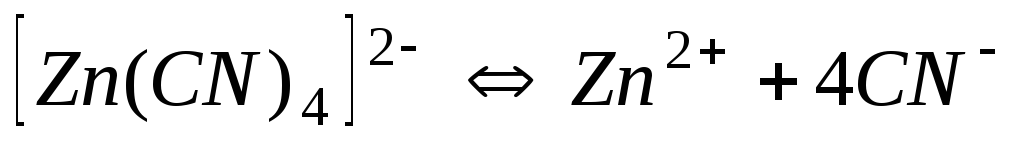
1,010-16
16,00

7,6610-18
17,11
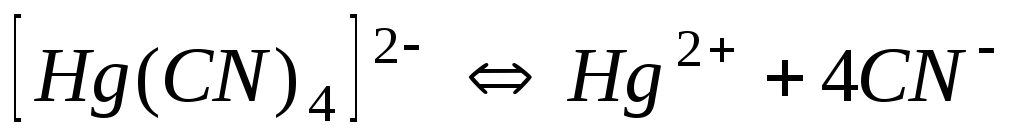
3,0210-42
41,52
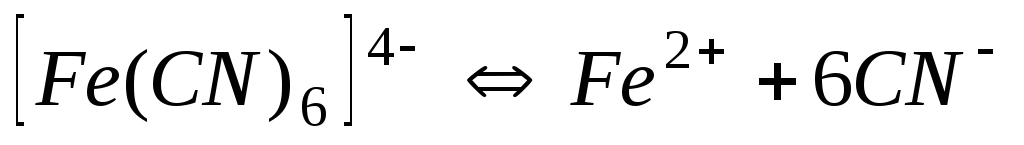
1,010-24
24,00
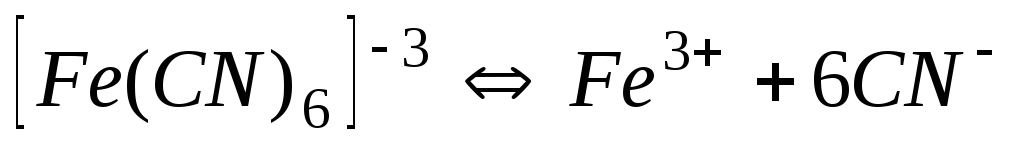
1,010-31
31,00
Аміакати

5,8910-8
7,23
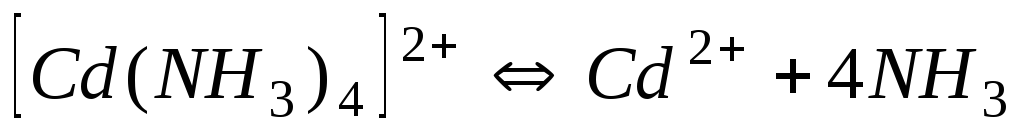
2,7510-7
6,56
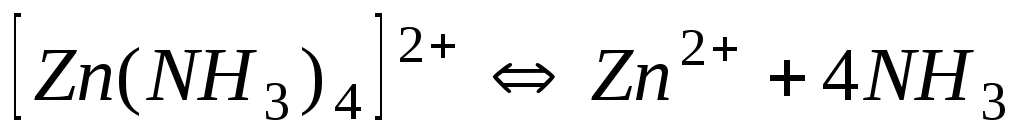
2,010-9
8,01

9,3310-13
12,03
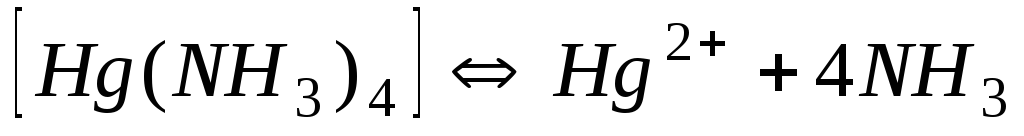
5,310-20
19,28
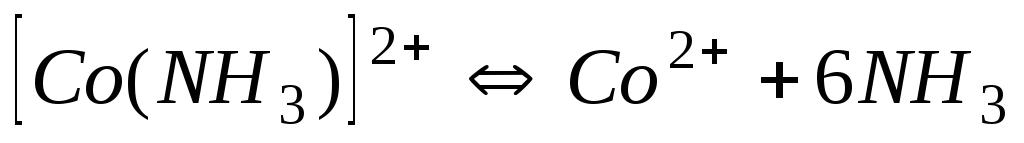
4,0710-5
4,39
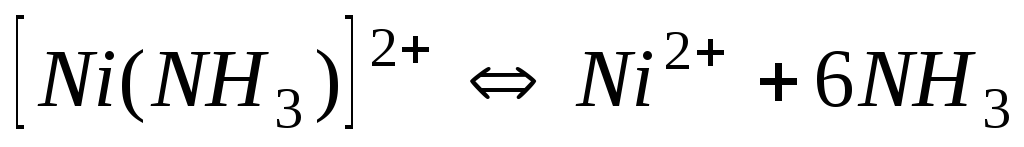
9,7710-9
8,01
Гідроксокомплекси
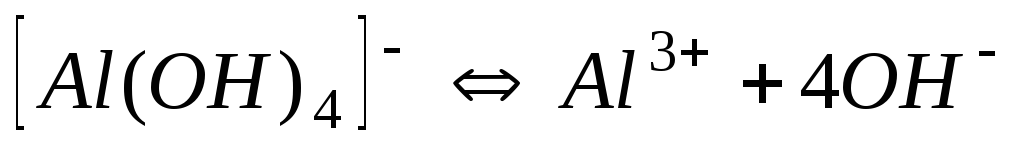
1,010-33
33,00
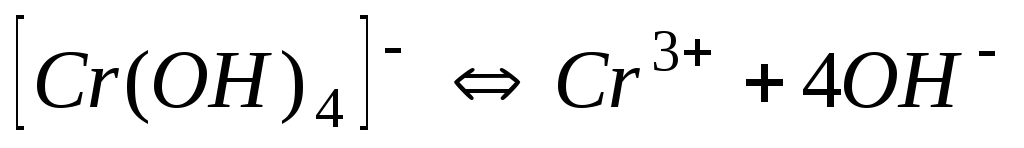
1,2610-30
29,00
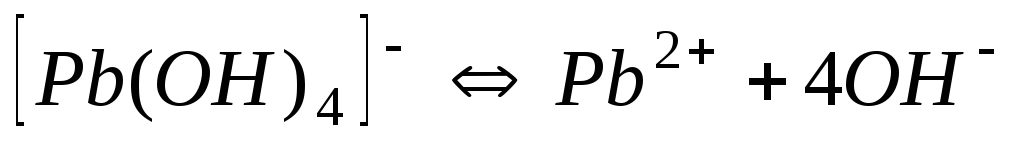
5,010-12
11,30
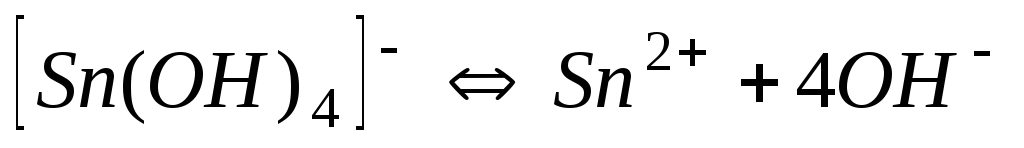
7,410-26
25,13
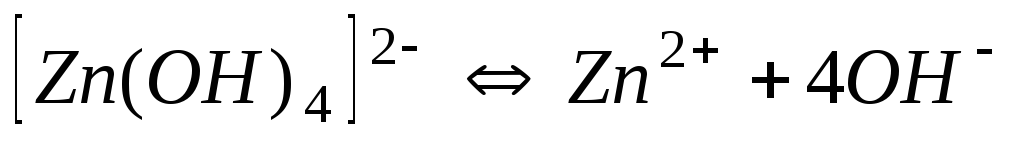
2,210-15
14,66
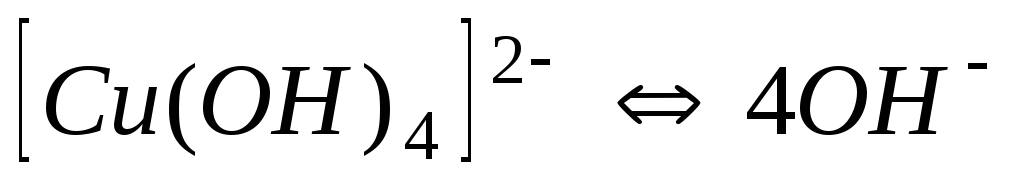
3,210-19
18,50
Комплекси з трилоном Б (Edta)
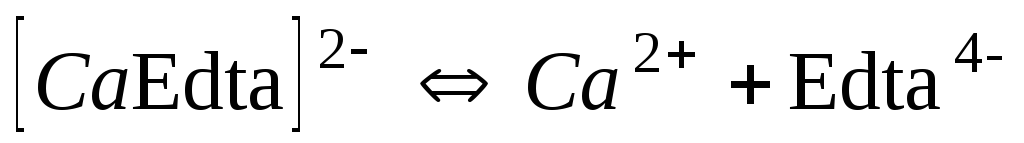
2,6910-11
10,57
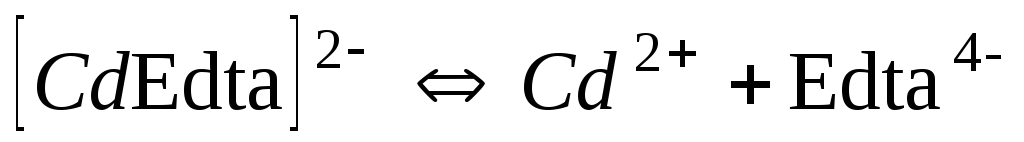
2,5710-17
16,59
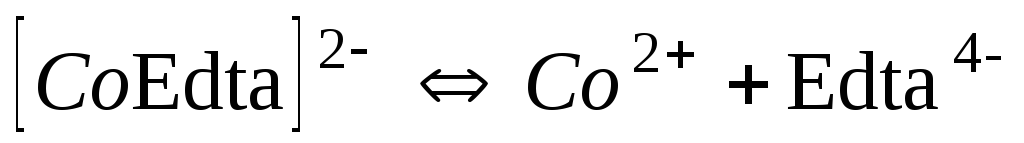
6,1710-17
16,21
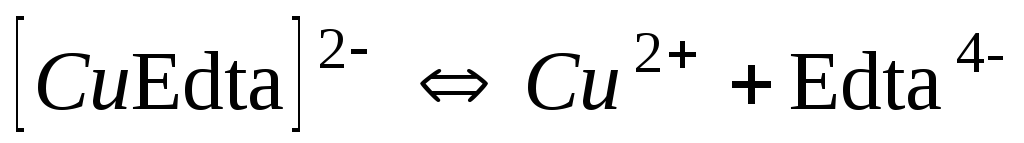
1,5810-19
18,80

4,6810-15
14,33

7,9810-26
25,10
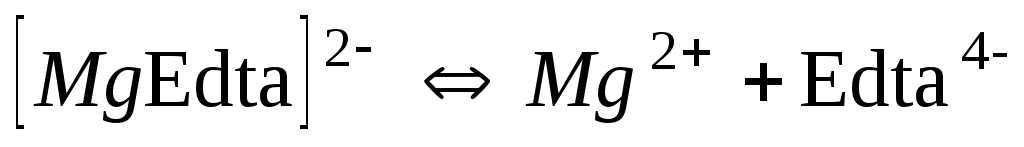
2,0410-9
8,69
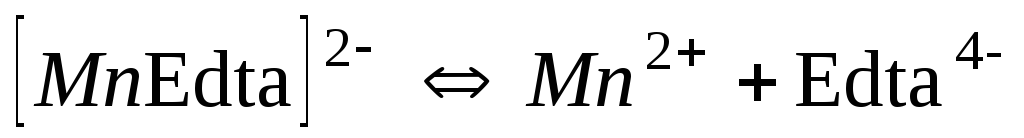
9,1210-15
14,04
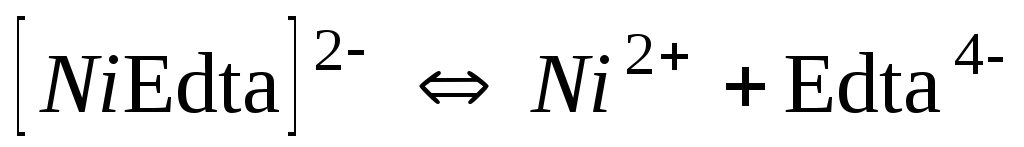
2,4010-19
18,62
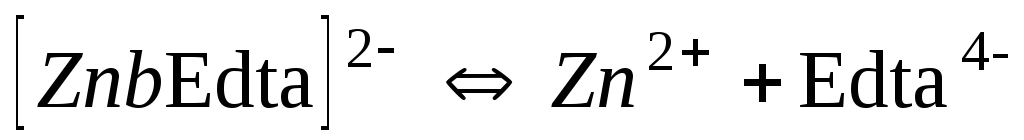
3,1610-17
16,50
Комплекси з оксалатами-іонами С2О42- (Ох2-)
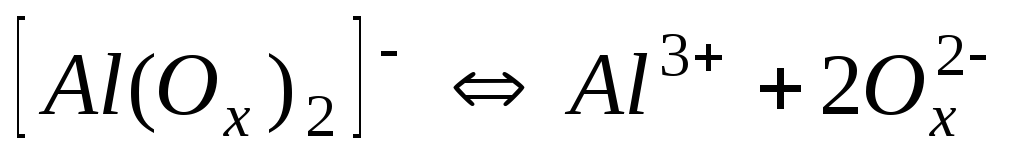
1,010-13
13,00

2,010-5
4,70

6,9210-7
6,16
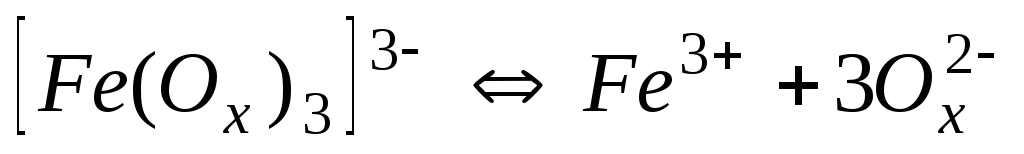
6,310-21
20,20
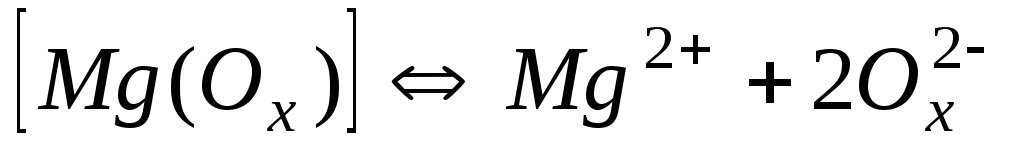
3,7210-4
3,43
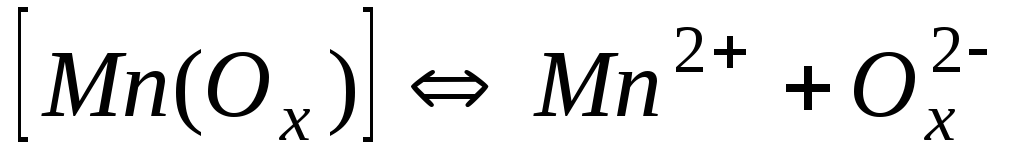
1,5110-4
3,82
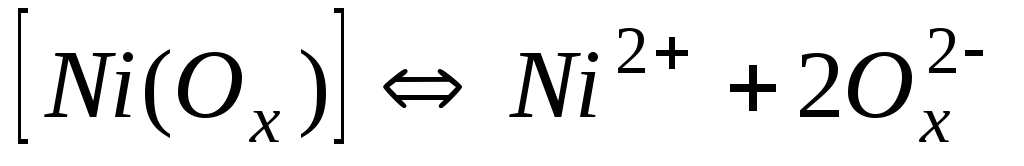
5,010-6
5,30

1,010-5
5,00
Т а б л и ц я Д. 2.4
Термодинамічні константи деяких речовин
|
Речовина
|
∆H°298, кДж/моль |
∆G°298, кДж/моль |
S°298, Дж/(моль . К) |
|
Al (к) |
0 |
0 |
28,31 |
|
Al2O3 (к) |
-1675,0 |
-1576,4 |
50,94 |
|
B (к) |
0 |
0 |
5,87 |
|
B2O3 (к) |
-1264,0 |
-1184,0 |
53,85 |
|
B2H6 (г) |
31,4 |
82,8 |
232,9 |
|
Ba (к) |
0 |
0 |
64,9 |
|
BaCO3 (к) |
-1202,0 |
-1138,8 |
112,1 |
|
Be (к) |
0 |
0 |
9,54 |
|
BeO (к) |
-598,7 |
-581,6 |
14,10 |
|
BeCO3 (к) |
-981,57 |
-944,75 |
199,4 |
|
C (алмаз) |
1,897 |
2,866 |
2,38 |
|
C (графит) |
0 |
0 |
5,74 |
|
CO (г) |
-110,5 |
-137,27 |
197,4 |
|
CO2 (г) |
-393,51 |
-394,38 |
213,6 |
|
C2H2 (г) |
226,75 |
209,2 |
200,8 |
|
C2H4 (г) |
52,28 |
68,12 |
219,4 |
|
CH4 (г) |
-74,85 |
-50,79 |
186,19 |
|
C2H6 (г) |
-84,67 |
-32,89 |
229,5 |
|
C6H6 (ж) |
49,04 |
124,50 |
173,2 |
|
CH3OH (ж) |
-238,7 |
-166,31 |
126,7 |
|
C2H5OH (ж) |
-227,6 |
-174,77 |
160,7 |
|
Ca (к) |
0 |
0 |
41,62 |
|
CaO (к) |
-635,1 |
-604,2 |
39,7 |
|
Ca(OH)2 (к) |
-986,2 |
-896,76 |
83,4 |
|
CaCO3 (к) |
-1206,0 |
-1128,8 |
92,9 |
|
Cl2 (г) |
0 |
0 |
223,0 |
|
HCl (г) |
-92,30 |
-95,27 |
186,7 |
|
HCl (ж) |
-167,5 |
-131,2 |
55,2 |
|
Cr (к) |
0 |
0 |
23,76 |
|
Cr2O3 (к) |
-1141,0 |
-1046,84 |
81,1 |
|
Cu (к) |
0 |
0 |
33,3 |
|
Cu2O (к) |
-167,36 |
-146,36 |
93,93 |
|
CuO (к) |
-165,3 |
-127,19 |
42,64 |
|
Cu(OH)2 (к) |
-443,9 |
-356,90 |
79,50 |
|
Cu(NO3)2 (к) |
-307,11 |
-114,22 |
193 |
|
Fe (к) |
0 |
0 |
27,15 |
|
FeO (к) |
-263,68 |
-244,35 |
58,79 |
|
FeCl2 |
-341,0 |
-302,08 |
119,66 |
|
Fe2O3 (к) |
-821,32 |
-740,99 |
89,96 |
|
FeCl3 (к) |
-405,0 |
-336,39 |
130,1 |
|
FeCO3 (к) |
-744,75 |
-637,88 |
92,9 |
|
H2 (г) |
0 |
0 |
130,6 |
|
H2O (г) |
-241,84 |
-228,8 |
188,74 |
|
H2O (ж) |
-285,84 |
-237,5 |
69,96 |
|
MgO (к) |
-601,24 |
-569,6 |
26,94 |
|
MgCO3 |
-1096,21 |
-1029,3 |
65,69 |
|
N2 (г) |
0 |
0 |
191,5 |
|
N2O (г) |
81,55 |
103,6 |
220,0 |
|
NO (г) |
90,37 |
86,69 |
210,62 |
|
NO2 (г) |
33,89 |
51,84 |
240,45 |
|
N2O4 (г) |
9,37 |
98,29 |
304,3 |
|
NH3 (г) |
-46,19 |
16,64 |
192,5 |
|
HNO3 (ж) |
-173,0 |
-79,91 |
156,16 |
|
NH4C1 (к) |
-315,39 |
-343,64 |
94,56 |
|
NH4OH (ж) |
-366,69 |
-263,8 |
179,9 |
|
О2 (г) |
0 |
0 |
205,03 |
|
РСl3 (г) |
-277,0 |
-286,27 |
311,7 |
|
РСl5 (г) |
-369,45 |
-324,55 |
362,9 |
|
PbO (к) |
-217,86 |
-188,49 |
67,4 |
|
PbO2 (к) |
-276,86 |
-218,99 |
76,44 |
|
S (ромб.) |
0 |
0 |
31,88 |
|
SO2 (г) |
-296,9 |
-300,37 |
248,1 |
|
SO3 (г) |
-395,2 |
-370,37 |
256,23 |
|
H2S (г) |
-20,15 |
-33,02 |
205,64 |
|
SrO (к) |
-590,4 |
-559,8 |
54,4 |
|
SrCO3 (к) |
-1221,3 |
-1137,6 |
97,1 |
|
Zn (к) |
0 |
0 |
41,59 |
|
ZnО (к) |
-349,0 |
-318,19 |
43,5 |
|
ZnS (к) |
-201,0 |
-198,32 |
57,7 |
Т а б л и ц я Д. 2.5
