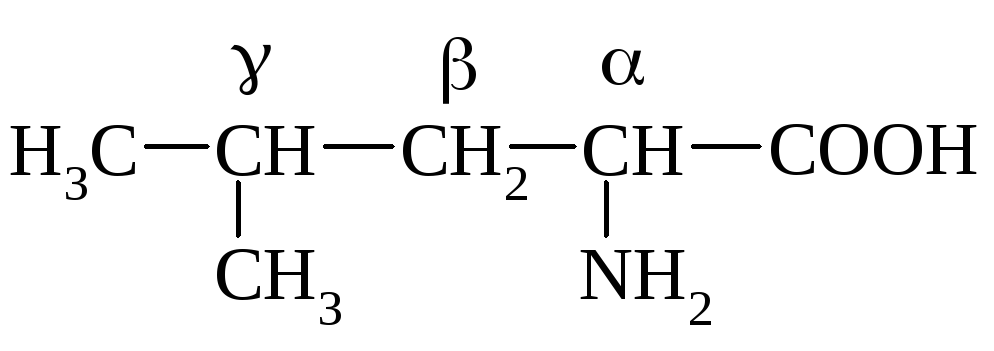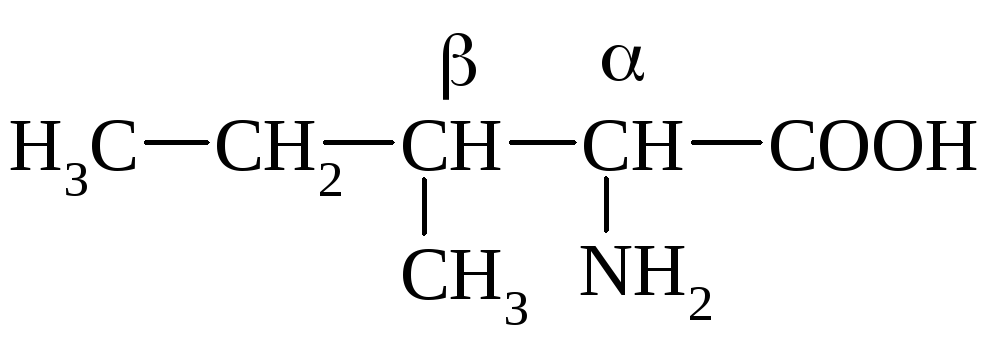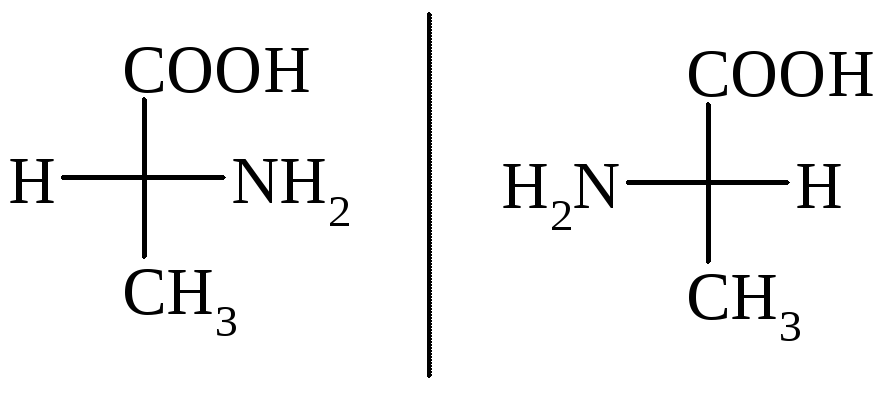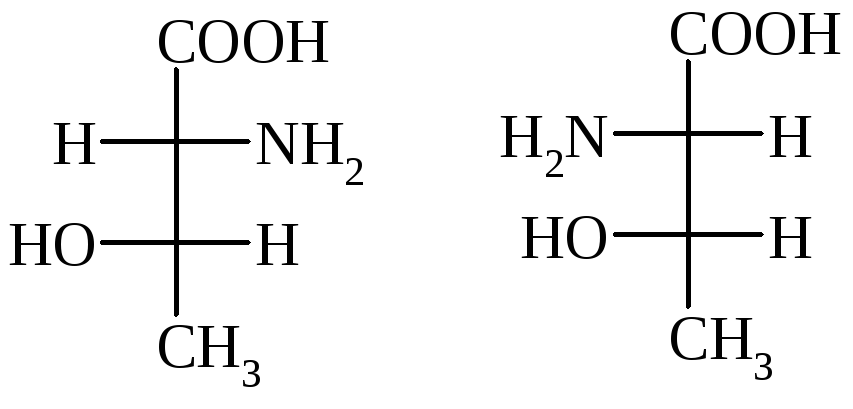- •Модуль 4 Тема занятия №2: “Биологически важные аминокислоты. Белки. Нуклеиновые кислоты.”
- •Номенклатура Обычно ак имеют тривиальное название.
- •Изомерия
- •Классификация
- •Химические свойства
- •I. Кислотно-оснóвные
- •Коричневый Белки
- •Функции белков:
- •Нуклеиновые к-ты (нк)
- •Химический состав нк
- •Мононуклеотиды
- •Аденозинтрифосфат, аденозинтрифосфорная к-та, атф Структура молекулы днк
- •Лабораторная работа
- •Тест Аминокислоты и нк для самостоят. Вариант 1.
- •Вариант 2.
- •Вариант 3.
- •Вариант 4.
- •Вариант 5.
Модуль 4 Тема занятия №2: “Биологически важные аминокислоты. Белки. Нуклеиновые кислоты.”
Цель занятия: изучить строение и химические свойства биологически важных аминокислот, белков, нуклеиновых кислот и их роль в организме.
Студент должен знать:
- строение, прототропную таутомерию, классификацию α-аминокислот;
- строение, структуру и свойства пептидов;
- строение, свойства, структуру белков и их водных растворов;
- строение нуклеиновых кислот;
- лактим-лактамную и прототропную таутомерии азотистых оснований;
- структуру РНК и ДНК.
Студент должен уметь:
- классифицировать аминокислоты и нуклеиновые кислоты;
- объяснить амфотерность аминокислот, их химическое поведение;
- писать схемы образования мононуклеотидов.
Аминокислоты (АК) - это гетерофункциональные соединения, содержащие амино- и карбоксильную группы:
![]()
Номенклатура Обычно ак имеют тривиальное название.
По рациональной номенклатуре их названия составляются путем прибавления к тривиальному названию приставки амино- и буквы греческого алфавита, указывающей положения – NH2 группы по отношению к – СООН.
МН в названии АК используется редко.
Изомерия
Изомерия цепи:
|
Лейцин, a-аминоизокапроновая к-та, a-амино-g-метилвалериановая к-та |
Изолейцин, a-амино-b-метил- валериановая к-та |
2. Изомерия положения гр. – NH2:
|
a-Аланин |
b-Аланин |
3. Оптическая изометрия (обладают все АК, кроме глицина). Отнесение к D- и L-ряду проводят по аналогии с глицериновым альдегидом по расположению Н и –NH2 гр.
Во всех случаях, когда a-АК содержит два и более асимметрических атомов углерода, конфигурацию ее определяют, исходя из a-углеродного атома.
|
D- L- Аланин |
D-Треонин Алло-L-треонин |
В организме обычно имеются L-, a- и алло-формы. В составе белков АК находятся только в L-форме. D-АК встречаются в антибиотиках (грамицидин).
Классификация
По числу –NH2, –COOH групп, а также в зависимости от R- АК подразделяют на: моноаминокарбоновые, моноаминодикарбоновые, диаминокарбоновые, ароматические и гетероциклические.
|
Аланин |
Лизин, a,e-диаминокапроновая к-та |
|
a-Аминоглутаровая к-та, Глутаминовая к-та |
Тирозин, n-оксифенилаланин |
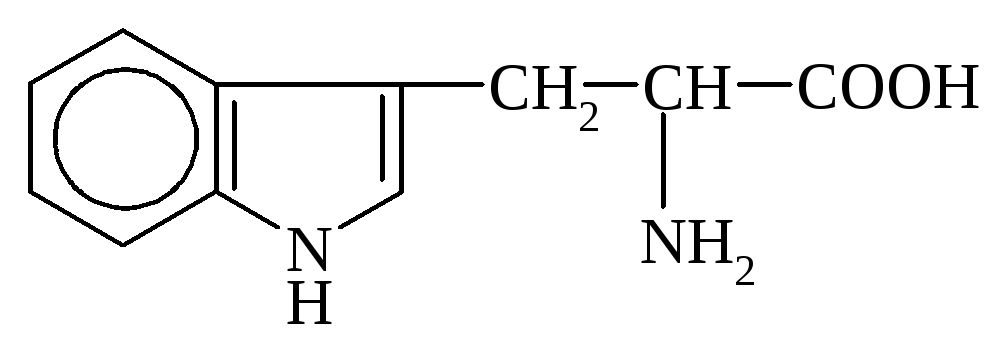
Триптофан,
b-индолилаланин,
3-индолил-2-аминопропановая к-та
Кроме вышесказанного выделяют также окси- и серусодержащие АК:
-
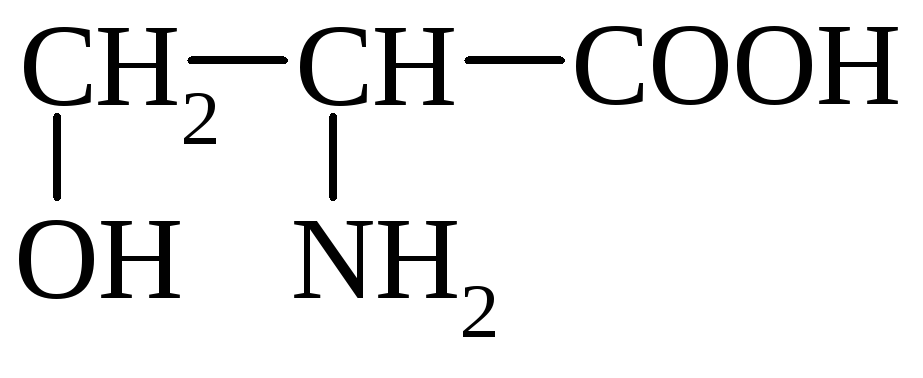
Серин
a-амино-b-оксипропионовая к-та
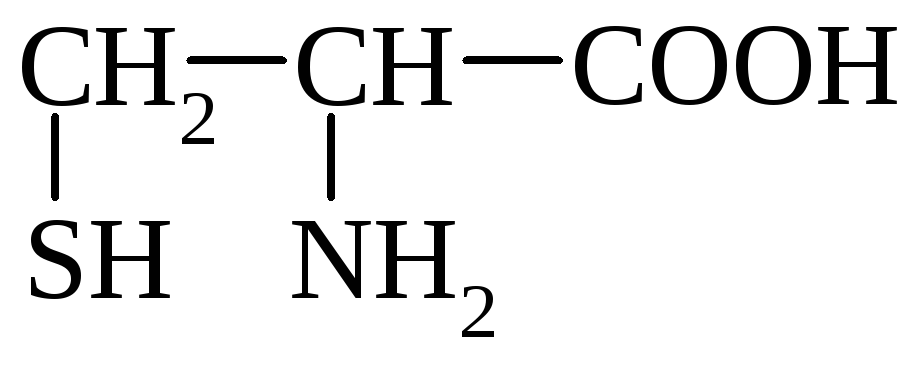
Цистеин,
a-амино-b-тиопропионовая к-та
Живые организмы различаются по своей способности синтезировать АК. АК, не синтезируемые в организме, наз-ся незаменимыми. Это гетероциклические и разветвленные АК.
Химические свойства
I. Кислотно-оснóвные
АК за счет –I группы –NH2 являются более сильными к-тами, чем соответствующие им карбоновые к-ты и более слабыми основаниями, чем амины.
a-АК являются амфотерными соединениями, т.к. содержат в одной молекуле –NH2 гр., обусловливающую оснóвные св-ва и –СOOH – кислотные. Поэтому в зависимости от среды АК могут существовать в р-ре в виде катионов, анионов или диполярных ионов:
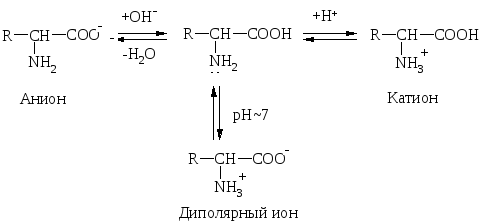
Значение рН р-ра, при котором АК имеет равное количество положительных и отрицательных зарядов, наз-ся изоэлектрической точкой (ИЭТ). Заряд белковой молекулы определяется суммой ионогенных групп –NH3+ и –COO–.
АК, как амфотерные соединения, образуют соли как с к-тами, так и с основаниями:
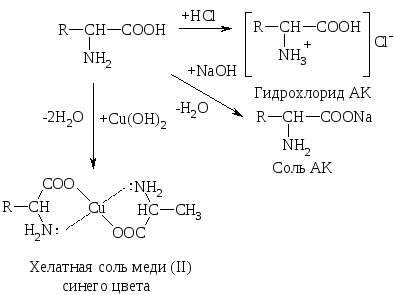
Р-ции по –СООН группе
АК могут диссоциировать, образовывать соли, сложные эфиры, ангидриды, амиды, хлорангидриды.
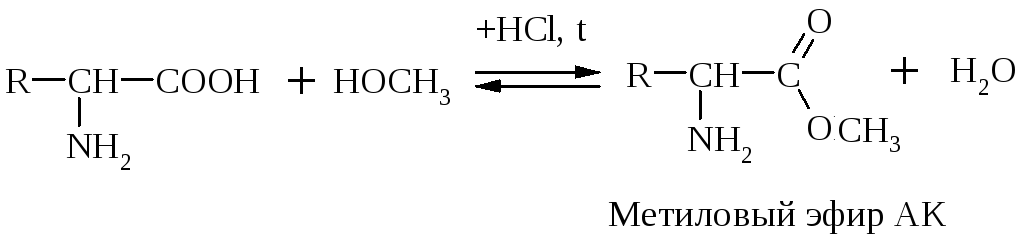
Эта р-ция используется как “защитная” в синтезе белков и пептидов.
Р-ции по –NH2 группе
а) Р-ция солеобразования (см.выше)
б) Р-ция с HNO2

Эта р-ция дезаминирования in vitro. По количеству выделившегося азота определяют кол-во АК (метод Ван-Слайка).
в) Хлорангидриды и ангидриды к-т образуют с АК ацилпроизводные (подобно аминам и мочевине):
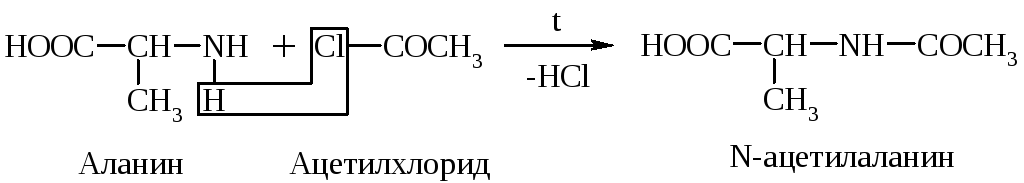
Эта р-ция используется для “защиты” –NH2 гр. в синтезе белков и пептидов.
г) Р-ция с формальдегидом
При взаимодействии с альдегидами a-АК, подобно первичным аминам, образуют основания Шиффа. Для аналитических целей применяется р-ция a-АК с формальдегидом, останавливающаяся на стадии N-гидроксиметильного производного АК (гидроксиметильной наз-ся гр. –СН2ОН):


Последняя р-ция лежит в основе метода формольного титрования. Сами АК вследствие амфотерности не могут быть оттированы щелочью. N-гидросиметильные производные АК содержат свободную –СООН гр. и могут быть определены количественно титрованием щелочью.
Отношение АК к нагреванию
а) a-АК при нагревании могут отщеплять одну или две молекулы воды. При отщеплении одной молекулы воды образуются дипептиды:

Дипептид обладает способностью взаимодействовать с новой молекулой АК с образованием трипептида, тетрапептида и полипептида. Последний является основой белковых молекул. Название ди– и полипептидов строится по названиям тех к-т, из которых они образуются. Поэтому АК, участвующая в образовании пептида имеет окончание –ИЛ, а концевая АК, сохранившая гр. –СООН – полное название:

Аланин Серин АланИЛсерин
Используется сокращенная запись полипептида с указанием концевых групп и названий АК первыми тремя буквами русского или латинского алфавита:
Н2N – Ала – Тир – Гли – Глу – СООН
Аla Tyr Gly Glu
При отщеплении двух молекул воды от двух молекул АК образуется дикетопиперазин (циклический амид):



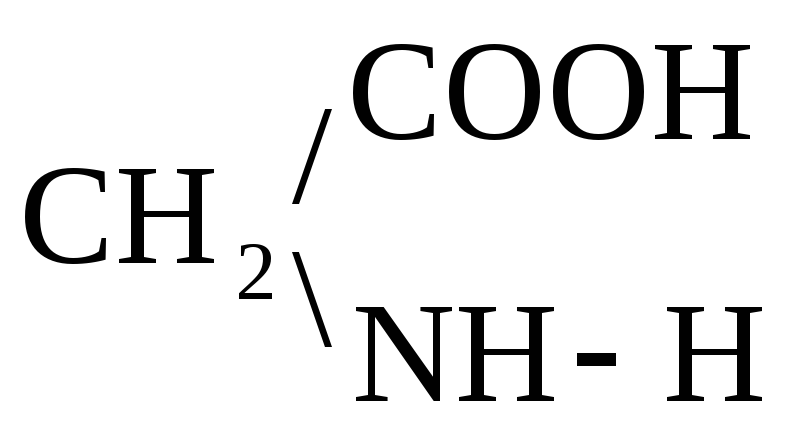 +
+
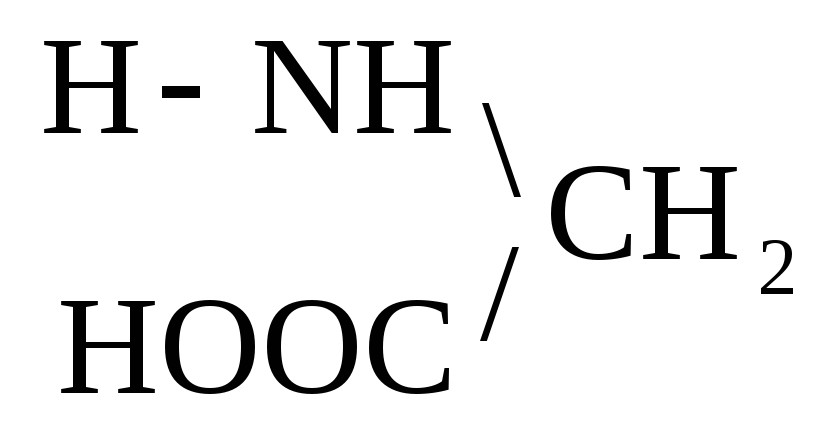
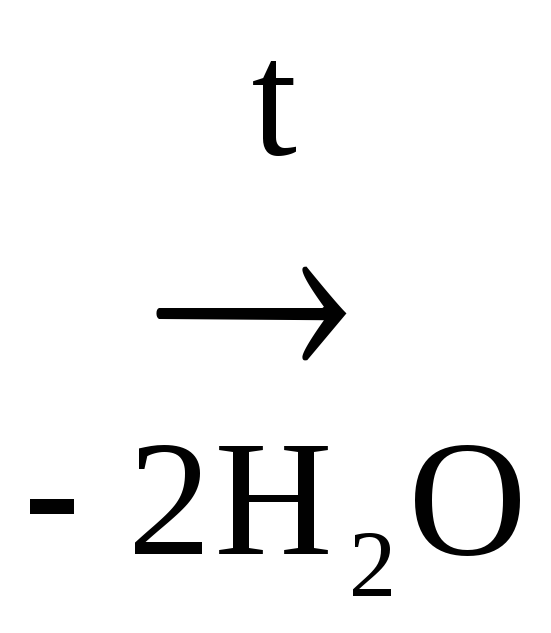

Глицин Дикетопиперазин
б) -АК выделяют при нагревании NH3 и образуют непредельную к-ту, т.е. идет р-ция дезаминирования:
Кротоновая
к-та СН3–СН=СН–СООН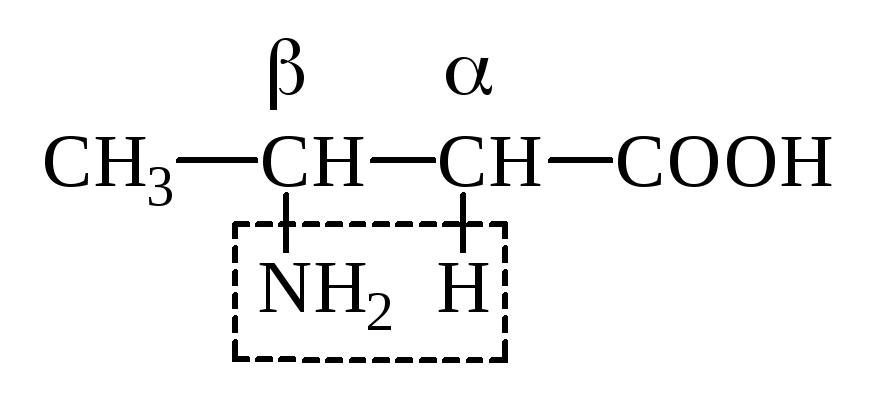
![]()
-Аминомасляная к-та
в) -АК образуют лактамы:
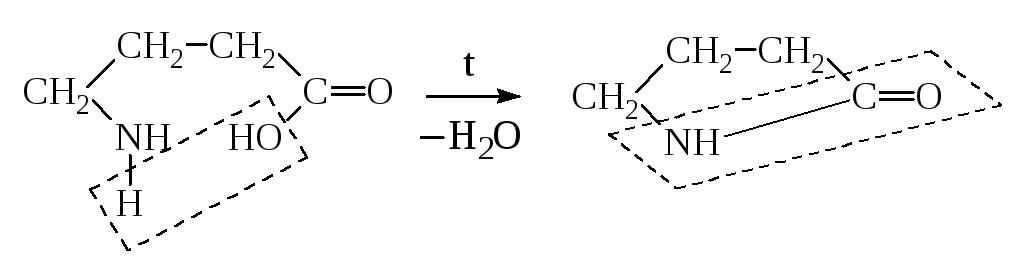
Лактамная
(пептидная) группа
Бутиролактам
-Аминомасляная к-та
Р-ции дезаминирования:
В организме человека и животных под действием различных ферментов происходят процессы дезаминирования. Во всех случаях гр. -NH2 освобождается в виде NH3, а продуктами дезаминирования могут быть жирные к-ты, окси- и кеток-ты. При этом окислительное дезаминирование преобладает:
а) Окислительное дезаминирование
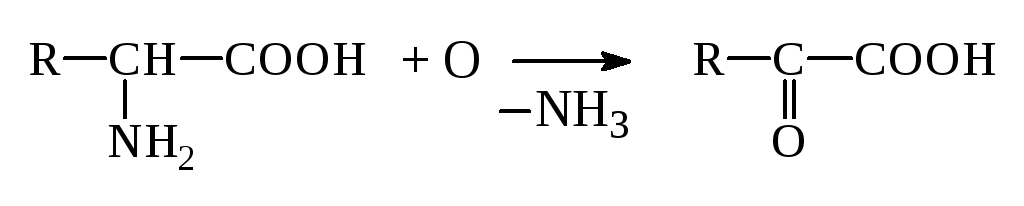
Оксок-та
б) Восстановительное
К-та

в) Гидролитическое
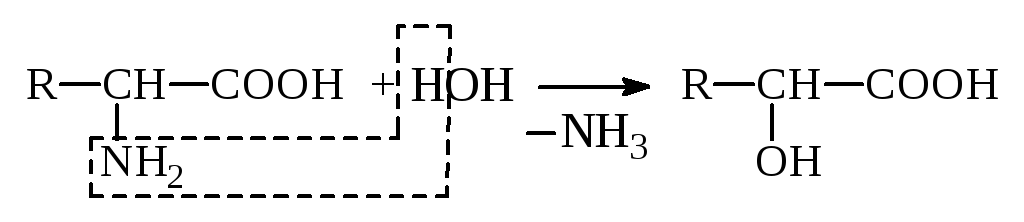
Оксик-та
г) Внутримолекулярное
Непредельная
к-та

Р-ции декарбоксилирования
Карбоновые
к-ты in
vitro
декарбоксилируются в очень жестких
условиях. Введение в -положение
ЭА групп -NH2,
![]() ,
–ОН способствует стабилизации карбоаниона
и поэтому такие замещеные к-ты очень
легко декарбоксилируются:
,
–ОН способствует стабилизации карбоаниона
и поэтому такие замещеные к-ты очень
легко декарбоксилируются:
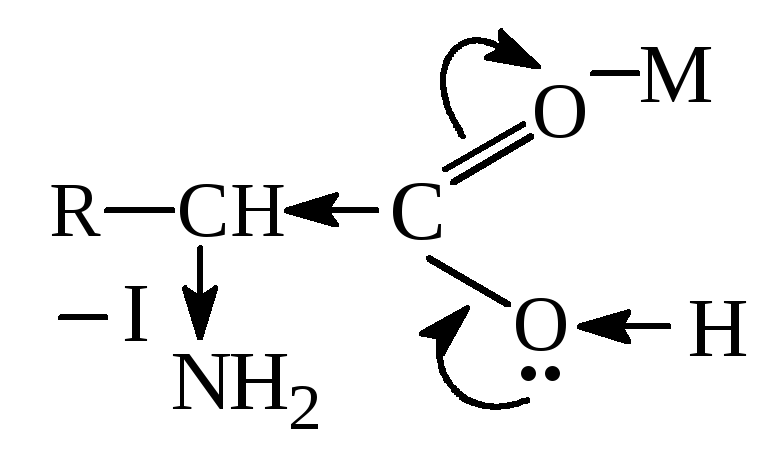
В лабораторных условиях АК легко декарбоксилируются в щелочной среде. В организме -АК декарбоксилируются под действием фермента декарбоксилазы:
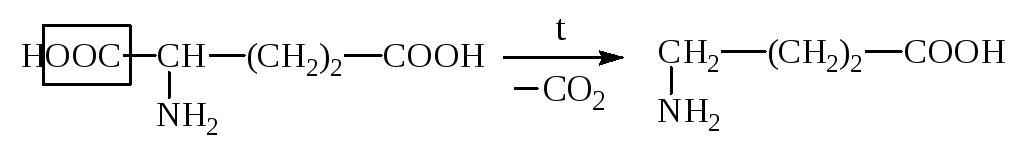
Глутаминовая к-та -Аминомасляная к-та, ГАМК
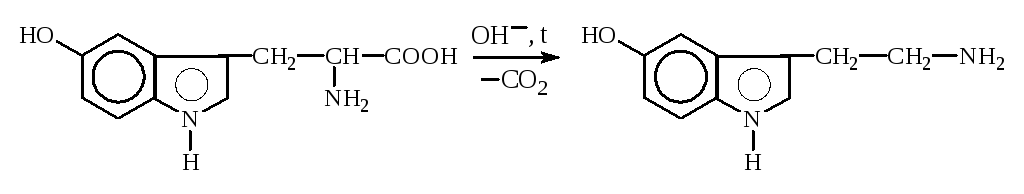
5-Окситриптофан 5-Окситриптамин,
серотонин
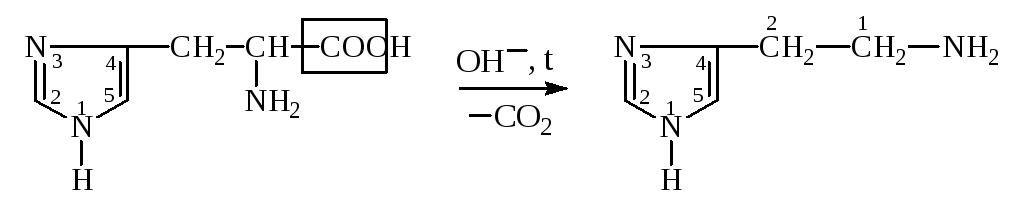
Гистидин, Гистамин,
-амино--[4(5)-имидазолил]- 2-имидозолиламиноэтан,
пропионовая к-та 4(5)-аминоэтилимидазол
Образующиеся амины имеют большое физиологическое значение и наз-ся биогенными аминами. Они участвуют в ряде р-ций обмена нервной и сердечно-сосудистой систем.
К биогенным аминам, образующимся из тирозина в процессе обмена веществ, относится группа катехоламинов: адреналин, норадреналин и дофамин:
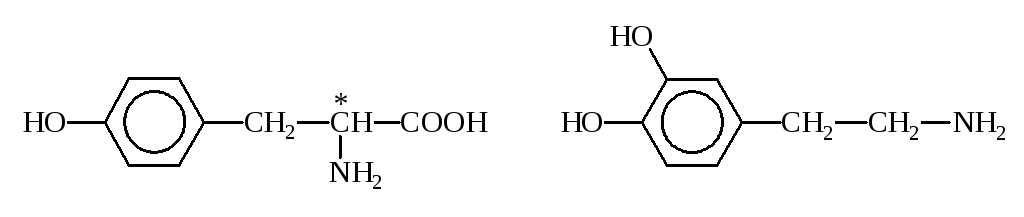
Тирозин Дофамин
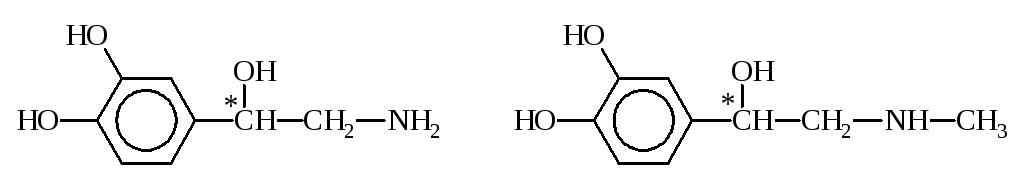
Норадреналин Адреналин
Дофамин, норадреналин и адреналин выполняют роль нейромедиаторов. Из тирозина синтезируются также пигменты кожи, глаз, волос.
Кроме р-ций декарбоксилирования в организме протекают под влиянием ферментов много строго специфических р-ций: переаминирования, трансаминирования и др.
Р-ции по радикалу
Все циклические АК, содержищие бензольное кольцо – триптофан, тирозин, фенилаланин – легко вступают в р-ции замещения по бензольному кольцу с На12, НО–NO2, HO–SO3H.
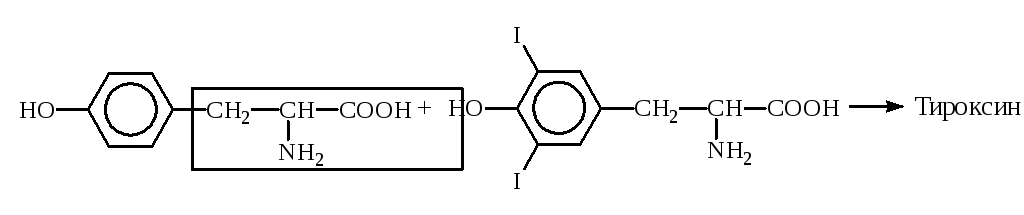
Путем йодирования тирозина в организме образуется гормон щитовидной железы тироксин:
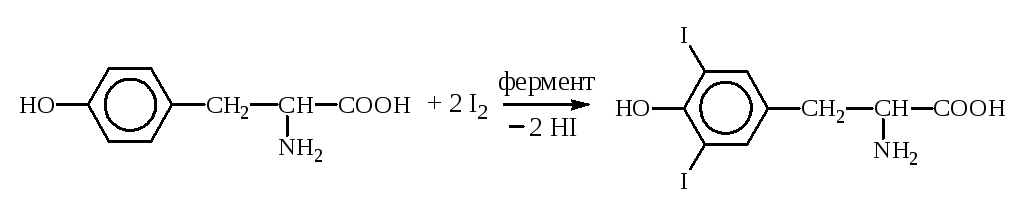
Тирозин Дийодтирозин
Качественная р-ция на ароматические АК – ксантопротеиновая – обусловлена нитрованием бензольного кольца с образованием нитросоединений желтого цвета. При добавлении к ним щелочи возникает оранжевое окрашивание:

Качественная р-ция на -АК
Это р-ция с нингидрином:
-AK
+ CO2 + R–CHO
Альдегид
Р-ция на присутствие серусодержащих АК
Цистеин Метионин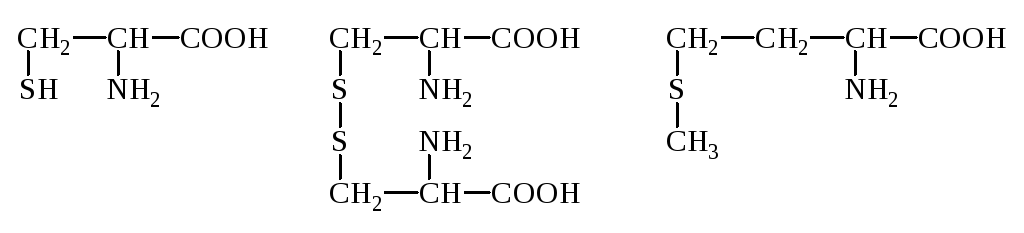
Цистин
Цистеин и цистин легко превращаются друг в друга за счет р-ции окисления-восстановления:
Цистеин
![]() Цистин + Н2О
Цистин + Н2О
Обмен серы в организме идет, в основном, за счет цистина и цистеина. Они обусловливают структуру белка, реактивность многих ферментов и гормонов. Качественной р-цией на серусодержащие АК является р-ция Фоля: