
Занятие 2 Мод2 Хим равновесие
.doc
![]()
Министерство здравоохранения и социального развития Российской Федерации
Государственное бюджетное образовательное учреждение высшего
профессионального образования
«Саратовский государственный медицинский университет
имени В.И. Разумовского» Министерства здравоохранения и социального
развития Российской Федерации
(ГБОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздравсоцразвития России)
Методические указания к лабораторно – практическому занятию
для студентов медицинских специальностей
Химическое равновесие
Дисциплина: общая химия.
I курс.
Очная форма обучения.
Длительность занятия: 90 минут.
Разработка составлена асс. Куликовой Л.Н.
2011 г
Цели
формирование у студентов представлений о факторах, влияющих на смещение равновесия биохимических процессов.
Исходные знания студентов:
Закон действующих масс. Принцип Ле-Шателье.
Студент должен знать: понятие «химическое равновесие». Термодинамические условия химического равновесия в изолированных и закрытых системах. Константа химического равновесия. Уравнения изотермы и изобары химических реакций.
Студент должен уметь: прогнозировать результаты физико-химических процессов, протекающих в живых системах, опираясь на теоретически положения, в зависимости от изменения температуры и давления (расчеты по уравнениям изотермы и изобары химической реакции).
План подготовки:
-
Ознакомиться с вопросами для подготовки к занятию.
Вопросы для подготовки к занятию
-
Химическое равновесие.
-
Обратимые и необратимые по направлению реакции.
-
Термодинамические условия равновесия в изолированных и закрытых системах.
-
Константа химического равновесия.
-
Уравнения изотермы и изобары химической реакции.
-
Осмыслить краткий теоретический материал (приложение 1) и текст лекции «Основные понятия термодинамики. Первое и второе начала термодинамики».
-
Если определённые участки лекции трудны для понимания, то необходимо обратиться к следующим учебникам:
|
№п/п |
Авторы |
Название |
Страницы |
|
1 |
Ершов Ю.А., Попков А.С., Берлянд А.С., Книжник А.З. |
Общая химия. Биофизическая химия. Химия биогенных элементов.- М.: Высш. шк.-2000.-560 с. |
32-41 |
|
2 |
Глинка Н.Л. |
Общая химия. - Л.: Химия.-1978.-720 с. |
184-201 |
|
3 |
Равич-Щербо М.И., Новиков В.В. |
Физическая и коллоидная химия.-М.: Высш. шк.-1975.-255 с. |
17-19 |
|
4 |
Ленский А.С. |
Введение в бионеорганическую и биофизическую химию.- М.: Высш. шк.-1989.-256 с. |
80-92 |
-
Ответить на вопросы для самоконтроля (приложение 2).
-
Выполнить тренировочный тест и проверить правильность выполнения по ключу (приложение 3).
-
Решить ситуационную задачу (приложение 4).
Приложение 1: Краткий теоретический материал
Химическое равновесие – это такое состояние системы, при котором скорости прямой и обратной реакций равны между собой.
В равновесии изменения изобарно-изотермического потенциала (∆G) и изохорно-изотермического потенциала (∆F) равны нулю.
Закон действующих масс:
скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в степенях их стехиометрических коэффициентов.
aA
+ bB ↔ сС + dD![]()
![]()
![]()
![]()
![]()
![]() (РDd
·PCc)
/(
РAa
·PBb)
(РDd
·PCc)
/(
РAa
·PBb)
а, b, c, d - стехиометрические коэффициенты
Константа равновесия может быть выражена не только через парциальные давления газообразных участников реакции, но и через молярные концентрации и мольные доли исходных веществ и продуктов реакции.
КР= КС (RT)∆n = Кχ (Pобщ) ∆n
КС – константа равновесия, выраженная через концентрации участников реакции
R- газовая постоянная, R=8,314 Дж/(моль К)
∆n-разность количеств вещества конечных и исходных газообразных участников реакции
Кχ– константа равновесия, выраженная через мольные доли участников реакции
Робщ – общее давление.
Направление химической реакции определяют по величине изобарно-изотермического потенциала:
ΔG<0 - протекает прямая реакция; самопроизвольный процесс;
ΔG=0, система находится в состоянии равновесия;
ΔG>0, протекает обратная реакция; несамопроизвольный процесс.
Рассчитывают ΔG по уравнению изотермы химической реакции:
ΔGх.р. = - RT ln Kp + RT ln (РDd ·PCc / РAa ·PBb)
R- газовая постоянная, R=8,314 Дж/(моль К).
Kp –константа равновесия
РD , РС - неравновесные давления газообразных продуктов реакции
РА , РB - неравновесные давления газообразных исходных веществ.
- RT ln Kp= ΔG0298, х.р.
Способы расчёта изобарно-изотермического потенциала:
1)
![]()
![]()
2)
![]()
![]() -
стандартное изменение энергии Гиббса
при образовании 1 моля вещества из
простых веществ (справочные данные).
-
стандартное изменение энергии Гиббса
при образовании 1 моля вещества из
простых веществ (справочные данные).
Принцип Ле- Шателье:
если на систему, находящуюся в состоянии равновесия подействовать извне, то система смещает равновесие в сторону противодействия внешнему воздействию.
Повышение температуры смещает равновесие в сторону протекания эндотермического процесса. Повышение давления - в сторону образования меньшего числа моль газообразных веществ.
Зависимость константы химического равновесия от температуры при постоянном давлении описывает уравнение изобары Вант-Гоффа:
дифференциальная форма уравнения изобары
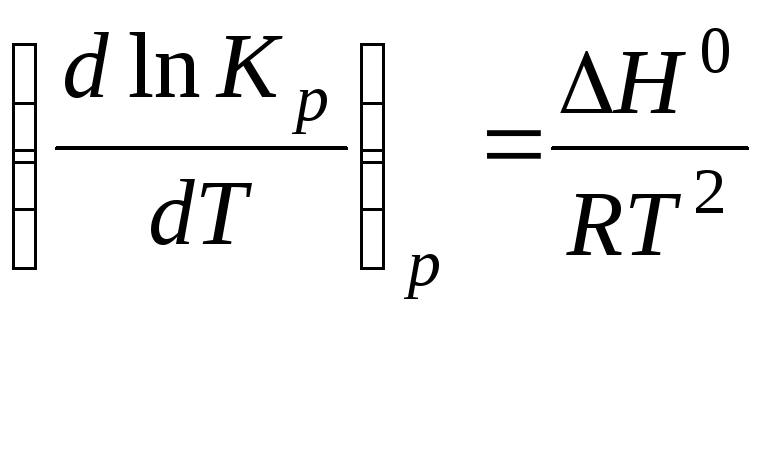 ,
,
где R- газовая постоянная, R=8,314 Дж/(моль К);
Kp – константа равновесия, выраженная через давления;
Т – температура;
∆Н – тепловой эффект реакции.
интегральная форма уравнения изобары
![]()
К1, К2 –константы химического равновесия реакции при температурах Т1 и Т2.
Зависимость константы химического равновесия от давления описывает уравнение Планка – Ван – Лаара:
![]()
Кх – константа химического равновесия, выраженная через мольные доли;
Р – давление;
∆n – изменение числа моль газообразных участников реакции.
Приложение 2: Вопросы для самоконтроля
-
Что называют химическим равновесием?
-
Какие реакции называют обратимыми по направлению реакции?
-
Какие реакции называют необратимыми по направлению реакции?
-
Назовите термодинамические условия равновесия в изолированных и закрытых системах.
-
Какими способами рассчитывают ∆G? Приведите расчётные формулы.
-
Через какие характеристики системы можно выразить константу равновесия?
-
Запишите уравнение изотермы и изобары химической реакции.
Приложение 3: Тренировочный тест
-
В системе 2SО2 + O2 —> 2SO3 исходные концентрации SО2 и О2 были соответственно равны 0,03 и 0,015 моль/л. В момент равновесия [SО2] стала равной 0,01моль/л. Константа равновесия равна
а) 180
б)260
в) 525
г) 800
2. При 508°С константа скорости реакции Н2(г) + J2(г) —>2HJ(г) равна 0,16 л/(моль·мин). Исходные концентрации Н2 и J2 соответственно равны 0,04 и 0,05 моль/ л. Начальная скорость реакции составляет_________ моль/( л·мин).
а) 3,2·10-4
б) 1,92·10-4
в) 9,6 ·10-5
г) 2,8 ·10-5
3. В системе 2SО2(г) + O2(г) —> 2SO3(г) исходные концентрации SО2 и О2 были соответственно равны 0,03 и 0,015 моль/л. В момент равновесия [SО2] стала равной 0,01, а равновесная [SО3] _____моль/ л
а) 0,005
б) 0,01
в) 0,02
г) 0,05
4. Если в системе 2Са(к) + О2(г) —> 2СаО(к) увеличить давление в 2 раза, то скорость прямой реакции
а) возрастет в 4 раза
б) возрастет в 2 раза
в) понизится в 2 раза
г) не изменится
5. Исходная концентрация СО и Сl2 в системе СО + Сl2 —>СОСl2 были равны 0,3 и 0,2 моль/л. Если концентрацию СО повысить до 0,6, а Сl2 до 1,2 моль/л, то скорость реакции между ними увеличится в
а) 2 раза
б) 6 раз
в)12 раз
г) 24 раза
Эталоны ответов к тесту: 1а, 2а, 3а, 4б, 5в
Приложение 4: Ситуационные задачи.
-
Константа равновесия системы СО2(г) + Н2(г) —> CO(г) + Н2О(г) равна 1. В начальный момент [СО2] и [Н2] были соответственно равны 0,2 и 0,8 моль/ дм3. Концентрация [СО] равн. Составляет ______(моль/ дм3)
-
Запишите выражения КР для реакций:
1. CO + H2 = С граф +H2O газ
2. 2CI2 + 2H2O газ = 4HCI(г) + О2
Как связаны КР и КС для этих реакций?
3) Железо и водяной пар реагируют по уравнению:
Fe тв + H2O газ = FeО тв + H2 газ. При температуре 1298К и Робщ = 1атм равновесие наблюдается при РH2 = 0, 562 атм. и Р H2O = 0,438 атм. При температуре 1173К равновесие наблюдается при Р(H2)= 0,592 атм., Р (H2O) = 0,408 атм. Рассчитайте средний тепловой эффект реакции в этом интервале температур.
4) При 1000К для реакции SO2 + NO2 = SO3 +NO; Кр = 7,6. В каком направлении будет протекать реакция при РSO2 = 1 атм.; PNO2 = 6 атм.; PSO3 = 2 атм.; PNO= 3 атм.
5) Напишите уравнение, описывающее влияние давления на химическое равновесие. Приведите примеры реакций, на равновесие которых влияет давление и не влияет.
6) Как влияет общее давление на равновесие: FeCO3 кр = FeO кр + CO2?
7) Для реакции N2+3H2 = 2NH3 при 6230К КР = 7,23 · 10 -14 (Н/м2)-2. В каком направлении будет протекать процесс при: РN2 = PH2 = PNH3 = 1,0132 · 105 Н/м2.
8) Как нужно изменить условия проведения реакции (Т и Р) CO + H2O(газ) = CO2 +H2, чтобы сдвинуть равновесие в сторону продуктов, если ΔН0800К = -36994 Дж/моль.
9). Для реакции: 2CO + 2H2 = CH4 + CO2 при 1000К КР = 2,57 · 10-8 (Н/м)-2. Определить, в каком направлении будет протекать реакция, если: РСО = 1,0132 · 104; РН2 = 2, 0264 · 104; РСН4 = 2, 0264 · 104; РСО2 = 6, 0792 · 104 Н/м2
10). Для реакции СТВ + 2Н2 Г = СН4 г, при 973К КР = 0, 1924 · 10-5 Н/м2, а при 1033К КР = 0,1159 · 10-5. Вычислить средний тепловой эффект реакции в этом интервале температур.
11) Что требуется сделать для для смещения равновесия гомогенной химической реакции 2НI 2H2 + O2, ΔH < 0, в сторону продуктов?
-
Как увеличить выход продуктов реакции 2Pb(NO3)2 (тв) 2 PbO(тв)+4 NO2(г)+О2 (г), ΔH > 0.
-
Запишите уравнение константы равновесия гетерогенной химической реакции 2H2S(г) + SO2 (г) 2S(к) + 2H2O(г) К = [H2O]2 / [H2S]2 · [SO2]
Лабораторная работа
Влияние изменения концентраций на химическое равновесие.
Воздействие концентраций на равновесие изучим на примере реакции хлорида железа (+3) с роданидом калия. м.
Обычно полное уравнение реакции представляют так:
F
 eCl3
+ 3KSCN
Fe(SCN)3
+ 3KCl.
eCl3
+ 3KSCN
Fe(SCN)3
+ 3KCl.
Этому молекулярному уравнению можно сопоставить разные ионные.
Если считать, что хлорид железа полностью распадается на ионы, а роданид железа совсем не распадается, получается следующее сокращённое ионное уравнение:
F
 e3+
+ 3SCN–
Fe(SCN)3.
e3+
+ 3SCN–
Fe(SCN)3.
Частичной диссоциации обеих солей железа отвечают другие ионные уравнения, например, такое:
F
 eCl2+
+ 2SCN–
Fe(SCN)2+
+ Cl–.
eCl2+
+ 2SCN–
Fe(SCN)2+
+ Cl–.
Запишите стандартное выражение для константы данного равновесия.
В пробирку налейте 10 мл раствора KSCN и прибавьте 1–2 капли разбавленного раствора FeCl3. Должен получиться слабоокрашенный раствор. Его разделите на 4 равные порции.
К первой порции прибавьте концентрированный раствор FeCl3. Во вторую порцию всыпьте ложечку сухого KSCN. К третьей порции добавьте ложечку сухого KCl или влейте 1–2 мл концентрированной HСl. Четвёртая пробирка предназначена для сравнения (исходное состояние).
Единственным ярко окрашенным веществом в системе является соединение ионов железа и роданида.
Проанализируйте изменения цвета в порциях 1-3 с точки зрения принципа Ле-Шателье. Какой из вариантов ионного уравнения противоречит опыту?
Сделайте выводы о проделанной работе.
