
- •Кафедра «Моделирование систем и информационные технологии» окислительно-восстановительные реакции Методические указания к лабораторным работам по курсу
- •Введение
- •1.Окислительно-восстановительные реакции. Основные понятия и определения
- •2.Важнейшие восстановители и окислители
- •2.1 Восстановители
- •2.2 Окислители.
- •2) Кислоты и их соли.
- •2.3. Окислительно-восстановительная двойственность
- •3.Составление уравнений окислительно-восстановительных реакций методом электронного баланса
- •4. Экспериментальная часть
- •Оглавление
- •Светлана Борисовна Белова
2.Важнейшие восстановители и окислители
2.1 Восстановители
1) Среди элементарных веществ – активные металлы и некоторые неметаллы.
К отдаче электронов склонны атомы элементов, у которых во внешнем электронном слое содержится малое число электронов.
При отдаче этих электронов устойчивый внутренний электронный слой становится внешним.
(Mg
- 2e:
2![]() - внутренний
слой стал внешним)
- внутренний
слой стал внешним)
8 электронов образуют устойчивый октет.
Следовательно, восстановителями являются:
активные металлы: щелочные, щелочноземельные, Al, Zn, Fe и другие
![]()
некоторые неметаллы:
 ,C
(в виде угля или кокса), P,
Si
,C
(в виде угля или кокса), P,
Si
![]()
![]() .
.
2)
Бескислородные
кислоты (HCl,
HBr,
![]() )
и их соли.
)
и их соли.
Носителями восстановительной функции являются анионы. Окисляясь, они образуют элементарные вещества.
В ряду галогенид–ионов
восстановительные свойства возрастают
от
![]() до
до![]() .
.
![]() .
.
3) Гидриды щелочных
и щелочноземельных металлов,
содержащие ион
![]() .
.
Окисляются до
![]() .
.
![]() .
.
4) Ионы металлов,
находящиеся в низшей степени окисления
(![]() и другие).
и другие).
Способны увеличивать с.о.. при взаимодействии с окислителем.
![]() .
.
2.2 Окислители.
1) Среди элементарных веществ – типичные неметаллы.
К приему электронов склонны атомы элементов, которым не хватает лишь небольшого числа электронов для образования устойчивого внешнего электронного слоя.
Это типичные
неметаллы: галогены в свободном виде
![]() .
.
Галогены
восстанавливаются до -1: ![]() .
.
Кислород
восстанавливается до -2: ![]() .
.
2) Кислоты и их соли.
Важнейшие соли:
 –дихромат калия.
Выступает в роли окислителя в кислой
среде. Окислителем служит ион –
–дихромат калия.
Выступает в роли окислителя в кислой
среде. Окислителем служит ион –
 ,
восстанавливающийся доCr+3.
,
восстанавливающийся доCr+3.
 –перманганат калия.
–перманганат калия.
Восстанавливается до:

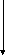

Кислая среда Нейтральная и слабая Щелочная среда
+2 щелочная среда +6
+4
![]()
![]()
![]()
|
Важнейшие кислоты |
Элемент-окислитель |
Уравнение полуреакции восстановления |
|
|
N |
|
|
|
H |
|
|
Разбавленная
|
H |
|
|
Концентрированная
|
S |
|
|
Кислород-содержащие кислоты галогенов и их соли
(пример:
|
Cl |
|
Состав продуктов
восстановления
![]() зависит от активности восстановителя
и концентрации кислоты; чем активнее
восстановитель и более разбавлена
кислота, тем глубже протекает восстановление
азота:
зависит от активности восстановителя
и концентрации кислоты; чем активнее
восстановитель и более разбавлена
кислота, тем глубже протекает восстановление
азота:
Продукты
восстановления
![]() :
:
![]()
 концентрация
концентрация
![]()
![]()

![]()
![]()
![]()
![]()
![]() активность
восстановителя
активность
восстановителя
Состав продуктов
восстановления
![]() определяется главным образом активностью
восстановителя:
определяется главным образом активностью
восстановителя:
Продукты
восстановления
![]()


![]()
малоактивные металлы (Cu, Sb), акт. Ме
НВr,
некоторые неметаллы (С)
+4 0 -2
S+4O2
S0
![]() -2
-2
3) Ионы металлов
в высшей степени окисления
(![]() ).
).
Степень окисленности уменьшается при взаимодействии с восстановителем.
![]() .
.
4) Н в с.о.. +1 выступает как окислитель главным образом в растворах кислот (при взаимодействии с Ме, стоящими в ряду напряжений до водорода)
![]() .
.
