
Лекция_4_ГИ_М_2014
.pdf
Рекомбиназная векторная система:
ТЭ в N. excelsior
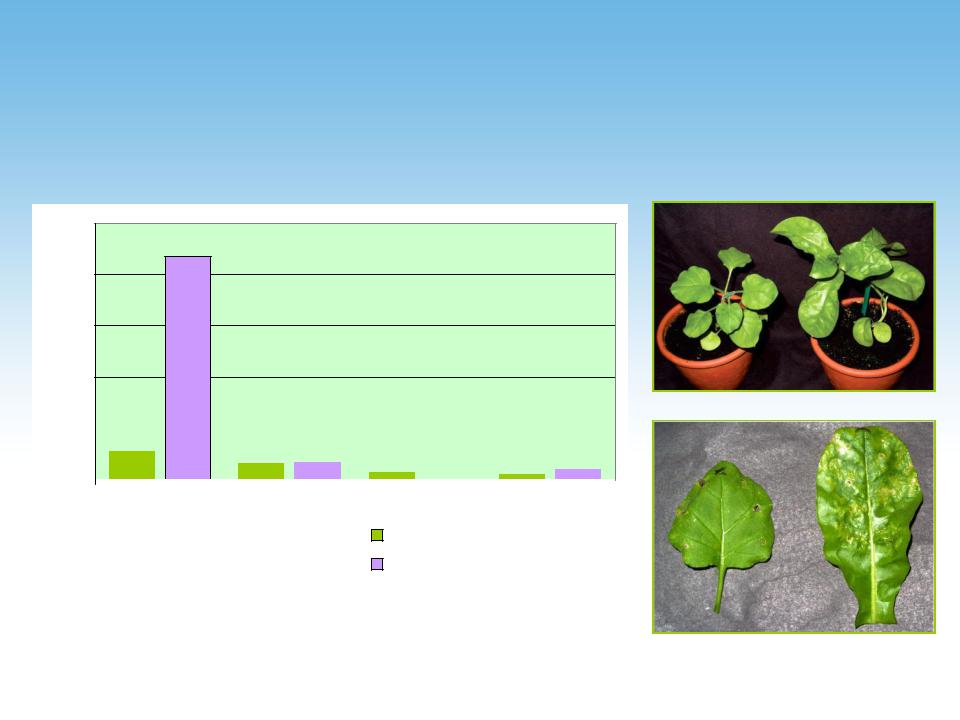
Среднее количество GFP, которое можно получить из одного растения
GFP, мг
25
21,75
20
15
10
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2,77 |
1,54 |
1,69 |
|
|
0,69 |
|
|
|
|
|
|
0,99 |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
0 |
|
|
|
|
|
0,03 |
|
0,51 |
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
1 |
|
|
|
2 |
|
|
|
|
|
|
3 |
|
|
|
|
4 |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
1 |
- N. excelsior; 2 - N. cavicola; |
|
35S система |
|
|
|
|
|
|
|
|
|||||||||||||
3 |
- N. exigua; 4 - N. benthamiana |
|
модульная рекомб. система |
|||||||||||||||||||||
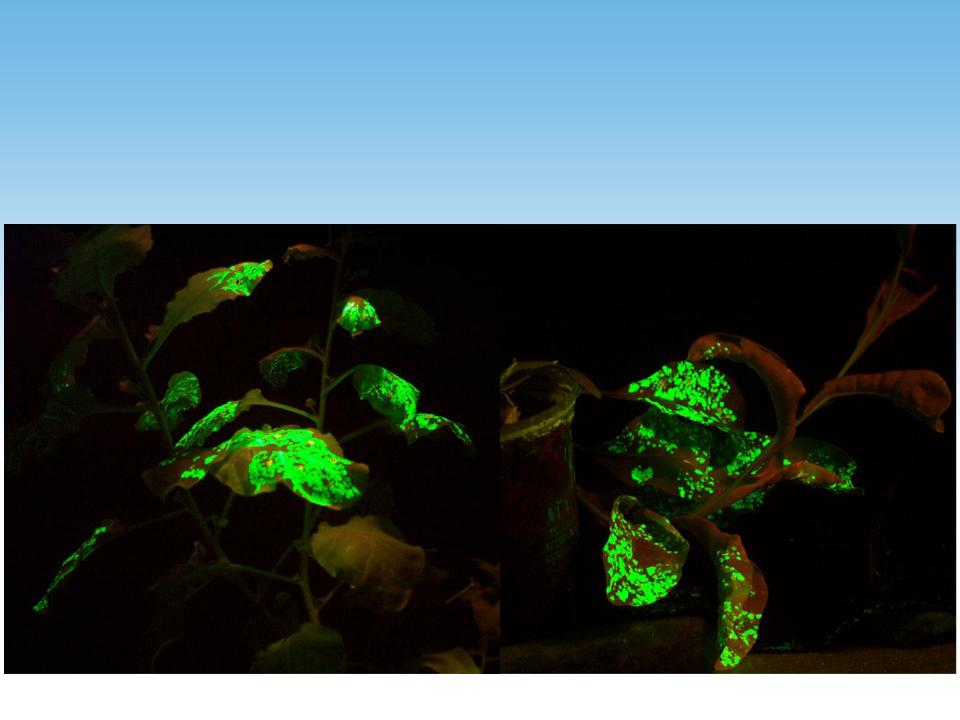
‘Magnifection’ - новая экспрессионная платформа, разработанная Icon Genetics

Примеры фармацевтических белков, полученных с помощью ТЭ
Белок |
Растение-хозяин |
Уровень накопления |
|
|
|
Single-chain Fv antibody (scFvT84.66) |
N. tabacum |
5 mg/kg FW |
|
|
|
T84.66/GS8 diabody |
N. tabacum |
0.02 – 0.2 % TSP |
|
|
|
GFP |
N. benthamiana |
4 – 40 % TSP |
|
N. excelsior |
2 – > 50 % TSP |
|
|
|
Interferon- |
N. benthamiana |
~10 % TSP |
a2B |
|
|
|
|
|
hGH |
N. benthamiana |
10 % TSP |
|
|
|
Y. pestis F1, V, and F1-V |
N. benthamiana |
1-2 mg/g FW |
antigens |
|
|
|
|
|
Full-size mAbs of the IgG class |
N. benthamiana |
500 mg/kg |
|
|
|
Hepatitis B core antigen (HBc) |
N. benthamiana |
7.14 % TSP |
|
|
|
Ag85B antigen |
N. benthamiana |
200-800 mg/kg FW |
|
|
|
ESAT6 antigen |
N. benthamiana |
2 mg/kg FW |
|
|
|
Aprotinin |
N. benthamiana |
1 mg/g FW |
|
|
|
Chicken anemia virus proteins (VP) fused with GFP |
N. benthamiana |
1.2 – 2.6 % TSP |
|
|
|
Highly-labile Ll protein of canine oral papillomavirus |
N. tabacum |
0.3 % TSP |
(COPV Ll) |
|
|
|
|
|
Human fibroblast growth factor 8b |
N. tabacum |
4 % TSP |
|
|
|
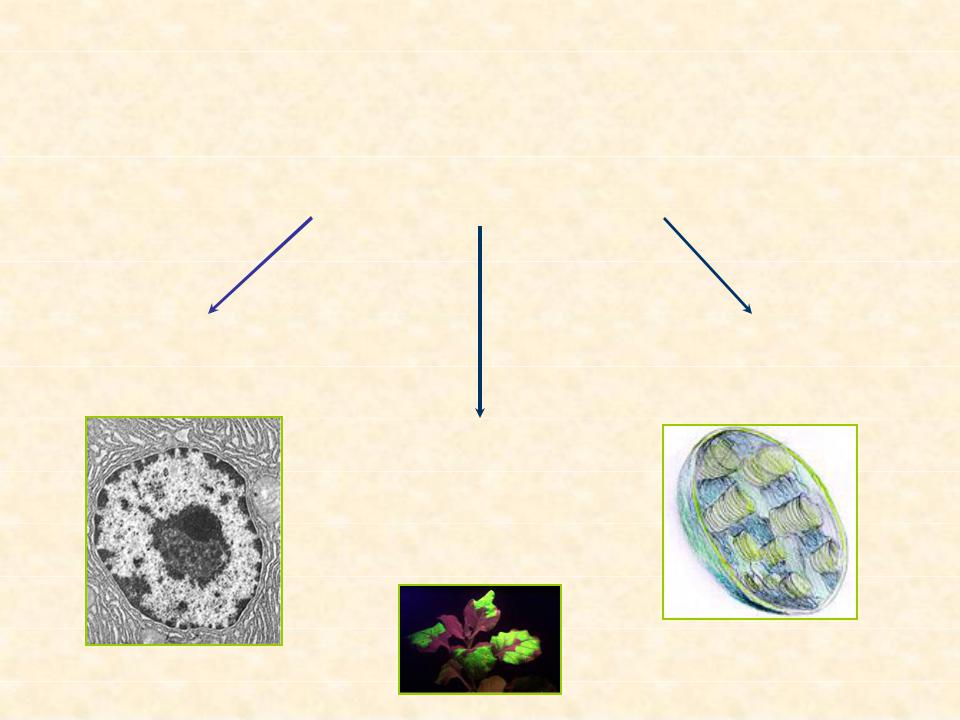
Растительные системы для экспрессии рекомбинантных белков
Ядерные |
Пластомные |
|
трансформанты |
||
трансформанты |
||
|
Системы для транзиентной экспрессии

Сравнение растительных систем для получения рекомбинантных белков
|
Продуктив- |
Возможност |
Время до |
Экологическ |
|
ность |
ь |
получения |
ий риск |
|
|
масштабиро |
продукта |
|
|
|
-вания |
|
|
|
|
|
|
|
Транзиентна |
Средняя / |
Средняя |
Короткое |
Низкий |
я экспрессия |
Высокая |
|
(дни) |
|
|
|
|
|
|
Ядерная |
Низкая |
Высокая |
Среднее |
Достаточный |
трансфор- |
|
|
(месяцы) |
|
мация |
|
|
|
|
|
|
|
|
|
Пластомная |
Средняя / |
Высокая |
Долгое (годы) |
Умеренный |
трансфор- |
Высокая |
|
|
|
мация |
|
|
|
|
|
|
|
|
|
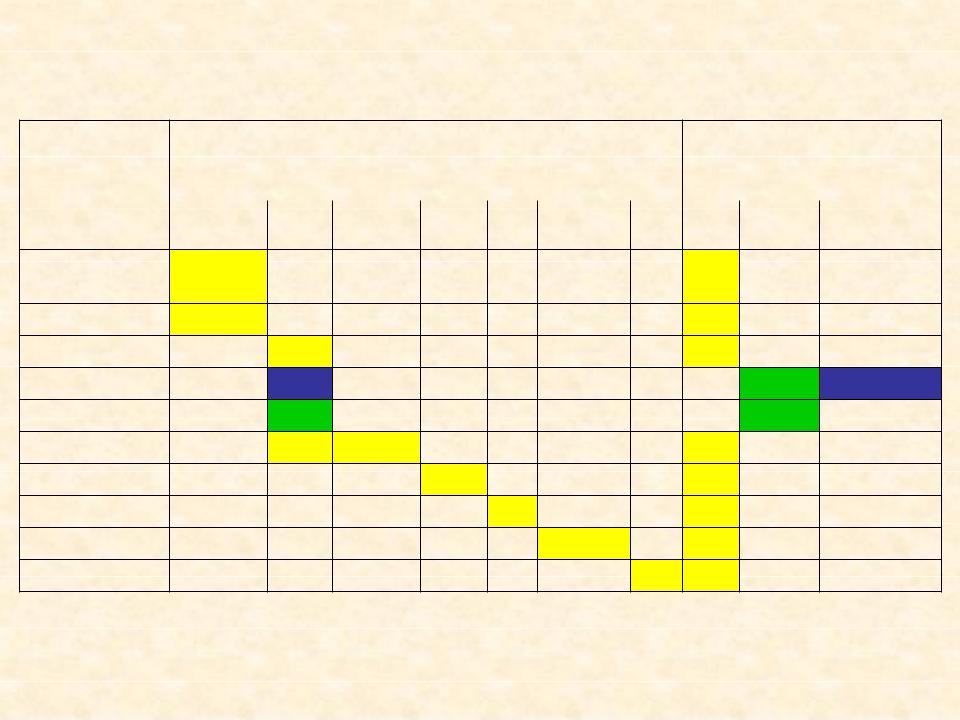
Производство фармацевтических белков на основе генетически-модифицированных растений
|
Системы наработки рекомбинантного белка |
Системы экспрессии |
|
КОМПАНИИ |
|
|
|
|
|
|
|
|
суспензии табак люцерна ряска мох A.thaliana рис |
ядро хлоро |
агроинфильт |
|
|
пласты |
рация |
Dow
AgroScience
Protalix
Planet Biotech
Bayer
Chlorogen
Medicago, Inc.
Biolex
Greenovation
Cobento
Ventia
Sourrouille C. et al., Recombinant Proteins From Plants. 2009.
