
- •Наноэлектроника
- •Основные идеи и принципы квантовой механики
- •Основы квантовой механики
- •Основы квантовой механики
- •Основы квантовой механики
- •Элементы квантовой теории твердых тел
- •Квантовые ямы в полупроводниковых гетероструктурах
- •Полупроводниковые лазеры
- •КВАНТОВЫЕ КАСКАДНЫЕ ЛАЗЕРЫ
- •Квантовый размерный эффект в кремниевых нанокристаллах
- •Одноэлектроника

Основы квантовой механики
Соотношение неопределенностей
Гейзенберга
Для координаты и импульса: x px h
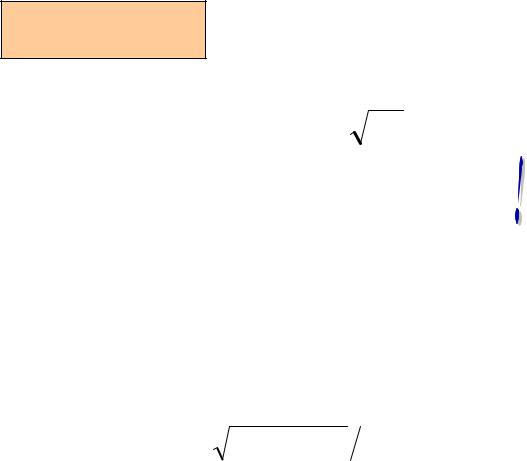
! Размер волны не измерить точно на длинах: x h / px DB
|
|
|
|
Для энергии и времени: |
E t h |
|
|
! Энергию волны не измерить точно на временах, меньше |
|||
периода волны : |
t h / E 1/ T |
||
E E0 E |
! Энергия частицы-волны не равна 0, |
||
даже если ее энергия покоя E0 010! |
|||
Основы квантовой механики
Волновая функция и уравнение Шредингера
Состояние частицы описывается волновой функцией:
(x, y, z,t)
Волновая функция имеет комплексный характер: Aei ,
А – амлитуда, φ - фаза , |
i |
|
|
|
|
|
i |
|
|
1 |
||
|
e |
cos |
isin , |
|
|
|||||||
Вероятность w найти частицу |
w |
|
|
|
2 |
V A2 V |
||||||
|
|
|||||||||||
в объеме V : |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Уравнение Шредингера (для частицы массой m в
стационарном поле с потенциальной энергией U(x):
|
|
|
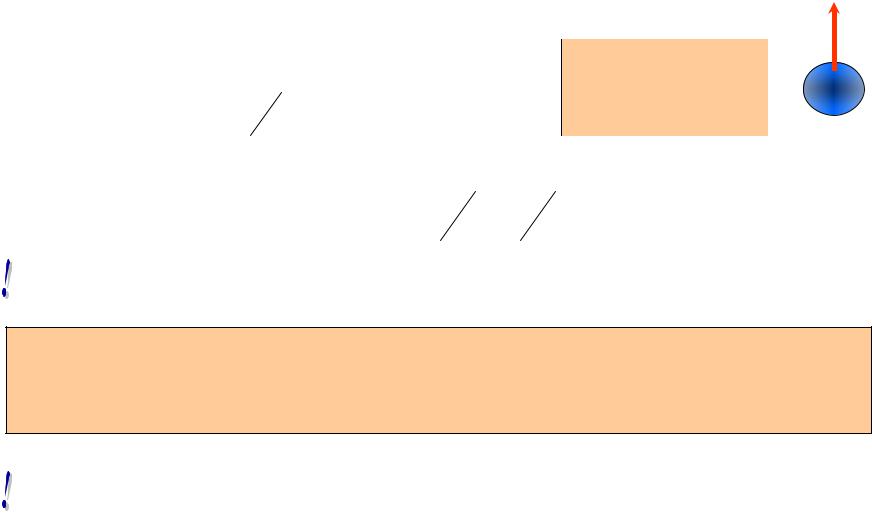
Если U(x) =const, то получим |
|
|
h2 |
|||
|
уравнение колебаний (!) : |
|
||
|
|
U (x) E 0 |
2 0 |
|
2m |
|
|||
|
|
|
2m E U h |
11 |
|
|
|
||
Основы квантовой механики Спин частицы и принцип Паули
Многие частицы обладают собственным моментом |
S |
|||||||||
количества движения - спином . |
|
|
|
|
|
|
|
|||
|
|
|
1 |
h |
|
|||||
Для электрона его значение равно: |
|
S |
|
|
||||||
или просто S 12 , в единицах . |
|
2 |
4 |
|
|
|
||||
|
|
|
|
|||||||
Проекция спина электрона на некоторую ось z |
|
|||||||||
принимает значения: Sz 1 |
2 |
; 1 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Спину соответствует собственный магнитный момент, а значит появляется добавочная энергия частицы в магнитном поле !
Принцип Паули: в атоме в каждом состоянии с
квантовыми числами (n,l,m) может находиться не более 2-х электронов с противоположными проекциями спина.
Принцип Паули позволяет объяснить внутреннюю структуру атомов и обосновать построение периодической системы 12 элементов Д.И.Менделеева.
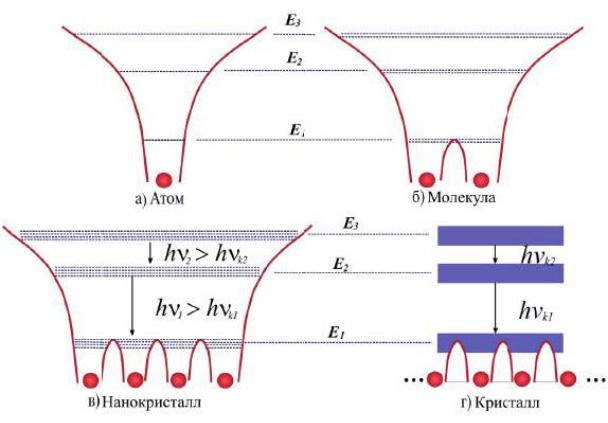
Электронная структура
Расположение уровней в атоме (а), молекуле (б), нанокристалле (в), кристалле (г)
13
