
H-31_vms_lections (ВМС)
.pdf
Важным эффектом введения хлора является увеличение адгезии, что позволяет использовать хлорированные продукты в типографских красках.
Сульфохлорирование осуществляют хлором в присутствии диоксида серы. Реакция протекает по следующей схеме:
|
|
CH2 |
|
CH2 |
|
|
+ SO2 +Cl2 |
|
- HCl |
|
CH2 |
|
|
CH |
|
+ PbO |
- PbCl2 |
|
|
|||||||||||
|
|
|
|
|
|
|
(а) |
|
|
|
|
(б) |
|
|
|
|||||||||||||||
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
SO2Cl |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
SO2 |
O |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
SO2 |
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
CH2 |
|
|
CH2 |
|
|
|
|
|
превращение |
(а) |
даже |
позволяет |
провести |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
Полимераналогичное |
|||||||||||||||||||||||||||
межмолекулярную реакцию (б) сшивания для улучшения свойств полимера. Сульфохлорирование полиэтилена позволяет получать из него эластичный продукт со
свойствами каучука, который можно затем обрабатывать оксидами металлов для повышения прочности и теплостойкости.
Хлорированные и сульфохлорированные эластомеры очень устойчивы к действию озона из-за отсутствия двойных связей.
Хлорирование ненасыщенных эластомеров позволяет повысить их химическую стойкость и адгезию к металлическим поверхностям.
Особое значение бромирование и хлорирование имеет для бутилкаучука. Бутилкаучук
– сополимер изобутилена с небольшим количеством (1-5%) изопрена.
~ |
|
|
|
CH3 |
|
CH3 |
|
|
|
|
|
|
|
CH3 |
|
|
|
CH3 |
|
CH3 |
|
|
|
|
~ |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
C |
|
CH2 |
|
C |
|
CH2 |
|
|
|
|
|
CH2 |
|
C |
|
CH |
|
CH2 |
|
|
|
|
C |
|
CH2 |
|
C |
|
CH2 |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
CH |
|
|
|
|
|
|||||||||||
|
|
3 |
|
|
|
|
|
|
|
|
|
|
n |
|
|
|
|
|
|
|
|
|
|
|
3 |
|
3 |
|
|
|
|
m |
||||||||||
Из-за низкой степени ненасыщенности число возможных поперечных связей в бутилкаучуке весьма ограничено, поэтому вулканизация его является длительным процессом, протекает в присутствии более активных ускорителей и при более высоких температурах, чем для других эластомеров. Для увеличения скорости вулканизации, улучшения адгезионных свойств и совместимости с другими каучуками, а также для повышения износостойкости и стойкости к тепловому старению бутилкаучук подвергают галогенированию. Галогенирование бутилкаучука, т.е. хлорирование или бромирование приводит к присоединению атомов галогенов главным образом в α-положении к двойным связям изопреновых звеньев, благодаря чему аллильные атомы галогенов очень подвижны и способны участвовать в вулканизации.
|
|
|
|
CH |
|
CH |
|
|
|
|
|
|
|
CH |
|
|
|
CH3 |
|
CH |
|
|
|
|
|
|||||||||||||||||||
~ |
3 |
|
3 |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
~ |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
C |
|
CH2 |
|
C |
|
CH2 |
|
|
|
|
|
CH2 |
|
C |
|
CH |
|
CH2 |
|
|
|
|
|
C |
|
CH2 |
|
C |
|
CH2 |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
CH3 |
|
|
|
|
n |
|
|
|
|
|
Br |
|
|
|
CH3 |
|
CH3 |
|
|
|
|
m |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Внутримолекулярные превращения, могут сопровождаться образованием циклов, что приводит к изменению структуры, а часто и длины макромолекул. Так, теплостойкий полимер с полупроводниковыми свойствами образуется при нагревании полиакрилнитрила при 200°С:
http://www.mitht.org
|
|
|
CH |
CH2 |
CH |
|
|
CH |
CH |
|
|
|
|||||||||
|
|
|
2 |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
||
CH |
|
CH |
|
|
CH |
|
|
to |
CH |
CH |
|
CH |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
N C |
|
|
N C |
|
|
N |
C |
C |
|
C |
|
|||||||
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
N |
|
N Полученный |
циклический |
|
полимер с сопряженными связями применяют для производства волокон и пленок, устойчивых до 800°С.
При нагревании диеновых эластомеров в присутствии кислот или хлоридов металлов переменной валентности протекает внутримолекулярная циклизация с образованием шестичленных колец. При этом эластичный полимер теряет свое основное качество и становится твердым и хрупким:
~ СH2 |
|
СH3 |
|
|
|
|
|
|
|
|
|
~ СH2 |
|
СH3 |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
С |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
СH2 ~ |
|
+ H |
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
СH2 ~ |
|
|
|
|||||||
СH |
|
СH |
|
|
|
|
|
СH2 |
|
СH |
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СH |
|
|
|
|
|
|
|
|
СH3 |
|
|
|
|
|
|
|
СH2 |
|
С |
|
|
|
|
|
СH |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
2 |
С |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|||||||||||||
|
|
|
СH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СH2 |
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
~ СH2 |
|
|
|
|
СH3 |
|
|
|
|
|
|
~ |
СH2 |
|
|
|
СH3 |
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С |
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
С |
|
|
|
|
|
|
|
|
|
_ H + |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СH2 ~ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СH2 ~ |
|||||||
|
|
|
|
|
СH |
|
|
|
СH |
|
|
|
|
|
|
|
|
|
СH |
|
|
С |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
СH2 |
|
|
С |
|
|
СH |
||||
|
|
|
|
|
СH2 |
|
|
|
С |
|
|
СH3 |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|||||||||
|
|
|
|
|
|
|
|
|
СH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СH2 |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
1.2. Межмолекулярные реакции полимеров. |
||||||||||||||||||||||||||
Межмолекулярные реакции по характеру изменений свойств исходных полимеров резко отличаются от полимераналогичных превращений. В последних сильно изменяется химическая природа функциональных групп в макромолекулах, однако сами макромолекулы остаются самостоятельно существующими структурными элементами полимера. Полимер не теряет способности к растворению, к переходу в вязкотекучее состояние при повышении температуры. Межмолекулярные реакции принципиально меняют характер поведения макромолекул полимера. Они могут происходить как при химическом взаимодействии функциональных групп разных макромолекул друг с другом, так и при взаимодействии низкомолекулярных веществ одновременно с двумя, тремя или более макромолекулами полимера. В результате исходные макромолекулы оказываются химически связанными друг с другом, или сшитыми, и образуется единая трехмерная сетчатая структура полимера. При этом, как правило, резко повышаются прочностные и динамические свойства полимера, теряется способность к растворению. Теряет смысл и само понятие макромолекулы, т.к. теперь свойства полимера могут быть описаны с помощью свойств отрезков макромолекул между узлами образовавшейся сетчатой структуры. Схематично реакцию образования сшитого полимера можно представить следующим образом:
http://www.mitht.org
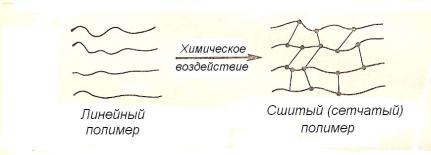
Химические связи, возникающие между исходными макромолекулами, называются поперечными связями. Звенья макромолекул, участвующие в образовании поперечных связей, называются узлами сетки. Участки одной макромолекулы между двумя соседними узлами называются цепями сетки. Как видно из схемы, концы макромолекул, ограниченные только одним сшитым звеном, отличаются от отрезков цепей внутри сетки, ограниченных двумя сшитыми звеньями. Первые называются свободными концами. При механических воздействиях на сетку напряжения распределяются между отрезками цепей, а свободные концы не несут нагрузки и составляют так называемую неактивную часть сетки.
В сшитом полимере понятием молекулярная масса обозначают величину молекулярной массы отрезка макромолекулы между узлами сетки. Если сшивание макромолекул протекает статистически, то принимают, что средняя молекулярная масса отрезка является величиной постоянной для данной степени сшивания. Зная исходную среднюю молекулярную массу полимера (Мо) и молекулярную массу отрезка цепи после сшивания (Мс), можно рассчитать индекс сшивания (γ), который является характеристикой степени сшивания полимера: γ = Мо/Мс, так как определяет число сшитых звеньев на одной исходной макромолекуле полимера. Чем больше число сшитых звеньев, тем более твердым и жестким становится полимер, тем более он термостоек и, как правило, прочен.
Образование трехмерных сшитых структур наиболее широко используется при производстве изделий из высокоэластичных материалов – каучуков или эластомеров. Эти полимеры обладают низкими механическими свойствами в несшитом состоянии, которые еще более снижаются при повышении температуры. Сшивание макромолекул в единую трехмерную пространственную структуру (вулканизация каучуков) позволяет ликвидировать оба этих недостатка, резко расширить температурные пределы эксплуатации каучуков и получить целый ряд других ценных свойств, присущих техническим резинам. Поэтому открытие в 1839 году американцем Ч. Гудьиром процесса вулканизации не только послужило мощным толчком к развитию резиновой промышленности, но и стало одним из наиболее значимых событий в развитии науки о полимерах. В ходе многочисленных, но несистематических опытов Гудьир установил, что каучук после нагревания с серой в присутствии соединений свинца превращается в прочный неклейкий и термически стойкий эластичный материал.
Со времени открытия вулканизации технические приемы этого процесса существенно изменились. Наиболее важным усовершенствованием процесса вулканизации каучука серой явилось введение в состав вулканизующей группы ускорителей и активаторов. Их применение позволило ускорить вулканизацию, уменьшить количество серы в смеси и резко улучшить качество резины.
Процесс вулканизации осуществляется нагреванием смеси каучука с серой, ускорителями и активаторами. В результате сложного комплекса химических превращений линейные макромолекулы каучука сшиваются фрагментами молекул серы, ускорителей. Под влиянием ускорителей молекула серы (S8) распадается на свободные радикалы или на ионы. Активные фрагменты серы реагируют с молекулами каучука:
http://www.mitht.org

|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
||||||
~ CH2 |
|
|
|
|
|
|
|
|
|
|
CH2 ~ |
|
|
|
|
|
~ CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
CH ~ |
|||||||
|
|
|
C |
|
|
|
CH |
|
|
|
|
|
|
|
|
|
C |
|
|
|
CH |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
+ S* |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
x |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
x |
~ CH2 |
|
|
C |
|
|
CH |
|
|
CH2 ~ |
|
|
|
|
|
~ CH2 |
|
C |
|
|
CH |
|
|
|
|
CH ~ |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
или |
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
Sx~ |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
~ CH2 |
|
|
|
|
|
|
|
|
|
CH2 ~ |
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Sx |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
~ CH2 |
|
|
|
|
|
|
|
|
CH2 ~ |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Sx ~ |
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Возникает сетчатая структура вулканизата, которая содержит поперечные химические связи между макромолекулами, причем в этих связях находится различное количество атомов серы.
Вулканизация эластомеров элементарной серой без ускорителей и активаторов применяется только в некоторых случаях – при производстве эбонита. Эбонит получается в результате нагревания смесей каучука с большим содержанием серы, избыточным по сравнению с эквивалентом двойных связей исходного эластомера. При таком содержании серы и при высоких температурах реакции (до 170˚С) наряду с описанными выше реакциями протекают и другие, вторичные процессы. В эбоните из натурального каучука основная часть серы входит в состав пятичленных тиоциклопентановых колец следующей структуры:
|
|
|
|
CH3 |
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
||||||||
~ CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 ~ |
||||
|
C |
|
CH |
|
CH2 |
|
|
CH2 |
|
C |
|
|
CH |
|
|||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||
|
S |
|
|
|
|
|
|
|
|
S |
|
|
|
|
|
|
|
S |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Эбониты или твердые резины представляют собой жесткий, вязкий материал, обладающий свойствами пластиков.
Сшивание макромолекул каучуков возможно и без серы за счет взаимодействия с веществами типа инициаторов полимеризации (например, органические пероксиды), которые способны оторвать атомы водорода с образованием свободных радикалов. Эти радикалы реагируют друг с другом или с двойной связью, причем образующиеся поперечные углерод-углеродные связи имеют ту же природу, что и химические связи в основной цепи полимера:
RO |
|
|
OR |
|
to |
|
2RO. |
|
|
|
|
|
||||
RO. |
+ ~ CH2 |
|
CH |
|
CH |
|
CH2 ~ |
|
~ CH2 |
|
|
CH |
||||
|
|
|
|
|
||||||||||||
|
|
|
||||||||||||||
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OR |
||
. CH
CH2 ~
~ CH2 |
|
CH |
|
CH |
|
CH2 ~ |
~ CH2 |
|
CH |
|
|
|
|||||||
|
|
|
|||||||
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
OR
~ CH2
CH CH2 ~ ~ CH2 CH CH CH2 ~
|
. |
|
2 ~ |
|||
|
CH |
|
CH |
|
CH |
|
|
|
|
|
|||
http://www.mitht.org
~ CH2 CH CH
OR
~CH2 CH
~CH2
CH2 ~
CH CH2 ~
|
|
CH |
|
CH |
~ |
|
|
|
|||
CH . |
2 |
||||
и т.д.
Таким образом, распадающийся пероксид вызывает процесс, подобный полимеризации и распространяющийся на разные макромолекулы полимера (так называемая кросс-полимеризация).
Как видно из приведенных примеров, для перехода от линейной структуры полимера к сетчатой достаточно минимум одной химической связи между соседними макромолекулами, т.е. одна молекула низкомолекулярного вещества способна вызвать качественное изменение состояния двух макромолекул полимера, связав, их друг с другом. При этом они теряют способность перемещаться в качестве самостоятельной кинетической единицы. ММ малой молекулы сшивающего агента значительно меньше ММ сшиваемых макромолекул полимера, а поэтому уже крайне малые добавки этих агентов приводят к образованию единой структуры сетчатого полимера.
Сшивание макромолекул можно проводить также путем физических воздействий, приводящих к образованию активных центров (радикалов или ионов) на макромолекулах. Например, при облучении ультрафиолетовым светом или при действии γ-лучей на насыщенные и ненасыщенные полимеры образуются свободные радикалы внутри макромолекул. Эти радикалы реагируют друг с другом или с двойными связями других макромолекул, что приводит к возникновению поперечных связей и образованию сетчатой структуры. Механизм этих реакций подобен рассмотренному выше случаю вулканизации каучуков пероксидами.
1.3.Реакции деструкции полимеров.
Кхимическим реакциям, позволяющим широко изменять или модифицировать свойства полимеров, относятся и реакции, связанные с распадом молекулярных цепей, приводящие к образованию продуктов со значительно пониженной ММ или низкомолекулярных веществ. Эти реакции называются реакциями деструкции. Они протекают в полимерах под воздействием тепла, света, излучений высоких энергий, кислорода, озона, механических напряжений и др.
В ряде случаев деструкция полезна: она может использоваться в исследовательских целях - для определения химического состава и строения полимера; для получения блок- и привитых сополимеров при механической обработки смеси двух полимеров; и наконец, для пластикации полимеров с целью облегчения их переработки за счет снижения ММ.
Открытие в 1826 году Т. Гэнкоком явления пластикации каучука, т.е. явления перехода его из эластического состояния в пластическое, сыграло исключительную роль в развитии химии полимеров. Т. Гэнкок попытался размельчать каучуковые изделия в специальном цилиндре с вращающимся внутри него валом. Вал и внутренняя поверхность цилиндра были покрыты зубьями, предназначенными для разрезания каучука. Первые же опыты привели к совершено противоположному результату – вместо того, чтобы измельчаться, каучук собирался в однородную пластичную массу. Пластицированный каучук обнаружил лучшую растворимость, а главное, оказался весьма удобным материалом для придания ему желаемой формы. Появились и более совершенные технологические приемы – каландрование, шприцевание, формование, которые и в настоящее время являются основными при изготовлении резиновых изделий. Эти процессы являются не чисто механическими, а отражают совокупность механохимических процессов распада и соединения длинноцепочечных молекул эластомера под действием сдвиговых усилий и процессов окисления.
http://www.mitht.org

Вследствие больших размеров и линейного строения молекул энергия межмолекулярного взаимодействия в полимерах во много раз превосходит энергию отдельных химических связей. Поэтому при сдвиговых усилиях в молекулярных цепях могут возникнуть напряжения, способные преодолеть энергию валентных связей между атомами цепи. Таким образом, происходит химический акт разрыва молекулярной цепи с образованием двух полимерных радикалов:
~ CH2 |
|
CH |
|
CH |
|
CH2 |
|
|
CH2 |
|
|
CH |
|
CH |
|
CH2 ~ |
напряжение |
|||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
~ CH2 |
|
|
|
|
|
|
. . |
|
|
|
|
|
|
|
CH2 ~ |
||||||||
|
|
CH |
|
|
CH |
|
|
CH2 |
+ |
CH2 |
|
|
CH |
|
|
CH |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
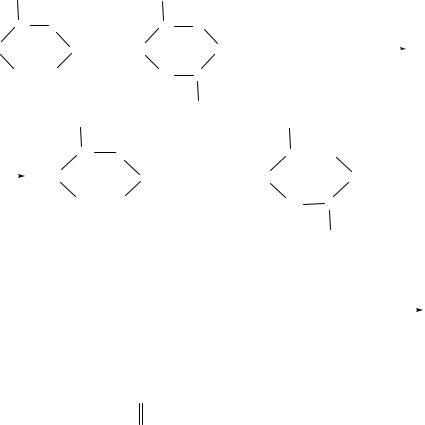
Возникающие при механическом воздействии полимерные радикалы способны принимать участие в химических реакциях. В частности они могут реагировать с молекулами полимера. При этом возможны реакции:
а) отрыва водорода от другой молекулы:
R |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
. |
+ R' |
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
R" |
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
CH2 |
|
|
|
|
|
CH |
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
CH3 |
|
+ R' |
|
|
|
|
|
CH2 |
|
|
|
|
CH |
|
|
|
CH |
|
|
|
. |
R" |
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
б) присоединения к двойной связи (в случае диеновых эластомеров): |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
R |
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
. |
+ |
|
R' |
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
R" |
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
2 |
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
CH |
2 |
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
R' |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R" |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
CH |
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
в) присоединения полимерного радикала по месту отрыва водорода с образованием |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
разветвленных структур: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||
R |
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
. |
+ |
|
R' |
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
. |
|
R" |
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
R' |
|
|
CH2 |
|
|
CH |
|
CH |
|
|
|
|
|
|
|
CH |
|
|
|
|
|
R" |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
г) рекомбинация полимерных радикалов, возникших в результате отрыва водорода, с |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
образованием поперечной связи между макромолекулами: |
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
~ CH2 |
|
|
|
|
CH |
|
|
CH |
|
|
CH ~ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
~ CH2 |
|
|
|
CH |
|
|
CH |
|
|
|
CH ~ |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
~ CH2 |
|
|
|
|
CH |
|
|
CH |
|
|
CH ~ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
~ CH2 |
|
|
|
CH |
|
|
CH |
|
|
|
CH ~ |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
Механохимические |
процессы |
|
|
протекают в |
|
различных условиях переработки и |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
эксплуатации полимеров. В частности, они играют существенную роль при смешении эластомеров с наполнителями, например с сажей. Полимерные радикалы взаимодействуют с активными участками поверхности частиц наполнителя с образованием химической связи между каучуком и наполнителем. Следствием этих реакций является возникновение сажекаучукового геля. Путем механической обработки смесей полимеров или полимеров с жидкими мономерами получают блок- и привитые сополимеры. В ряде случаев
http://www.mitht.org
механическое воздействие на полимер инициирует химические реакции с кислородом или другими низкомолекулярными соединениями, т.е. этот сравнительно недорогой и доступный прием обработки позволяет проводить химическую модификацию полимеров.
Однако, в большинстве случаев деструкция полимеров является процессом нежелательным, т. к. ухудшает физико-механические и другие свойства полимеров.
Процессы деструкции можно классифицировать не только по видам, вызывающих их воздействий, но и по характеру протекания химических реакций в полимерах под действием этих факторов. Если рассматривать деструкцию как процесс, обратный полимеризации, то можно также предложить разделение реакций деструкции на две группы: ступенчатые и цепные. К первой следует отнести такие реакции распада, которые приводят к единичным актам разрыва макромолекул. Разрыв связей протекает по случайному закону, и каждая связь рвется независимо от другой связи.
Чаще всего беспорядочная деструкция наблюдается при действии химических агентов на гетероцепные полимеры. Глубина деструкции зависит от количества низкомолекулярного реагента и времени его воздействия. Такая деструкция может быть остановлена на любой стадии путем снижения температуры, удаления реагента или, наоборот, доведена до предела - до образования устойчивых молекул мономеров. Распад молекул целлюлозы под каталитическим действием кислот протекает по случайному закону:
|
OH |
|
|
|
OH |
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
||||||||||
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|||||||
|
|
CH |
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
||||||||||||
~ CH |
|
|
|
CH |
|
|
O |
|
|
|
CH |
CH |
|
|
O ~ + H2O + H2SO4 |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
CH |
|
|
O |
|
|
|
|
|
|
CH |
CH |
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
||||
|
CH2 OH |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
OH |
|
|
|
OH |
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
CH |
|
O |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
~ CH |
|
O |
CH |
|
OH + HO |
|
|
CH |
CH |
|
|
O ~ |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
CH |
CH |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
CH2 OH |
|
|
|
|
|
|
|
OH |
|
|
|
||||||||||||
Реакция может пойти до образования мономеров (глюкоза) и далее.
Аналогичным образом идет деструкция белков и полиамидов под действием кислот и щелочей:
~ R1 |
|
|
NH |
|
C |
|
|
R |
|
|
C |
|
|
NH |
|
R1 ~ + H2O |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
кислота, щёлочь |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
O |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|||||||
~ R1 |
|
|
NH2 + HO |
|
|
C |
|
|
|
R |
|
|
C |
|
|
NH |
|
R1 ~ |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O O
Деструкция ненасыщенных полимеров под действием озона также протекает по случайному закону в результате активной атаки озоном двойной связи и последующего распада озонидов. Из-за очень высокой скорости взаимодействия озона с двойными связями полимера реакция протекает только на поверхности, что приводить к её растрескиванию.
http://www.mitht.org
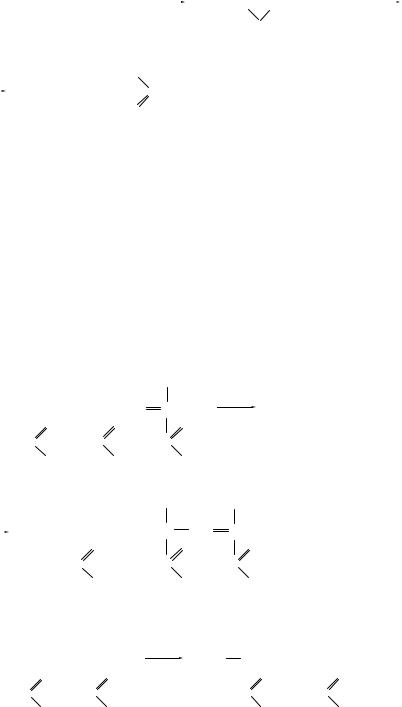
|
|
|
CH3 |
|
|
|
|
|
|
|
CH3 |
|
|||||||||||||||
~ CH2 |
|
|
|
|
|
|
|
|
|
|
CH2 ~ + O3 |
|
|
|
|
~ CH2 |
|
|
|
|
|
|
CH2 ~ |
H2O; спирт |
|||
|
C |
|
CH |
|
|
|
|
|
|
|
|
C |
|
CH |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
to |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O3 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
озонид |
|
|||||
|
|
|
|
|
|
|
|
|
CH3 |
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
~ CH2 |
|
|
|
|
|
|
O + |
|
|
|
CH2~ |
|
|||||||||||||
|
|
|
C |
|
|
|
CH |
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||
O
Ко второй группе реакций деструкции относятся цепные реакции деструкции, т.е. такие, при которых на один акт разрыва полимерной молекулы под действием какого-либо деструктирующего фактора приходится несколько актов распада в других местах цепи. Как и цепная полимеризация, цепная деструкция может протекать по радикальному или ионному механизму. Инициирование цепной деструкции происходит под влиянием факторов, вызывающих образование радикалов или ионов в цепях полимера: под действием тепла, света, излучений высоких энергий, а также химических веществ, распадающихся на свободные радикалы или ионы. Частным случаем цепной деструкции является цепная деполимеризация, протекающая путем последовательного отщепления мономерных звеньев от концов молекулярных цепей и приводящая в итоге к полному переходу полимера в мономер. При этом ММ полимера последовательно уменьшается. Так протекает, например, термическая деструкция полиметилметакрилата, содержащего на концах цепей двойные связи:
|
|
|
|
|
CH3 |
|
|
CH3 |
|
|
|||||||||||||||||
~ CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
CH2 |
|
|
|
C |
|
|
|
|
CH |
|||||||||||
|
|
|
|
|
|
|
|
|
O |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
OCH3 |
|
|
|
|
|
|
OCH3 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|||||||
|
|
~ CH2 |
|
|
|
|
|
|
|
|
|
|
. |
+ |
|||||||||||||
|
|
|
|
C |
|
|
|
|
CH2 |
|
|||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OCH3 |
|
|
||||||
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
CH3 |
|
|
||||||||||||
~ CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
. |
|
|
|
C |
|
|
CH2 |
|
|
C |
|
|
|
CH2 |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
O |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
C |
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
OCH3 |
|
|
|
|
|
|
OCH3 |
|
||||||||||
CH3
C
O
C
OCH3
CH3
C |
CH |
. |
|
O
C
OCH3
to |
~ CH2 |
|
to
CH3
C
O
C
OCH3
CH3 CH3
|
|
. |
|
|
|
CH2 и т.д. |
|
C |
|
CH2 |
+ C |
|
|||
|
|
||||||
|
|
O |
|
|
O |
||
|
|
|
|
||||
C |
|
|
C |
|
|
||
|
|
OCH3 |
|
|
OCH3 |
||
1.4. Старение и стабилизация полимеров.
Комплекс химических и физических изменений полимеров, приводящих к ухудшению их механических свойств и снижению работоспособности изделий из них, называется
старением полимеров.
Одним из основных химических агентов, вызывающих старение органических полимеров, является кислород, который растворим в полимерах, что приводит к протеканию реакций в объёме. Окисление полимеров может активироваться различными факторами: тепловым воздействием (термоокислительное старение), солями металлов переменной валентности (отравление полимера металлами), светом, излучениями высоких энергий
http://www.mitht.org

(световое и радиационное старение), механическими воздействиями (утомление). Распад полимерных молекул может протекать также под действием высоких температур и в отсутствие кислорода (термическая деструкция, деполимеризация и тепловое старение), под влиянием озона (озонное и атмосферное старение), химических веществ, расщепляющих функциональные группы в полимерах, например, путем гидролиза (химическая деструкция).
По механизму цепных реакций развивается также окислительная деструкция полимеров. В развитии цепных реакций окисления основная роль принадлежит пероксидным и гидропероксидным соединениям, которые образуются на первых стадиях взаимодействия кислорода с полимером. По теории А.Н. Баха образование пекроксидов может происходить вследствие активации молекулярного кислорода за счет свободной энергии двойных связей соединения, участвующего в реакции, и превращении молекулы кислорода О=О в группу – О–О–. Установлено, что предельные соединения присоединяют активированные молекулы кислорода в основном к атомам углерода метиленовых групп в α-положении к двойной связи, образуя гидропероксиды:
~ CH2 |
|
CH |
|
CH |
|
CH2 ~ + O2 |
|
~ CH |
|
CH |
|
CH |
|
CH2 ~ |
|
|
|
|
|
|
|
OOH
Гидропероксиды являются автокатализаторами цепной реакции окисления. Как и все цепные реакции, эта схема включает стадии инициирования, роста и обрыва цепи. Главную роль в инициировании играют полимерные гидропероксиды ROOH, которые распадаются или взаимодействуют с молекулой полимера RH:
ROOH |
|
|
. . |
|||
|
|
|
|
RO + OH |
||
|
|
|
|
|
RO + RO + H O |
|
2ROOH |
|
. . |
||||
|
|
|
2 2 |
|||
|
|
|
|
|
. . |
|
ROOH + RH |
|
|
|
R + RO + H2O |
||
Развитие и разветвление цепи происходит в результате взаимодействия образовавшихся полимерных радикалов с кислородом, а так же в результате взаимодействия пероксидных полимерных радикалов с новыми молекулами полимера и отрывом от них атомов водорода, находящихся в α-метиленовой по отношению к двойной связи группе, с образованием новых полимерных радикалов:
. |
|
. |
|
|||
R + |
O2 |
|
|
RO2 |
|
|
. |
|
|
|
|
. |
|
RO2 |
+ RH |
|
|
ROOH + |
R |
|
|
|
|||||
. |
|
|
|
|
. |
|
RO |
+ RH |
|
|
ROH + R |
||
|
|
|||||
. |
+ RH |
. |
|
|||
OH |
|
|
R + H2O |
|
||
|
|
|
||||
Обрыв цепи происходит в результате столкновения двух радикалов и образования неактивных продуктов при их взаимодействии, например:
2R
.
 R R
R R
сшивка
. . |
|
|
R + RO2 |
|
ROOR |
|
||
|
|
пероксид |
Продукты реакций окисления полимеров разнообразны; в них обнаружены органические соединения следующих классов:
http://www.mitht.org
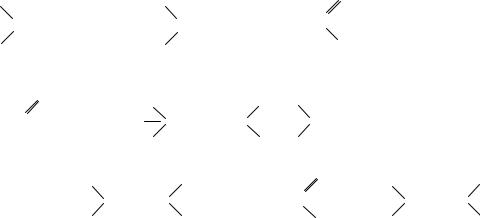
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|||
|
|
|
C |
|
|
|
O |
|
|
OH |
|
|
|
|
|
|
C |
|
|
OH |
|
|
|
|
C |
OH |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
гидропероксиды |
|
|
|
|
|
|
|
спирты |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
кислоты |
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
C |
|
|
|
O |
|
|
R |
|
|
|
|
|
C |
|
|
O |
|
C |
|
|
|
|
|
C |
|
|
O |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
сложные эфиры |
|
|
|
|
|
простые эфиры |
|
|
|
|
кетоны |
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
C |
|
|
|
|
|
|
|
|
C |
|
C |
|
C |
и др. |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
O |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
эпоксиды |
|
|
|
|
|
|
альдегиды |
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пероксиды |
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Проблема стабилизации полимеров - это главным образом проблема поиска эффективных ингибиторов, или стабилизаторов, которые будучи добавлены в полимер в очень малых количествах, не давали бы возможности развиваться нежелательному цепному процессу деструкции макромолекул.
Замедление процесса окисления, исходя из механизма реакции, может идти по двум направлениям: ингибирование инициирования и ингибирование развития и разветвления цепи. В соответствии с этим, противостарители (стабилизаторы, ингибиторы, антиоксиданты) могут быть подразделены на две большие группы: противостарители, ингибирующие инициирование (превентивные противостарители) за счет разложения гидропероксидов, поглощения светового излучения, дезактивации ионов металлов переменной валентности, и противостарители, обрывающие цепи.
Активность ингибиторов зависит от их строения. Многие соединения (меркаптаны, сульфиды, дитиокарбаматы, дитиофосфаты, эфиры фосфористой кислоты и др.) могут ингибировать окисление за счет взаимодействия с гидропероксидами с образованием неактивных продуктов и являются превентивными противостарителями.
Наиболее распространенными противостарителями, которые обрывают цепи, связывая пероксидные радикалы, являются фенолы и амины, способные легко отдавать водород:
ROO· +АН → ROOH+A·
Защитное действие противостарителя будет определяться стабильностью радикала А·, который может в дальнейшем реагировать с другими свободными радикалами, возникающими при окислении полимера, с образованием неактивных продуктов:
R· + А· → RA RO· + А· → ROA
ROO· + А· → ROOA А· + А· → АА
и таким образом задерживать окисление или взаимодействовать со стабильными молекулами с образованием новых радикалов, которые будут осуществлять передачу цепи:
А· + RH → R· + AH
А· + О2 → АОО· + RH → АООН + R·
и соответственно ускорять окисление.
Несмотря на то, что старение вызывается главным образом действием кислорода, единого универсального противостарителя нет. В зависимости от назначения изделий,
http://www.mitht.org
