
органика
.pdf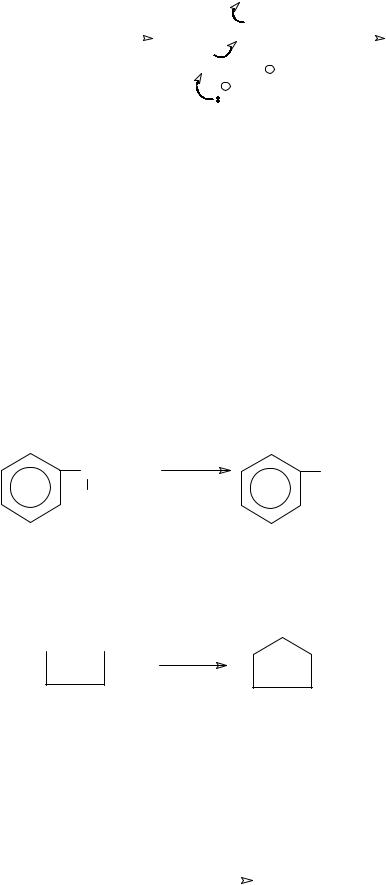
Для вторичных и первичных галогенопроизводных характерен механизм бимолекулярного элиминирования Е2:
|
|
|
KOH, t |
|
|
|
|
|
|
Cl |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
CH3CH2 |
|
CHCH3 |
|
|
CH3 |
CH |
|
|
CHCH3 |
|
|
|
CH3CH=CHCH3 |
|||||||
|
C2H5OH |
|
_H2O |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Cl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
_KCl |
|
||
|
|
|
H |
|
K |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
OH |
|
|
|
|
||||||||
переходное состояние
2.4. Восстановление галогенопроизводных
Восстановление галогенопроизводных до соответствующих углеводородов можно осуществить различными способами:
восстановление водородом в момент выделения
Zn
CH3CH2CH2Br  CH3CH2CH3
CH3CH2CH3
HCl
каталитическое гидрирование
H2, Ni
CHCH3 _HCl CH2CH3
Cl
восстановление комплексными гидридами, например, алюмогидридом лития

 Br LiAlH4
Br LiAlH4
2.5.Реакции галогенопроизводных с металлами
Взависимости от природы металлы реагируют с галогенопроизводными по-разному. При воздействии металлического натрия галогенопроизводные по реакции Вюрца превращаются в алканы, например, из этилхлорида образуется бутан.
2CH3CH2Cl + 2Na |
|
|
CH3CH2CH2CH3 + 2NaCl |
|
|
||
|
21 |
||
|
www.mitht.ru/e-library |
||
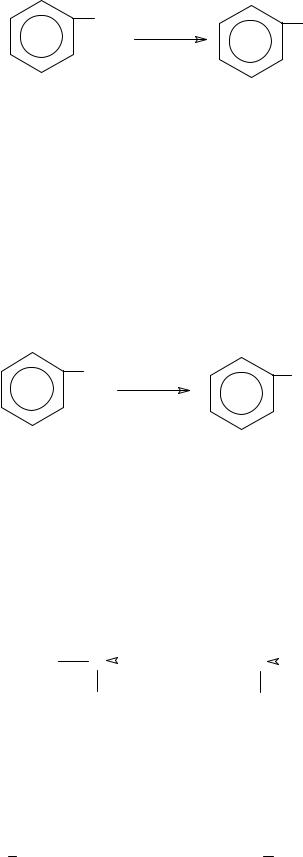
С менее реакционноспособным литием образуются литийорганические соединения, например:
Cl |
2Li |
Li |
|
_LiCl |
|
фениллитий
При нагревании с магнием в диэтиловом эфире алкил- и арилгалогениды превращаются в магнийорганические соединения – так называемые реактивы Гриньяра:
Mg
CH3CH2CH2I  CH3CH2CH2MgI
CH3CH2CH2MgI
пропилмагнийиодид
Br Mg |
MgBr |
фенилмагнийбромид
Металлорганические соединения, такие как литий- и магнийпроизводные углеводородов, являются чрезвычайно реакционноспособными соединениями, которые из-за высокой полярности связи углерод-металл представляют собой сильные С-нуклеофилы.
|
|
|
|
|
|
|
|
C |
Li |
|
C MgX |
||||
|
|||||||
|
|
||||||
Реактивы Гриньяра и литийорганические соединения являются также сильными основаниями и реагируют с соединениями, проявляющими кислотные свойства. Поэтому их синтез проводят только в безводных растворителях, поскольку вода, как кислота, реагирует с этими соединениями, гидролизуя их.
R MgX + H2O  R H + Mg(OH)X
R H + Mg(OH)X
22
www.mitht.ru/e-library
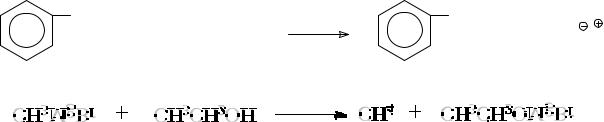
Подобным же образом реактивы Гриньяра реагируют и с другими более или менее сильными кислотами, например, с карбоновыми кислотами или спиртами:
CH2MgCl |
CH3 |
+ CH3COOH |
+ CH3COO MgCl |
3. Задачи и упражнения
1.Напишите формулы всех структурных и конфигурационных изомеров состава С5Н11Сl и назовите их.
2.Приведите способы получения трет-бутилхлорида: а) из 2- метилпропена; б) из 2-метил-2-пропанола.
3.Получите из соответствующих спиртов: а) пара- бромбензилбромид; б) пропилиодид; в) 1-хлорпентан.
4.Предложите схемы следующих превращений: а) пропилхлорида в изопропилхлорид; б) изопропилхлорида в пропилбромид; в) бензола в пара-хлорбензилхлорид; г) 1-хлорпропана в 3-хлор-1- пропен.
23
www.mitht.ru/e-library
5.Напишите уравнения следующих реакций: а) 1-пропанол и тионилхлорид при нагревании; б) втор-бутилбромид и фторид калия; в) 2-хлорпропан и иодид натрия; г) пара-нитротолуол и хлор
на свету; д) толуол и бром в присутствии трибромида алюминия; е) 1-бутен и хлор при 400О С; ж) 1,3-пентадиен и хлороводород.
6.Следующие реакции происходят по механизму SN1; обратите внимание на строение субстрата и растворитель и изобразите эти механизмы: а) трет-бутилхлорид и водный раствор едкого кали; б) аллилбромид и вода; в) бензилхлорид и ацетат натрия в воде; г) (R)-3-хлор-3-метилгептан и водный раствор гидросульфида натрия.
7.Следующие реакции протекают по механизму SN2; обратите внимание на строение субстрата и растворитель и изобразите эти механизмы: а) 1-хлорбутан и нитрит натрия в диметилформамиде; б) бензилхлорид и иодид натрия в ацетоне; в) (S)-2- хлоргексан и цианид натрия в диметилсульфоксиде; г) метилиодид и трет-бутилат натрия в трет-бутиловом спирте.
8.Предположите, по какому механизму осуществляются следующие взаимодействия, и изобразите эти механизмы: а) трет- бутилбромид и водный раствор гидроксида натрия; б) 3-хлор-2- метил-1-пропен и водный раствор ацетата натрия; в) (S)-3-бром- 3-метилгексан и водный раствор едкого натра; г) 1-хлорпропан и иодид натрия в ацетоне; д) (R)-2-хлорпентан и нитрит натрия в диметилформамиде; е) метилиодид и ацетиленид натрия в диметилсульфоксиде; ж) 2,4-динитрохлорбензол и этилат натрия.
9.Напишите уравнения следующих реакций: а) 2-метил-3- хлоргексан и гидроксид калия при нагревании; б) метилбромид и магний; в) (S)-2-хлорбутан и цианид калия; г) бромбензол и литий; д) 1-бутен и бром; е) изопропилбромид и натрий; ж) бензилхлорид и алюмогидрид лития.
24
www.mitht.ru/e-library

СПИРТЫ
Спирты являются производными углеводородов, в которых один или несколько атомов водорода при sp3-гибридных атомах углерода замещены гидроксильной группой. В соответствии с количеством гидроксильных групп различают одноатомные спирты общей формулы R-ОН, где R – углеводородный остаток, и многоатомные спирты, или полиолы (диолы, триолы и т.д.).
В зависимости от того, с каким атомом углерода связана гидроксильная группа, одноатомные спирты подразделяют на первич-
ные, вторичные и третичные, например:
CH3 |
CHCH2OH |
первичный спирт |
|
|
(2-метил-1-пропанол, или изобутиловыйспирт) |
CH3 |
|
|
|
|
|
|
|
|
|
CHCH3 вторичный спирт |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
OH |
(1-фенилэтанол) |
|
|
|
|
|
|
|
|
|
|||
CH3 |
|
|
CH3 |
третичный спирт |
||||||
|
|
|
|
|
|
|
|
|
||
|
C |
|
OH |
|||||||
|
|
|||||||||
|
|
|
|
|
|
|
|
|
(2-метил-2-пропанол, илитрет-бутиловый спирт) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
||||||||
|
|
|
||||||||
1. Способы получения
1.1. Гидратация алкенов
Присоединение воды к алкенам с образованием спиртов является электрофильной реакцией, катализируемой кислотой. Региоселективность реакции, определяемая правилом Марковникова, обусловлена, как и при гидрогалогенировании алкенов, преимущественным протеканием реакции через наиболее устойчивый карбокатион. Так, гидратация 2-метилпропена в присутствии серной кислоты как катализатора приводит к образованию трет-бутилового спирта, поскольку из двух образующихся при протонировании этого алкена карбокатионов более устойчивым является третичный (трет-бутил-катион):
|
|
|
CH3 |
H2O |
|
|
|
CH3 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
CH3 |
|
C |
|
CH2 |
CH3 |
|
C |
|
CH3 |
|||||||
|
|
|
|
|
|
|
|
|
||||||||
|
H |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
25 |
|
|
|
|
|
www.mitht.ru/e-library

Гидратацию алкенов можно осуществить и присоединением серной кислоты с последующим гидролизом образующегося продукта присоединения – алкилсульфата, например:
CH3 |
|
CH=CH2 |
H2SO4 |
CH |
|
CH |
|
CH |
H2O |
|
CH |
|
CH |
|
CH |
|||||
|
|
|
|
_H SO |
|
|
||||||||||||||
|
|
|
|
3 |
|
|
3 |
3 |
|
|
|
|
3 |
|||||||
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
O |
|
SO3H |
2 |
4 |
|
|
OH |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
изопропилсульфат
Так как присоединение серной кислоты к алкенам происходит тоже в процессе электрофильной реакции, то общий результат гидратации и в этом случае – гидратация по правилу Марковникова.
1.2. Гидролиз галогенопроизводных
Алкилгалогениды при гидролизе превращаются в соответствующие спирты. Гидролиз представляет собой нуклеофильное замещение и может быть осуществлен как при непосредственном взаимодействии с водой, так и при взаимодействии с водным раствором щелочи, например:
|
|
|
CH3 |
|
H2O |
|
|
|
|
CH3 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
CH3 |
|
C |
|
CH2CH3 |
|
|
CH3 |
|
C |
|
CH2CH3 |
||||||||
|
|
|
_ |
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
HBr |
|
|
|
|
|
|
|
|
|
|
|
|
|
Br |
|
|
|
|
OH |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
CH3CH2CH2CH2 |
|
Cl |
NaOH, H2O |
CH3CH2CH2CH2 |
|
OH |
|||||||||||||
|
|
_NaCl |
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
В зависимости от строения алкилгалогенида и условий реакции гидролиз может происходить либо по механизму SN1, либо по механизму SN2.
1.3. Восстановление карбонильных соединений
Спирты могут быть получены восстановлением альдегидов и кетонов, причем из альдегидов образуются первичные спирты, а из кетонов – вторичные. Восстановление осуществляют либо водородом на катализаторе, либо комплексными гидридами, такими как алюмогидрид лития (LiAlH4) или боргидрид натрия (NaBH4). Кроме того, алюмогидрид лития может восстановить до первичных спир-
26
www.mitht.ru/e-library
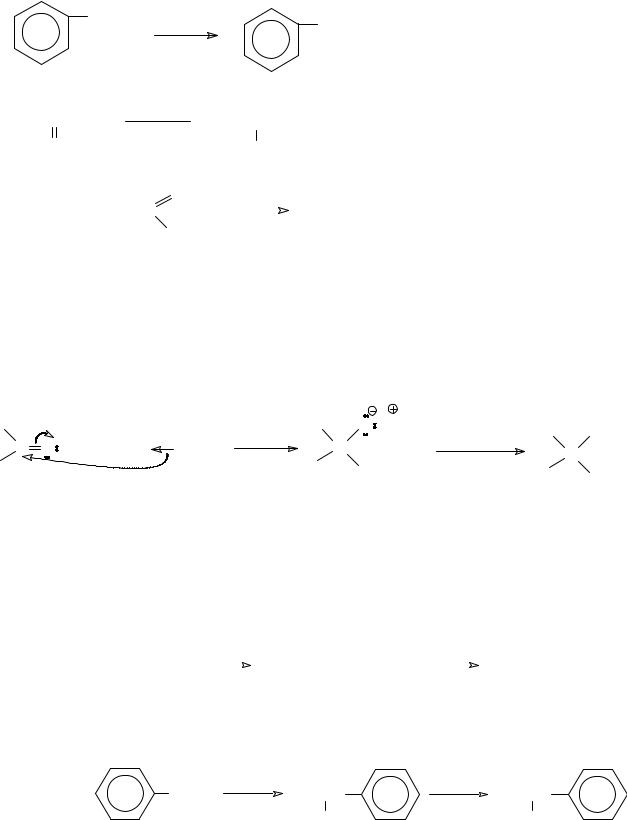
тов карбоновые кислоты и сложные эфиры. Следующие примеры иллюстрируют восстановление карбонильных соединений до спиртов:
CH=O H , Ni |
CH OH |
2 |
|
|
2 |
CH3CCH3 NaBH4 CH3CHCH3
CH3CHCH3
O OH
O LiAlH4
CH3CH2CH2CH2C |
|
CH3CH2CH2CH2CH2 |
|
OH + CH3OH |
|
|
OCH3
1.4. Получение спиртов реакцией Гриньяра
Реактивы Гриньяра присоединяются к карбонильным соединениям – альдегидам и кетонам с образованием алкоголятов, которые при гидролизе превращаются в спирты:
R |
|
+ |
|
|
R |
O MgX |
H2O |
R |
OH |
C O |
|
R" |
MgX |
|
C |
_Mg(OH)X |
R' C |
|
|
R' |
|
|
|
|
R' |
R" |
R" |
Первичные спирты получают взаимодействием реактива Гриньяра с формальдегидом, например, изобутиловый спирт образуется при реакции формальдегида с изопропилмагнийбромидом и последующем гидролизе в соответствии с уравнением:
CH2=O + (CH3)2CHMgBr |
|
(CH3)2CHCH2OMgBr |
H2O |
(CH3)2CHCH2 |
|
OH |
|
|
|
Вторичные спирты получают из альдегидов, например:
CH3CH=O + |
MgCl |
CH3CH |
H2O |
CH3CH |
|||
|
|
OMgCl |
OH |
27
www.mitht.ru/e-library
Для получения третичных спиртов используют взаимодействие кетонов с реактивами Гриньяра. При этом возможно несколько альтернативных схем синтеза одного и того же третичного спирта. Так, например, 3-метил-3-гексанол может быть получен:
из метилэтилкетона и пропилмагнийбромида
CH3 |
|
CCH2CH3 |
1.CH3CH2CH2MgBr |
CH CH |
CH3 |
|
|
|
|
|
|
|
|
|
|||||
|
|
CCH CH CH |
|||||||
|
|
||||||||
|
|
|
2.H2O |
3 |
2 |
|
2 |
2 |
3 |
O |
|
OH |
|
|
|
||||
|
|
|
|
|
|||||
из метилпропилкетона и этилмагнийбромида
CH3CCH2CH2CH3 |
1.CH3CH2MgBr |
CH CH |
CH3 |
|
|
|
|||
|
|
|
|
||||||
|
CCH CH CH |
||||||||
|
|||||||||
|
|
|
2.H2O |
3 |
2 |
|
2 |
2 |
3 |
O |
|
OH |
|
|
|
||||
|
|
|
|
|
|||||
из пропилэтилкетона и метилмагнийбромида
CH3CH2 |
|
|
|
CCH2CH2CH3 |
1.CH3MgBr |
|
CH3 |
||
|
|
|
CH3CH2 |
|
CCH2CH2CH3 |
||||
|
|
|
|
||||||
|
|
|
2.H2O |
|
|
||||
|
|
|
|
||||||
O |
|
OH |
|||||||
|
|
||||||||
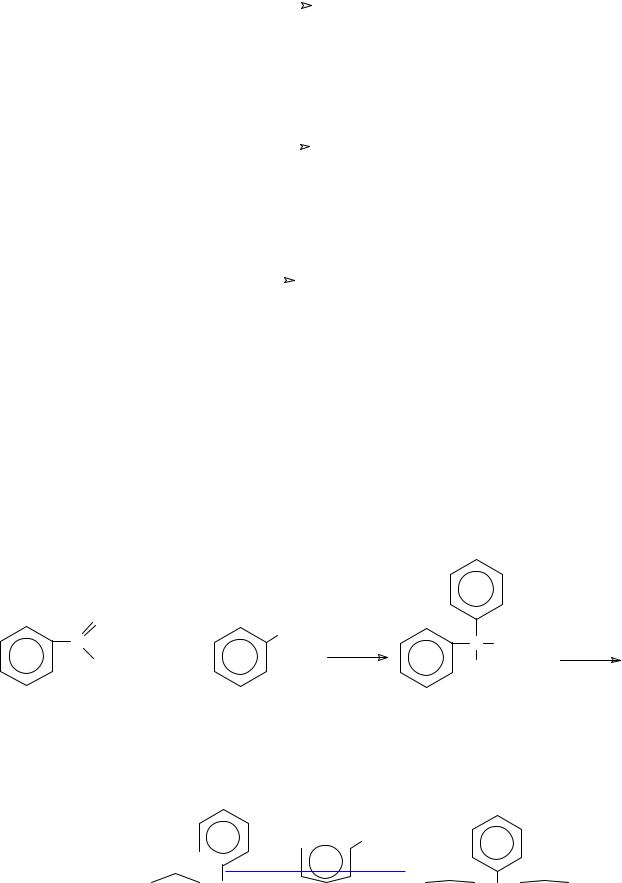
Кроме кетонов для синтеза некоторых третичных спиртов с помощью реакции Гриньяра используются также сложные эфиры. Продукт присоединения реактива Гриньяра к карбонильной группе сложного эфира стабилизируется отщеплением алкоксигруппы (в виде алкоксидмагнийгалогенида), и образующийся кетон присоединяет вторую молекулу реактива Гриньяра. Так, при взаимодействии этилбензоата с двумя эквивалентами фенилмагнийбромида и последующем гидролизе может быть получен трифенилкарбинол (трифенилметанол):
O |
|
MgBr |
C |
|
|
+ |
C OMgBr |
|
OCH CH |
OCH2CH3 |
|
2 3 |
|
28
 MgBr
MgBr  www.mitht1. .ru/e-library
www.mitht1. .ru/e-library
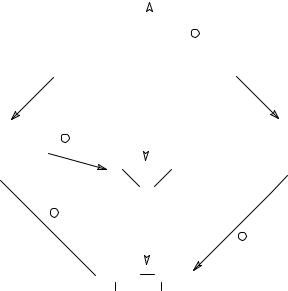
1.5. Получение диолов и триолов
Общие подходы к синтезу диолов и триолов можно рассмотреть на примере простейших представителей этих спиртов – этиленгликоля (1,2-этандиола) и глицерина (1,2,3-пропантриола).
Для получения этих спиртов существует много различных возможностей, основанных на химических реакциях этилена и пропилена. Ниже приведены примеры превращения этилена в этиленгликоль с использованием таких общих реакций алкенов, как присоединение хлора, гипохлорирование, эпоксидирование, а также гидроксилирование с помощью перманганата калия.
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
CH2 |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
OH |
|
OH |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
KMnO4, |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
H2O, |
|
OH |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
Cl2 |
|
|
|
|
|
|
|
|
Cl2 |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
CH =CH |
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
H2O |
2 |
2 |
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
O2 |
|
|
|
|
|
|
|
|||||||||
|
CH2 |
|
|
CH2 |
|
|
|
|
|
|
|
CH2 |
|
|
CH2 |
||||||||||
|
|
|
|
|
|
|
Ag |
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
OH |
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||
Cl |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
Cl |
Cl |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
H2O, |
|
|
|
O |
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2O, |
|
|
||||||
|
|
|
|
|
|
|
OH |
|
|
H2O |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
 CH2 CH2
CH2 CH2
OH OH
При получении глицерина из пропилена осуществляют сначала аллильное хлорирование, затем к аллилхлориду присоединяют хлор в воде, образовавшуюся смесь хлоргидринов действием щелочи превращают в эпихлоргидрин, который на последней стадии
29
www.mitht.ru/e-library

подвергают щелочному гидролизу, при котором происходит и раскрытие водой трехчленного оксиранового цикла.
|
|
|
Cl2, |
|
|
|
|
|
ClCH2 |
|
|
|
|
CH |
|
CH2OH |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
CH3 |
|
CH=CH2 |
ClCH2 |
|
CH=CH2 |
Cl2 |
|
|
|
|
Cl |
|
|
|
|
|
NaOH |
|||||
|
o |
|
H2O |
|
|
|
|
+ |
|
|
|
|
|
|
||||||||
|
|
|
500 C |
ClCH2 |
|
|
|
|
CH |
|
|
|
CH2Cl |
|
|
|||||||
|
|
|
|
аллилхлорид |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
ClCH2 |
|
CH |
|
CH2 |
H2O |
|
HOCH2 |
|
|
CH |
|
CH2OH |
|
|
NaOH |
|
|
|
|||||||
|
|
|
|
|
||||||||
|
|
O |
|
|
OH |
|||||||
|
|
|
|
|
|
|||||||
эпихлоргидрин |
|
|
|
|
|
|
|
|
||||
2. Химические свойства
Все реакции, характерные для спиртов, можно формально разделить на реакции, протекающие с разрывом связи О-Н, и реакции, в которых происходит разрыв связи С-О. В первом случае, т.е. при разрыве связи О-Н молекула спирта проявляет нуклеофильные или кислотные свойства, во втором случае – электрофильные или основные свойства.
2.1. Кислотно-основные свойства
Подобно воде, спирты являются амфотерными соединениями. Они проявляют кислотные свойства, реагируя как О-Н-кислоты с достаточно сильными основаниями.
R O










 H +
H +  B
B 
 R O
R O + H B
+ H B
алкоксид-анион
По кислотным свойствам спирты немного уступают воде (рКа 16-18), поскольку их сопряженные основания – алкоксид-анионы – менее устойчивы в растворе, чем гидроксид-анион, из-за меньшей сольватации. При этом кислотные свойства спиртов уменьшаются в ряду метанол – первичные спирты – вторичные спирты – третичные спирты по этой же причине: более объемные третичные алкоксиданионы менее сольватированы, чем вторичные или, тем более, первичные. Введение электроноакцепторных заместителей в молекулу спирта приводит к усилению кислотных свойств, т.к. такие за-
30
www.mitht.ru/e-library
