Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
«Московский государственный университет тонких химических технологий имени м.В. Ломоносова»
ЦЕНТР КОЛЛЕКТИВНОГО ПОЛЬЗОВАНИЯ
ОСНОВНАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА ПОСЛЕВУЗОВСКОГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ (АСПИРАНТУРА) ПО СПЕЦИАЛЬНОСТИ
05.13.01 – Системный анализ, управление и обработка информации (химическая промышленность)
ОТЧЕТ
ПО ПРОИЗВОДСТВЕННОЙ ПРАКТИКЕ
Аспирант: Трегубов Артём Витальевич
Научный руководитель: Бурляева Елена Валерьевна
Руководитель практики от ЦКП: Городский Сергей Николаевич
Москва 2014
Введение
Цель практики: ознакомление с приборной базой центра коллективного пользования МИТХТ, освоение методов исследования.
Место прохождения практики: центр коллективного пользования МИТХТ.
Задачи практики:
-
Освоение принципов работы приборов, их устройства
-
Пробоподготовка образцов для анализа
-
Проведение испытаний
-
Обработка результатов испытаний
-
Интерпретация полученных данных
Содержание практики
|
№ |
Виды и содержание работ |
Количество часов |
Отметки о выполнение |
|
1 |
Ознакомление с содержанием производственной практикой, ее целями и задачами |
|
|
|
2 |
Инструктаж по правилам охраны труда и внутреннего распорядка |
|
|
|
3 |
Ознакомление с материально-технической базой ЦКП и методологическим обеспечением |
|
|
|
4 |
Спектроскопия ядерного магнитного резонанса(ЯМР) |
|
|
|
5 |
Дифференциальная сканирующая калориметрия(ДСК) |
|
|
|
6 |
Динамический механический анализ(ДМА) |
|
|
|
7 |
Рентгенофазовый анализ(РФА) |
|
|
|
8 |
Работа по специальной научно-методической литературой и написание отчета по производственной практике |
|
|
|
9 |
Итоговая аттестация за производственную практику |
|
|
Спектроскопия ядерного магнитного резонанса (ямр)
Цель работы
Получение ЯМР спектра исследуемого вещества. Калибровка относительно внутреннего стандарта. Фурье – преобразование спектра. Интегрирование пиков спектра. Сопоставление пиков с предполагаемой структурой.
Теоретические основы метода
ЯМР - явление резонансного поглощения радиочастотной электромагнитной энергии веществом с ненулевыми магнитными моментами ядер, находящимся во внешнем постоянном магнитном поле. Ненулевым ядерным магнитным моментом обладают ядра Н1, Н2, С13, N14, N15, F19, Si29, P31 и др. [1]
ЯМР обычно наблюдается в однородном постоянном магнитном поле, на которое накладывается слабое радиочастотное поле перпендикулярное исходному полю. Для веществ, у которых ядерный спин I= 1/2 (Н1, Н2, С13, N14, N15, F19, Si29, P31 и др.).
Такие ядра представляют собой магнитный диполь, тогда в простейшем случае (протон) происходит расщепление:
δE=±μzB0
И разность энергии спиновых состояний:
ΔE=2 μzB0
Где B0 – магнитное поле, μz– zкопонента магнитного кванотового числа.
Особенности ЯМР:
- Высокая разрешающая способность – на десять порядков больше, чем у оптической спектроскопии.
- Возможность вести количественный учет (подсчет) резонирующих ядер. Это открывает возможности для количественного анализа вещества.
- Спектры ЯМР зависят от характера процессов, протекающих в исследуемом веществе. Поэтому эти процессы можно изучать указанным методом. Причем доступной оказывается временная шкала в очень широких пределах – от многих часов до малых долей секунды.
- Современная радиоэлектронная аппаратура и ЭВМ позволяют получать параметры, характеризующие явление, в удобной для исследователей и потребителей метода ЯМР форме. Данное обстоятельство особенно важно, когда речь идет о практическом использовании экспериментальных данных.
Главным преимуществом ЯМР по сравнении с другими видами спектроскопии является возможность преобразования и видоизменения ядерного спинового гамильтониана по воле экспериментатора практически без каких-либо ограничений и подгонки его под специальные требования решаемой задачи. Из-за большой сложности картины не полностью разрешенных линий многие инфракрасные и ультрафиолетовые спектры невозможно расшифровать. Однако в ЯМР преобразование гамильтониана таким образом, чтобы можно было подробно проанализировать спектр, во многих случаях позволяет упростить сложные спектры.
Идентификацию сигналов того или иного протона в молекуле производят посредством определения химического сдвига - смещение сигнала ЯМР в зависимости от химического состава вещества, обусловленное экранированием внешнего магнитного поля электронами атомов. При появлении внешнего магнитного поля возникает диамагнитный момент атомов, обусловленный орбитальным движением электронов. Это движение электронов образует эффективные токи и, следовательно, создает вторичное магнитное поле, пропорциональное в соответствии с правилом Ленца внешнему магнитному полю и противоположно направленное. Данное вторичное поле накладывается на внешнее магнитное поле вблизи ядра и в результате локальное магнитное поле в том месте, где находится атомное ядро, уменьшается.[2]
Принцип работы прибора
Сердцем спектрометра ЯМР является мощный магнит. Образец, помещенный в стеклянную ампулу диаметром около 5 мм, заключается между полюсами сильного электромагнита. Затем, для улучшения однородности магнитного поля, ампула начинает вращаться, а магнитное поле, действующее на нее, постепенно усиливают. В качестве источника излучения используется радиочастотный генератор высокой добротности. Под действием усиливающегося магнитного поля начинают резонировать ядра, на которые настроен спектрометр. При этом экранированные ядра резонируют на частоте чуть меньшей, чем ядра, лишенные электронных оболочек. Поглощение энергии фиксируется радиочастотным мостом и затем записывается самописцем. Частоту увеличивают до тех пор, пока она не достигнет некого предела, выше которого резонанс невозможен.[3]
.
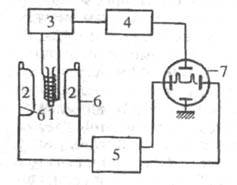
Рис.1. Схема спектрометра ЯМР.[4]
1 - катушка с образцом;
2 - полюса магнита;
3 - генератор радиочастотного поля;
4 - усилитель и детектор;
5 - генератор модулирующего напряжения;
6 - катушки модуляции магнитного поля;
7 - осциллограф.
В спектрометре Bruker DPX 300 используется импульсный вариант возбуждения ядер, осуществляют его не «постоянной волной», а с помощью короткого импульса, продолжительностью несколько микросекунд. Амплитуды частотных компонент импульса уменьшаются с увеличением расстояния. Но так как желательно, чтобы все ядра облучались одинаково, необходимо использовать «жесткие импульсы», то есть короткие импульсы большой мощности. Продолжительность импульса выбирают так, чтобы ширина частотной полосы была больше ширины спектра на один-два порядка. Мощность достигает нескольких тысяч ватт.
Прибор калибруют используя внутренний стандарт –триметилсилан.
В результате импульсной спектроскопии получают не обычный спектр с видимыми пиками резонанса, а изображение затухающих резонансных колебаний, в котором смешаны все сигналы от всех резонирующих ядер — так называемый «спад свободной индукции» (FID, free induction decay, Рис. 2).
Для преобразования данного спектра используют математические методы, так называемое фурье-преобразование, по которому любая функция может быть представлена в виде суммы множества гармонических колебаний.
После Фурье – преобразования полученный спектр интегрируют (Рис. 3). Если структура соединения предполагается известной то выбирается калибровочный пик (на рисунке крайний справа триплет СН3 – групп).

Рис.2. ЯМР спектр до Фурье-преобразования.

Рис.3. Н1-ЯМР спектр после преобразования.
Пробоподготовка
Для того, чтобы провести анализ, подбирают растворитель для исследуемого вещества. После упаривания растворителя растворяют 10 – 20 мг исследуемого вещества в аналогичномдейтерированном растворителе. Это делается чтобы сигналы H1 растворителя свести к минимуму. Раствор помещают в специальную ампулу (Рис. 4). Уровень раствора в ампуле должен быть около 3-5 см (≈0.6-1 см3 раствора).
Рис. 4. Ампулы для ЯМР.
Использование полученных данных
После
интегрирования спектра следует определить
соответствие пиков и резонирующих ядер.
Для этого используют известную величину
химического сдвига в миллионных долях,
пользуясь таблицами, схемами (Рис. 5),
компьютерными программами. По интенсивности
пиков определяют количество ядер той
или иной группы.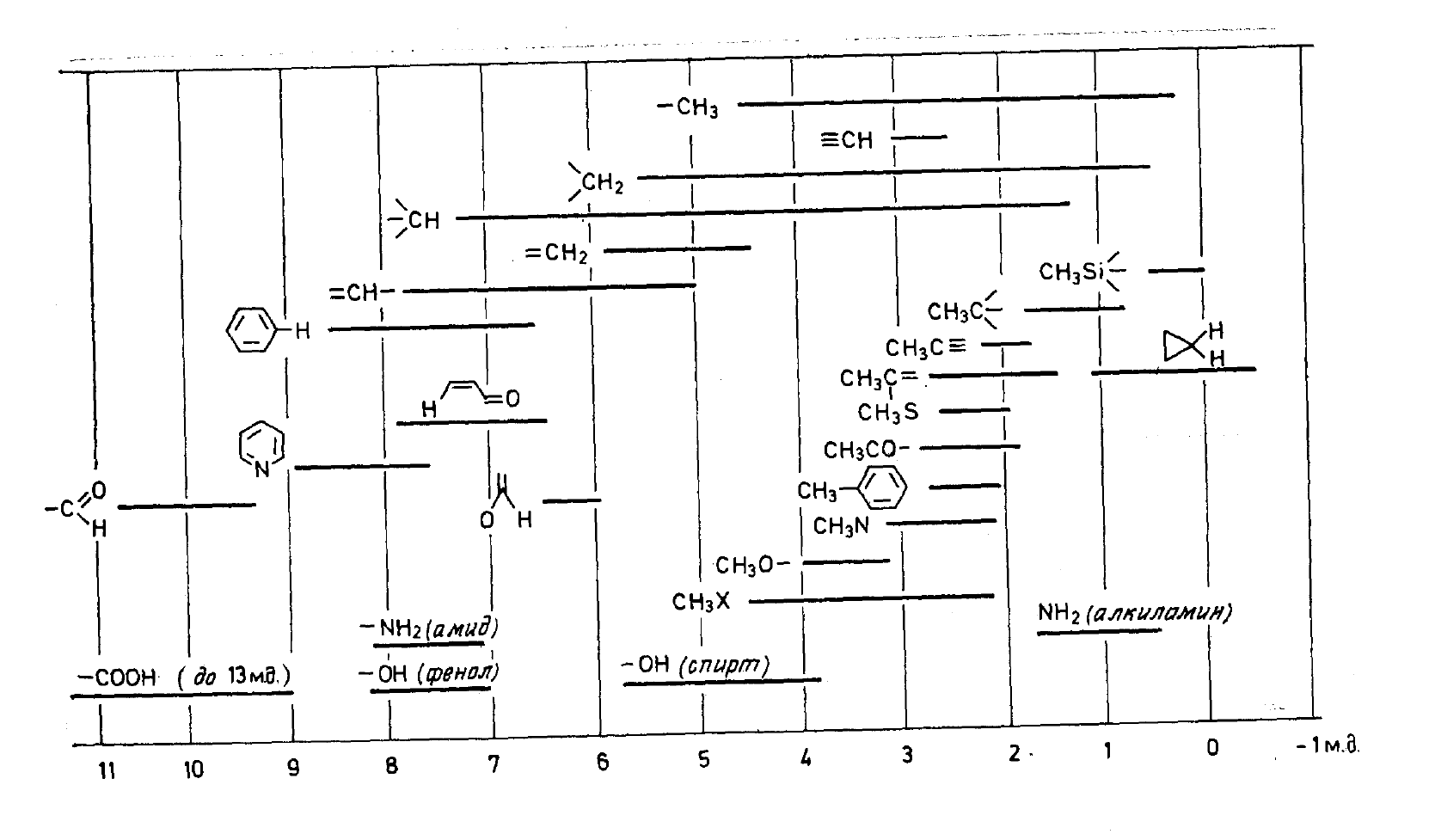
Рис. 5. Химический сдвиг для протонов различных групп.
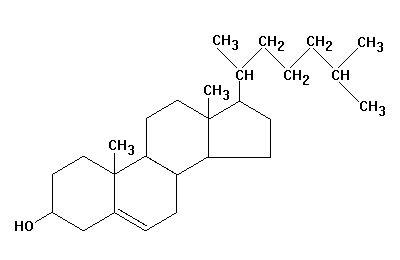
На рисунках 6 и 7 пример водородного и углеродного ЯМР спектров для молекулы холестерина